2024年3月12日国家药监局批准舒格利单抗注射液(Sugemalimab、择捷美/Cejemly)联合含氟尿嘧啶类和铂类药物化疗用于一线治疗表达PD-L1的胃及胃食管结合部腺癌
2024年3月12日国家药监局批准舒格利单抗注射液(Sugemalimab、择捷美/Cejemly)联合含氟尿嘧啶类和铂类药物化疗用于一线治疗表达PD-L1的胃及胃食管结合部腺癌
2024年3月12日,中国国家药品监督管理局(NMPA)批准辉瑞/基石药业的创新性免疫治疗药物舒格利单抗注射液(Sugemalimab、择捷美/Cejemly)联合含氟尿嘧啶类和铂类药物化疗用于表达PD-L1(综合阳性评分[CPS]≥5)的不可手术切除的局部晚期或转移性胃及胃食管结合部腺癌(G/GEJ)的一线治疗。这是全球首个针对该适应症获批的PD-L1单抗,标志着胃癌治疗迈入精准免疫时代。
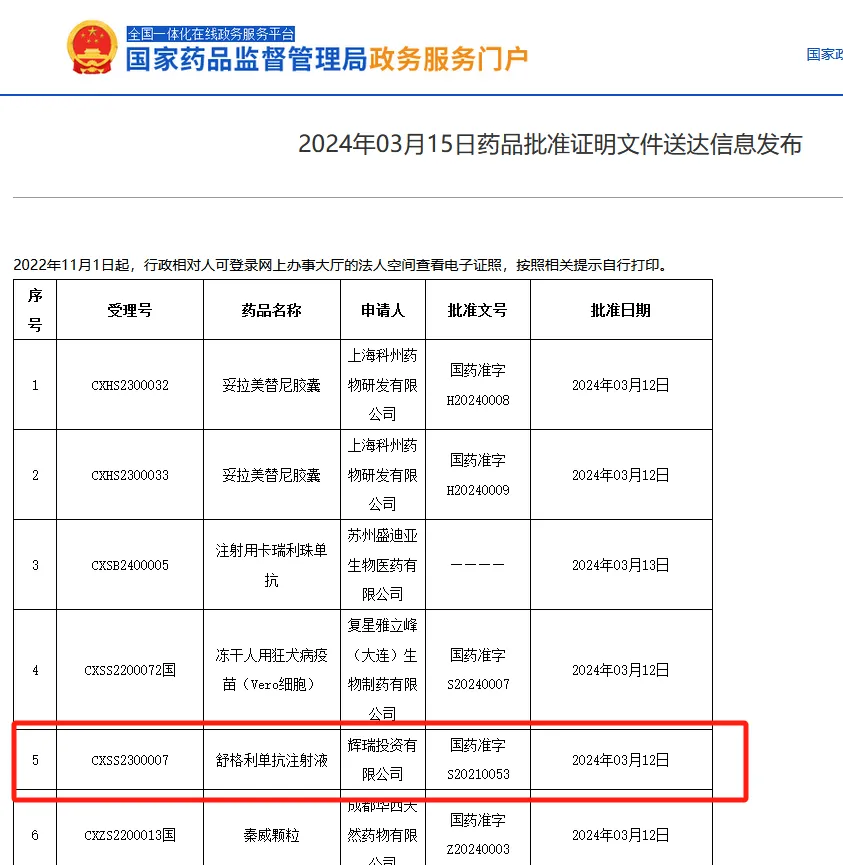
获批依据
舒格利单抗的此次获批主要基于一项名为GEMSTONE-303的III期临床试验,该研究是首个使用PD-L1单抗达成PFS和OS双终点阳性的临床研究,其设计严谨,结果可靠,为舒格利单抗在晚期G/GEJ腺癌一线治疗中的应用提供了强有力的证据。
研究设计
研究类型:多中心、随机、双盲、安慰剂对照的III期临床试验;
研究人群:既往未经治疗、HER2 阳性状态不明、PD-L1 表达≥5%、不可切除的晚期或转移性G/GEJ腺癌患者;
分组情况:按照ECOG PS(0 或 1)和PD-L1 CPS评分(5-9%或≥10%)进行分层,1:1随机分配至舒格利单抗+CAPOX组和安慰剂+CAPOX组;
治疗药物:舒格利单抗(1200mg,Q3W,IV)或安慰剂联合CAPOX(卡培他滨,1000mg/㎡,口服,BID,D1-14,Q3W;奥沙利铂,130mg/㎡,IV,Q3W;最多6个周期);
主要研究终点:研究的主要终点是无进展生存(PFS)和总生存(OS),PFS是指从随机化到疾病进展或死亡的时间,OS是指从随机化到死亡的时间,这两个指标是评估肿瘤治疗效果的重要标准,能够全面反映药物对患者生存状况的影响;
次要研究终点:次要研究终点包括客观缓解率(ORR)、缓解持续时间(DoR)及12个月和24个月的OS率,ORR是指完全缓解(CR)和部分缓解(PR)的患者比例,反映了药物的短期疗效;DoR是指从首次缓解到疾病进展或死亡的时间,反映了药物的持续疗效;OS率则是指在特定时间点仍存活的患者比例,进一步验证了药物的长期疗效。
研究结果
无进展生存期(PFS):舒格利单抗+CAPOX组的中位PFS为7.62个月,显著优于安慰剂+CAPOX组的6.08个月(HR=0.66,P<0.0001),在CPS≥10的人群中,PFS获益更为明显(7.79个月vs 5.52个月, HR=0.58,P=0.0001),这一结果表明,舒格利单抗联合化疗显著延长了患者的无进展生存期,尤其在PD-L1高表达人群中效果更为显著。
总生存期(OS):舒格利单抗+CAPOX组的中位OS为15.64个月,显著优于安慰剂+CAPOX组的12.65个月(HR=0.75, P=0.0060);在CPS≥10人群中,中位OS延长5.36个月,降低死亡风险36%(17.81个月vs12.45个月, HR=0.64, P=0.0022);这一结果表明,舒格利单抗联合化疗显著延长了患者的总生存期,尤其在PD-L1高表达人群中效果更为显著。
客观缓解率(ORR):舒格利单抗+CAPOX组的ORR达68.6%,在CPS≥10患者中更是高达71.4%,较安慰剂+CAPOX组提升近23%;这一结果表明,舒格利单抗联合化疗显著提高了患者的客观缓解率,尤其在PD-L1高表达人群中效果更为显著。
缓解持续时间(DoR):舒格利单抗+CAPOX组的中位DoR为6.87个月,显著优于安慰剂+CAPOX组的4.63个月;这一结果表明,舒格利单抗联合化疗不仅提高了患者的缓解率,还延长了缓解的持续时间。
安全性:舒格利单抗联合化疗方案总体安全性良好,不良反应可控,未发现新的安全信号;这一结果表明,舒格利单抗联合化疗具有良好的耐受性和安全性,患者可以放心使用。
舒格利单抗简介
舒格利单抗作为一种全人源、全长的IgG4抗PD-L1单克隆抗体,通过以下双重抗肿瘤机制,展现了优异的临床疗效和安全性:
1.阻断PD-1/PD-L1信号通路
舒格利单抗通过抗体Fab段结合肿瘤细胞表面的PD-L1,阻断PD-1/PD-L1信号通路,抑制T细胞抑制信号,增强T细胞抗肿瘤作用,这一机制使得免疫系统能够更有效地识别和攻击肿瘤细胞。
2.激活抗体依赖的细胞介导的吞噬作用(ADCP)
舒格利单抗通过抗体Fc段结合巨噬细胞表面的FcγR,激活ADCP作用,诱导巨噬细胞进一步杀伤肿瘤,ADCP作用的实现,可使免疫系统发挥更大的作用,进一步增强抗肿瘤效果。
3.避开抗体依赖的细胞介导的细胞毒作用(ADCC)
舒格利单抗避开了ADCC作用,减少了不必要的细胞毒性,从而提高了治疗的安全性。
4.低免疫原性和抗原性
作为人源化抗体,舒格利单抗的抗原性相对较小,产生抗抗体的几率明显减少,进一步增强了其疗效和安全性。
舒格利单抗在中国获批的适应症
截至目前,舒格利单抗在国内已相继获批五项适应症:
●联合化疗一线治疗转移性鳞状和非鳞状非小细胞肺癌(NSCLC)患者;
●治疗同步或序贯放化疗后未出现疾病进展的、不可切除、III期非小细胞肺癌患者;
●治疗复发或难治性结外NK/T细胞淋巴瘤患者;
●联合氟尿嘧啶类和铂类化疗药物一线治疗不可切除的局部晚期,复发或转移性食管鳞癌患者;
●联合含氟尿嘧啶类和铂类药物化疗用于表达PD-L1(综合阳性评分[CPS]≥5)的不可手术切除的局部晚期或转移性胃及胃食管结合部腺癌的一线治疗。
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
里程碑!mRNA-4157联合派姆单抗让
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

刚刚!"双免王炸"纳
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2025肺癌生存新希望:六大"
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
早期甲状腺癌术后五年生存率超99%,但要
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
早期甲状腺癌术后五年生存率超99%!但忽
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




