晚期实体瘤迎来新希望!大名鼎鼎的TILs疗法正式在国内开展临床
晚期实体瘤细胞免疫治疗,肿瘤浸润淋巴细胞TILs疗法临床试验招募正式开展
提起近两年声名大噪的的免疫疗法,很多人可能都已经知道PD-1和CAR-T,但这只是冰山一角。在实体肿瘤中最具潜力的TILS(肿瘤浸润淋巴细胞)疗法LN-145已获得了FDA授予的突破性疗法称号,用于治疗化疗后复发的晚期宫颈癌患者,预计这款疗法将在2020年第三季度上市,一旦获批,这将成为实体肿瘤首款获批的过继性细胞免疫疗法。业内专家估计这款相当于量身定制的免疫疗法价格也会较高,约在70000~80000美金,对于大部分国内的患者来说遥不可及。
近日,国内的患者终于迎来希望,这款专门针对于实体肿瘤的TILs疗法终于在国内正式开展临床试验了,据全球肿瘤医生网医学部了解,国内的TILs疗法是在传统肿瘤浸润淋巴细胞(TIL)疗法基础上经过改良,并进一步给予基因修饰,提升其克服肿瘤微环境和增加自我扩增的能力,在前期的概念验证临床研究中已取得了非常积极的疗效和安全性,目前已获得批准正式开展人体临床试验招募患者,想了解详情的病友可以咨询全球肿瘤医生网医学部。
深度科普:肿瘤TILs疗法的前世今生
01、开创者-免疫界泰斗Rosenberg
过继性T细胞疗法--TIL细胞疗法是由免疫界泰斗Rosenberg及其团队开创的新方法。
资料显示,老爷爷今年已经78岁了,是世界著名的癌症学和免疫学专家,也是美国癌症研究院(NCI)的外科主任。
Rosenberg认为,癌细胞入侵时,自身的免疫系统会试图打败体内蔓延的肿瘤。
过去三十年间,他和他的团队一直在致力做一件事情:如何发现并放大“打败”工作做得最好的那部分免疫系统细胞。这就是TIL--肿瘤浸润的淋巴细胞.

Steven Rosenberg(NCI)
02、TIL-体内杀伤能力最强的免疫细胞
TIL(Tumorinfiltrating lymphocytes)指肿瘤浸润的淋巴细胞。
在癌症的早期阶段,免疫系统试图通过动员淋巴细胞的特殊免疫细胞来攻击肿瘤。在手术切除的肿瘤组织中,我们发现大部分是肿瘤细胞,也有少部分淋巴细胞。这些淋巴细胞中有部分是针对肿瘤特异性突变抗原的T细胞,Rosenberg博士认为它们才是深入到敌军内部打击能力最强的免疫细胞,但是由于一些原因(比如肿瘤微环境和PD-1),他们的功能受到了抑制,不能在肿瘤组织中有效的杀伤肿瘤细胞。但是,科学家通过一些体外培养方法把这些肿瘤组织中的某类型的淋巴细胞富集起来,再回输给患者,就能够发挥抗肿瘤作用,而且联合PD-1效果会更好。
03、1988年,实体肿瘤的克星-TILs疗法的诞生
1986年的体外研究表明,从手术切除的恶性黑色素瘤中获得的人源TILs含有能够特异性识别自体肿瘤的T淋巴细胞,当存在大量的肿瘤浸润淋巴细胞时,表明机体启动了对抗肿瘤的免疫反应。
这些研究使得Rosenberg1988年首次证明使用自体TILs的过继性T细胞疗法可以介导转移性恶性黑色素瘤患者的肿瘤客观消退。这意味着,实体肿瘤的克星-TILs疗法正式诞生。
目前,美国国家癌症研究所NCI在这方面已经取得了非常大的成功,并且已在其他主要癌症中心实施治疗,例如Moffitt癌症中心。
2011年,美国国家癌症研究所(NCI)外科主任Steven A. Rosenberg团队发表在国际顶级期刊《Clinical cancer research》上的对于转移性黑色素瘤的2期临床研究显示,TIL治疗黑色素瘤患者的客观缓解率(ORR)为56%,完全缓解率(CR)高达24%。并且研究表明,浸润肿瘤的免疫细胞数量与患者的生存机会成正比。黑色素瘤是具有相对高的突变负荷的癌症之一,肿瘤被这些免疫细胞润,参与早期试验的一些患者对这种疗法的反应持续了十多年。

此后,Iovance公司基于自体肿瘤浸润淋巴细胞(TIL)专门针对黑色素瘤研发了Lifileucel(LN-144)免疫疗法。
2019年,FDA授予肿瘤浸润淋巴细胞(TIL)治疗方法LN-145为突破性的治疗指定,这是用于实体瘤的细胞免疫疗法首次获此殊荣,相信距离上市也仅是时间问题,一旦FDA批准,这将是首款用于实体瘤的细胞免疫疗法,将给癌症患者带来巨大的生存获益。
04、TILs疗法与其他细胞免疫疗法有何不同
和CAR-T一样,TILs属于过继性免疫治疗的一种,但是这是一种赶超CAR-T的新型实体瘤T细胞疗法。
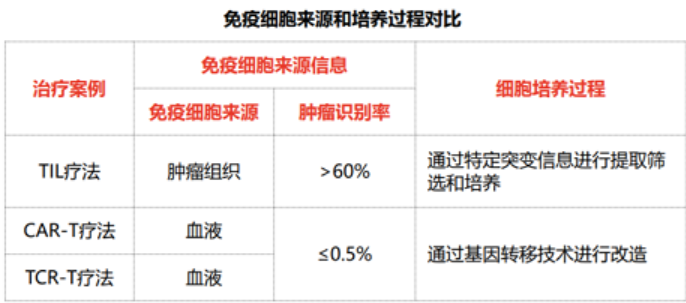
1.识别杀伤能力更强
TIL的免疫细胞来自于肿瘤组织,其自然靶向该患者肿瘤特异性抗原。而其他细胞免疫疗法大部分来取自血液,这直接决定了免疫细胞识别肿瘤的能力。据估计,肿瘤里分离出的免疫细胞,有60%以上能识别肿瘤,而血液里面分离的免疫细胞,不到0.5%。
2.细胞培养过程不同
这种新型的疗法不是像传统的简单的扩增回输,而是要确定患者病例中特定的突变。之后利用突变信息找到能够最有效瞄准这些突变的T细胞,最后提取出专门患者肿瘤中细胞突变的T细胞,这些细胞具有精准识别癌细胞的能力。相比之下,CAR-T和TCR-T中用于治疗的T细胞是通过基因转染技术改造的外周血T细胞,是进行修饰而非筛选培养,因此,精准识别的能力与TIL细胞相差甚远。
3.扩增数量庞大
TILs细胞经过分离筛选后,会加入白细胞介素2进行培养,增加免疫细胞存活的几率,最大限度的扩增免疫细胞,达到数百亿~数千亿级别,确保T细胞的有效性和活性后重新注入到患者体内。同时,研究人员发现联合另一种“明星抗癌药”PD-1抑制剂Keytruda,Keytruda即属于另一种免疫疗法免疫检查点阻断,在某些癌症中有更加显著的效果。
05、TILs疗法的治疗流程
第一步,我们得到病人的肿瘤组织块,其中混杂着体积较大的肿瘤细胞(浅蓝色)以及体积小而圆的T淋巴细胞(红色,绿色,深蓝色);
第二步,肿瘤样本被运送到专有的GMP设施,在那里TIL被分离并繁殖,将不同种类的T淋巴细胞在细胞板上克隆化,并加入高浓度的IL-2来选择培养,在三周内产生数十亿TIL。
第三步,在IL-2的刺激下不同种类的T淋巴细胞都得到了克隆扩增,形成了细胞群;
第四步,用病人的肿瘤细胞和扩增后的T淋巴细胞反应,凡是能够发生杀瘤效应的T淋巴细胞群作为阳性TIL群留下(红色),其余的丢弃(绿色,深蓝色);
第五步,用负载了肿瘤特异性抗原的树突状细胞(DC)进一步扩增培养肿瘤特异性的TIL;
第六步,患者开始一周的预处理治疗(清髓)以准备接受TIL.TIL产品作为一次性疗法施用,在TIL输注后立即接受多达6剂白细胞介素2(IL-2),来支持患者体内TIL的生长和激活。
TILs疗法在各类实体肿瘤中的临床数据
TILs疗法对于多种临床上难治的实体肿瘤取得了惊艳四座的临床效果。去年的ASCO会议上,基于TILS细胞的美国创新型疗法LN-145和LN-144(Lifileucel)在治疗宫颈癌和黑色素瘤的临床结果一经公布,就引起了医学界的广泛关注,其中黑色素瘤中的TIL治疗具有持续数十年的完全应答(CR)的潜力,这种长期的作用归功于记忆T细胞的持久性并在各类实体肿瘤中取得了突破性进展。
一,黑色素瘤
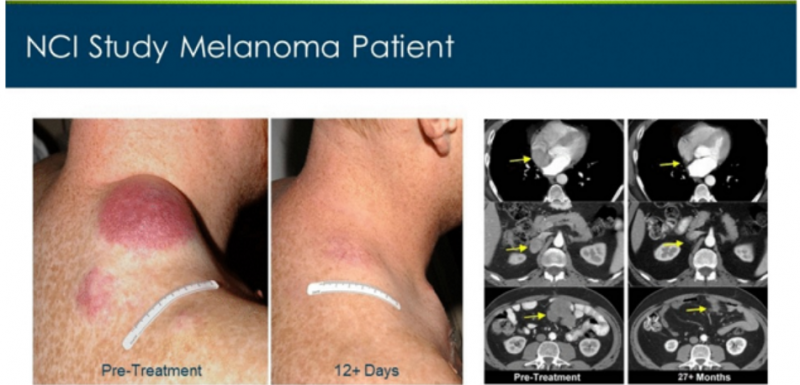
2009年Rosenberg教授发表的针对黑色素瘤的三项连续的临床试验中,接受TILs治疗的客观缓解率在49%至72%之间。其中25名接受TILs疗法的试验中,有7名(28%)达到了完全缓解!值得一提的是,完全患者的患者大部分可达到临床治愈!其中一位患者在接受治疗的12天肿瘤就出现了迅速的缩小。
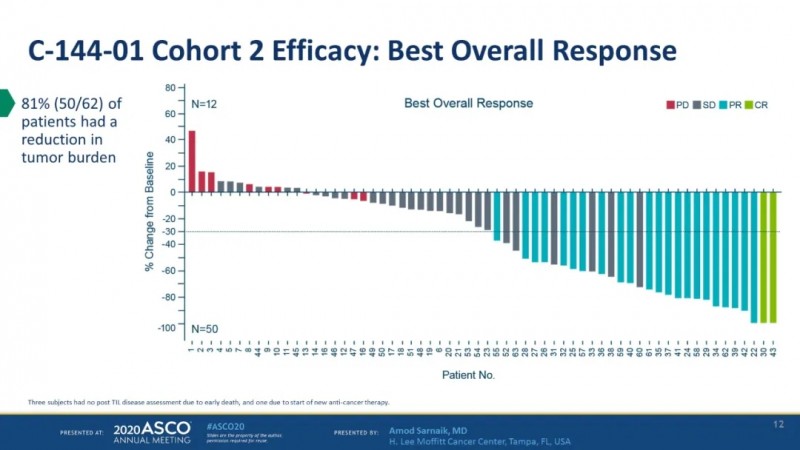
在今年的ASCO会议上,基于TILS细胞的创新型疗法LN-144(Lifileucel)更新了黑色素瘤的临床结果,再次引起了轰动。
C-144-01是一项2期临床试验,招募66名已被诊断患有IIIc期或IV期转移性黑色素瘤的患者。这些患者的特点是至少接受了3~4种全身性治疗都失败后的患者,所有人都接受过PD-1抑制剂治疗,80%接受过CTLA-4抑制剂 ,23%的患者接受过BRAF / MEK抑制剂,可以说是临床上用尽了治疗方案,山重水复疑无路的极晚期患者。还有44%的患者存在肝或脑转移。
该临床试验旨在确定TIL治疗疗法LN-144是否安全有效地治疗转移性黑色素瘤(帮助患者延长寿命和/或减缓癌症进展)。
这些患者在接受手术后,将肿瘤组织中的TIL细胞进行培养后回输,平均注入的TIL细胞:28 x 10^9;IL-2剂量:6次。
实验结果
不负众望!在最新报道的66例接受过PD-1治疗晚期黑色素瘤患者的试验中,结果显示:
1.疾病控制率(DCR)高达80.3%;
2.客观缓解率达到36.4%;
3.中位随访时间为8.8个月,未达到中位反应持续时间。
更引人注目的是,患有PD-L1阴性的患者也有响应,这说明对免疫检查点抑制剂无效的患者仍能获益于TIL疗法。
对于PD-1治疗后进展的患者,几乎没有其他治疗选择,这种治疗方案的效果几乎无与伦比。
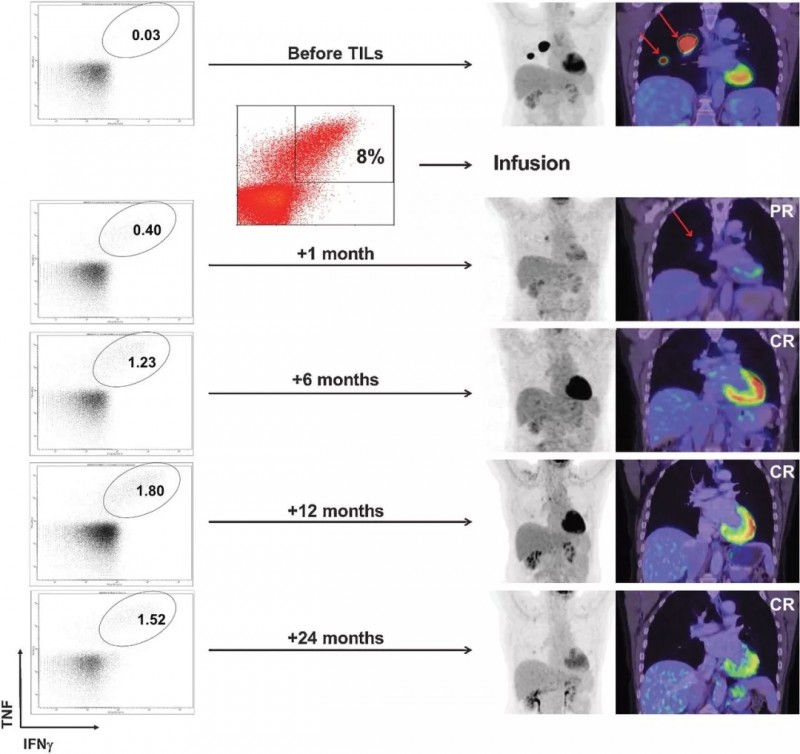
一位晚期黑色素瘤患者肿瘤在治疗前出现广泛转移,在接受TILs疗法后一个月病灶明显缩小,治疗6个月达到完全缓解,治疗两年后仍然处于完全缓解状态,并且体内持续存在肿瘤反应性CD8 + T细胞。
二,宫颈癌-首次获FDA突破治疗指定,有望上市
Iovance公司基于自体肿瘤浸润淋巴细胞(TIL)研发的另一款针对其他实体肿瘤的疗法称为LN-145。
2019年6月,FDA基于innovaTIL-04(C-145-04)积极的试验的数据,治疗晚期宫颈癌患者的反应率(ORR)高达44%,授予肿瘤浸润淋巴细胞(TIL)治疗方法LN-145为突破性的治疗指定,这是用于实体瘤的细胞免疫疗法首次获此殊荣。Iovance Biotherapeutics公司与FDA进行讨论之后宣布重大喜讯:FDA支持LN-145治疗晚期宫颈癌的监管申请。这一反馈让Iovance公司可能在2020年下半年为LN-145递交生物制剂许可申请(BLA),加快其上市的进程,一旦FDA批准,这将是首款用于实体瘤的细胞免疫疗法,将给癌症患者带来巨大的生存获益。
第二阶段innovaTIL-04(C-145-04)积极的试验在2019年2月4日的数据截止时,有27名可评估的患者。平均注入的TIL细胞:28 x 109;IL-2剂量:6次。
结果显示:
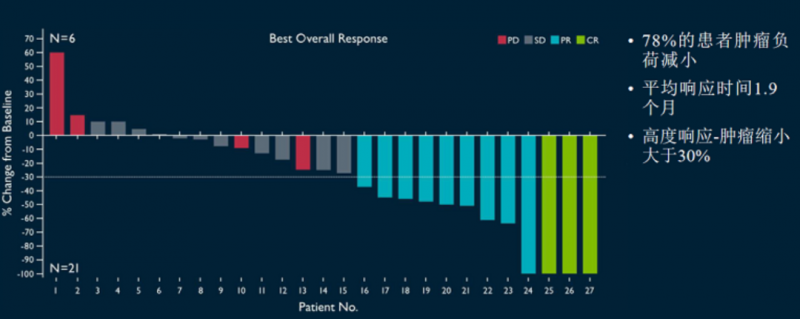
1.客观缓解率(ORR)44%,完全缓解率(CR)11%,疾病控制率(DCR)高达85%。即12名的患者有效果,包括1名完全应答,9名部分应答和2个未确认的部分应答;
2.中位随访时间为3.5个月,12例患者中有11例持续应答;
3.没有任何严重的副作用发生。
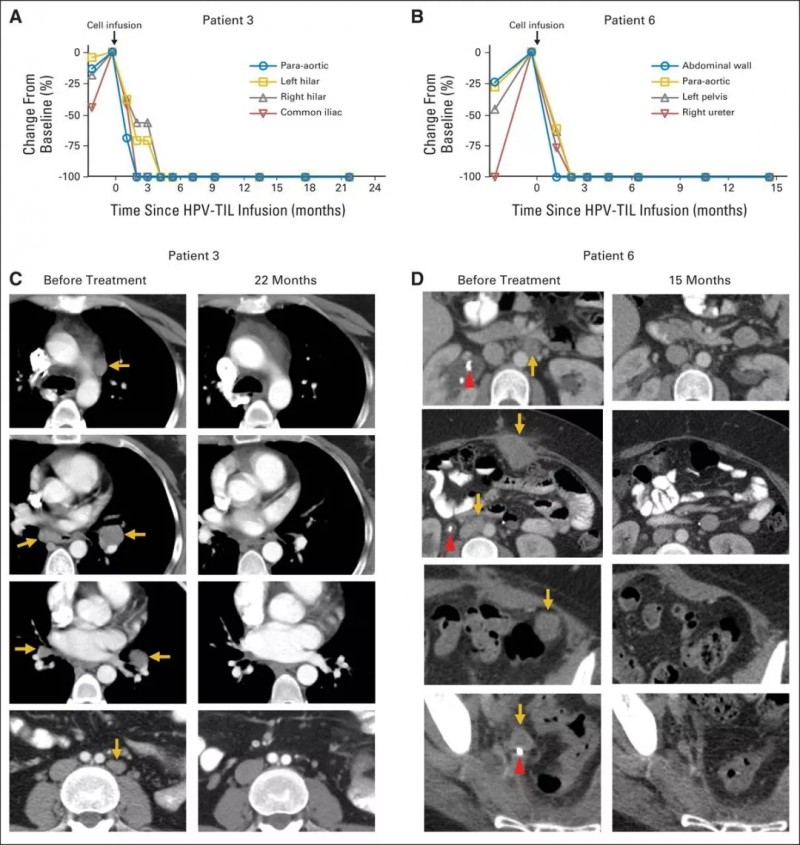
一名患有转移性鳞状细胞癌并接受了多种联合化疗方案,包括顺铂,长春新碱和博来霉素,然后用吉西他滨加顺铂联合放疗。随后发现转移,包括主动脉旁,双侧肺门,颅下和髂骨部位(图1A和1C)。治疗后,她在所有疾病部位都完全消退(图1A和1C)。
另一患者患有转移性腺癌。她的原发性肿瘤对化放疗无效。随后转移到更多的腹膜后淋巴结和肝脏表面,在TIL治疗前,她在腹膜后,腹壁,旁系,肝旁和盆腔部位有肿瘤进展(图1B和1d)。在治疗后,出现完全的临床缓解(图1B和1d)。
值得振奋的是,在化疗期间或之后进展的宫颈癌患者的治疗选择有限,之前报道的晚期宫颈癌化疗或免疫治疗二线治疗的应答率仅在4%-14%之间。而这款新型的非常安全的细胞免疫疗法为晚期宫颈癌患者带来了44%的应答率,并且在一些患者中表现出持久的应答效果,研究人员表示这种治疗方式可以实现长期疾病控制的希望。希望这款疗法能尽快获批上市。
三,非小细胞肺癌-为PD-1耐药的患者再续生存期
肺癌是全球发病和死亡最高的癌症,尽管近年来靶向和免疫治疗发展已经让肺癌越来越趋于慢性病的治疗,但是对于一些患者来说,当最后的保底药物PD-1发生耐药后,仍让患者们感到恐慌。
美国时间4月27日,在今年的AACR会议上,一项由美国知名癌症中心莫菲特癌症研究中心(H. Lee Moffitt )开展的基于TIL细胞治疗的Ⅰ期临床结果公布:
在12名可评估的非小细胞肺癌患者中,TIL疗法可达到25%的总缓解率,其中两名患者达到持久的完全缓解。

尽管这项研究规模很小,但还是令肿瘤学家们感到振奋,因为这些患者都是临床上已经接受过PD-1(Opdivo)治疗后病情进展的晚期患者,这些患者可以说是山重水复疑无路,最为难治的患者群体了。
当从这些患者体内的肿瘤病灶中提取出抗癌能力超强的TILs细胞,并在体外扩增培养成数十亿有着精准杀伤能力的免疫大军,回输到体内作战时,大部分患者在首次TIL治疗后进行 CT扫描就开始出现明显的肿瘤消退。
这项试验共有32名患者参加,最终有16名患者接受TILS治疗,其中12名患者可以评估。在平均随访1.4年时,3名患者病情缓解,其中两名完全患者,并且已超过一年。另一名患者的缓解即将得到确认。
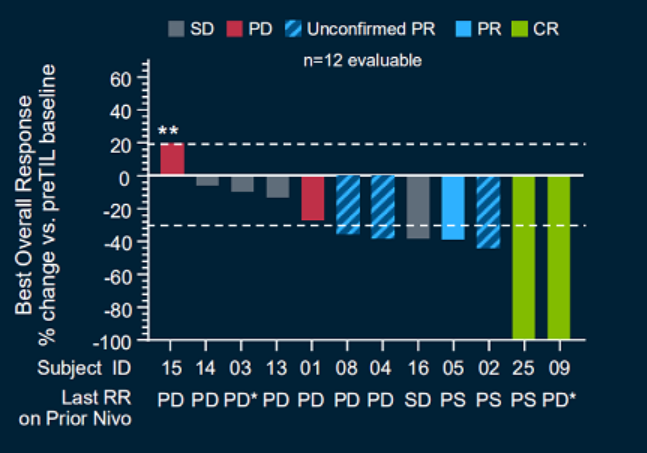
大部分患者在接受TILs治疗后,肿瘤病灶都有所缩小,在接受治疗后的第一次CT扫描时,肿瘤病灶直径平均缩小38%!
因此,在PD-1治疗后,TILs疗法仍具有令晚期转移性非小细胞肺癌达到持久缓解的能力,这是非常了不起的,期待这款疗法能加大研究,早日获批上市,为晚期患者的生命持续续航!
四,其他实体肿瘤
目前,这款新型的免疫疗法暂未上市,但在全球范围内开展了多项针对各类实体肿瘤(非小细胞肺癌,结直肠癌,卵巢癌,黑色素瘤...)的临床试验。
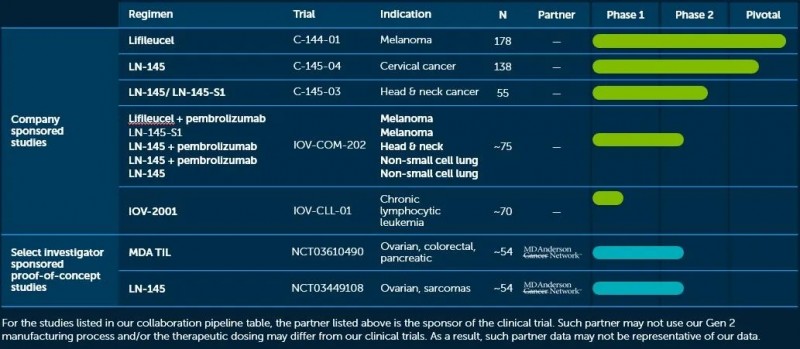
(正在进行的各项临床研究进展)
重要提示
目前,美国的TILs治疗技术只能通过新鲜肿瘤组织提取TILs细胞,因此,肿瘤患者在手术后第一时间将肿瘤组织中杀癌能力最强的这部分TILs细胞储存起来,在手术后或癌症复发时扩增回输到体内,这将是战胜癌症最宝贵的机会之一。国内的TILs技术在此基础上进行了调整,可通过血液或抽取胸腹水提取。目前美国和国内的TILs疗法均未正式上市,只能通过临床试验接受治疗,大家需要慎重选择。我们期待这款新型免疫疗法能够早日获批上市,给肿瘤患者带来新的治疗选择。
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

肺癌根治术后如何预防高危复发?五大疗法齐
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
早期膀胱癌术后五年生存率高达90%,这五
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

警惕!乳腺癌复发偏爱这3大人群!术后一定
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【实体瘤溶溜病毒免费招募】溶瘤病毒Ml(
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
从多处转移到完全缓解!新型CAR-T细胞
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
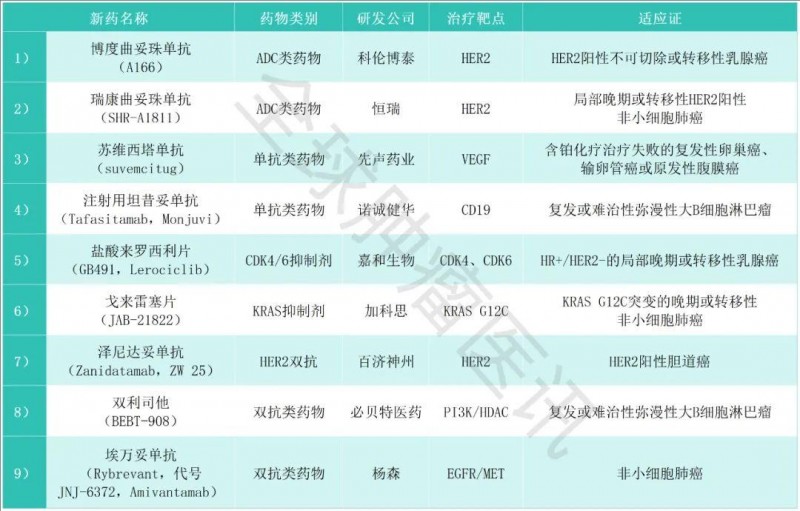
救命药加速入场!2025第二季度9款抗癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




