癌症治疗革命!mRNA疫苗成功"训练"免疫系统,癌症患者迎来新的生命曙光
癌症治疗革命!mRNA疫苗成功"训练"免疫系统,癌症患者迎来新的生命曙光
癌症是全球第二大死因,每年导致近1000万人死亡,传统疗法如化疗和放疗虽有一定效果,但存在严重副作用、缺乏特异性及对晚期癌症疗效有限等问题,近年来,mRNA肿瘤疫苗凭借其快速研发、高度个性化及精准靶向等优势,成为癌症免疫治疗领域的革命性突破。本文将从科学原理、技术进展、临床成果及未来挑战等多维度,全面解析这一新兴疗法如何重塑癌症治疗格局。
一、mRNA疫苗的科学基础与核心机制
1.mRNA疫苗的核心原理
mRNA(信使核糖核酸)疫苗通过合成特定序列的mRNA分子,指导人体细胞生成肿瘤抗原蛋白,这些抗原被免疫系统识别后,激活针对癌细胞的特异性免疫反应;与传统疫苗不同,mRNA疫苗无需直接递送病原体或蛋白,而是利用人体自身的“生物工厂”生产抗原,极大提升了安全性和灵活性。
2.抗原选择的精准性
mRNA疫苗靶向的抗原分为两类:
- 肿瘤相关抗原(TAAs):在癌细胞中高表达,但正常细胞也可能少量存在(如黑色素瘤中的酪氨酸酶);
- 肿瘤特异性抗原(TSAs):由癌细胞基因突变产生,仅存于肿瘤组织(如HPV相关癌症中的E6/E7蛋白)。
通过基因测序技术筛选患者特异性TSAs,可设计高度个性化的疫苗,减少误伤健康细胞的风险。
二、mRNA疫苗的技术分类与递送系统
1.疫苗类型
- 非复制型mRNA疫苗:结构包括5’帽、编码区及poly(A)尾,稳定性高但需较大剂量(如辉瑞/BioNTech的BNT111);
- 自我扩增型mRNA疫苗(saRNA):整合病毒复制酶基因,可在细胞内扩增mRNA,显著降低剂量需求。
2.递送系统的创新
mRNA易被酶降解,高效递送是技术关键:
- 脂质纳米颗粒(LNPs):目前主流载体,可保护mRNA并促进细胞摄取(如Moderna疫苗采用4组分LNPs);
- 病毒样颗粒(VLPs):模拟病毒结构,提升靶向性(如针对HPV的嵌合型VLP疫苗);
- 聚合物载体:如聚乙二醇-聚赖氨酸(PEG-PLys)纳米颗粒,延长血液循环时间并增强肿瘤渗透。
三、免疫激活的全链条作用机制
1.抗原呈递与免疫启动
mRNA疫苗通过载体进入细胞后,在细胞质中翻译为抗原蛋白,这些蛋白被加工为肽段,与主要组织相容性复合体(MHC-I)结合后呈递至细胞表面,激活CD8+ T细胞直接杀伤癌细胞。
2.先天与适应性免疫的协同
mRNA中的特定序列(如尿苷修饰)可激活Toll样受体(TLR7/8),诱导树突状细胞成熟并分泌干扰素-γ(IFN-γ)等细胞因子,进一步增强T细胞和B细胞反应。
3.长期免疫记忆的形成
疫苗诱导的高亲和力T细胞可形成记忆细胞,提供持续的抗肿瘤保护,降低复发风险。
四、提升疗效的四大策略
1.序列优化与化学修饰
- 密码子优化:调整mRNA序列的GC含量,提升翻译效率;
- 假尿苷修饰:降低免疫原性并延长半衰期(如Moderna采用的N1-甲基假尿苷)。
2.联合疗法突破免疫抑制
- 免疫检查点抑制剂:PD-1/PD-L1抑制剂(如帕博利珠单抗)可解除肿瘤微环境中的免疫抑制,与疫苗联用显著提高疗效(临床试验显示黑色素瘤患者无复发生存期延长);
- 细胞因子调节剂:如IL-12或STING激动剂,可增强抗原呈递细胞的活性。
3.精准递送与局部给药
- 瘤内注射:直接将疫苗递送至肿瘤部位,减少全身副作用(如BNT122疫苗在结直肠癌中的试验);
- 吸入式LNPs:针对肺癌等呼吸系统肿瘤,提高肺部靶向性。
4.人工智能辅助抗原筛选
利用机器学习分析肿瘤基因组数据,快速识别患者特异性抗原,缩短疫苗设计周期。
五、临床试验里程碑与突破性成果
1.黑色素瘤
- mRNA-4157:联合帕博利珠单抗治疗术后高风险患者,Ⅲ期临床试验显示无复发生存期(RFS)显著延长;
- BNT111:针对TAAs(如NY-ESO-1)的疫苗,单药或联合PD-1抑制剂均显示高应答率。
2.其他实体瘤
- 前列腺癌:BNT112疫苗靶向PSA、PSMA等抗原,Ⅰ期试验显示良好安全性;
- 卵巢癌:个体化TSA疫苗在早期试验中诱导T细胞浸润,部分患者肿瘤缩小。
3.血液系统恶性肿瘤
- RNA-CART-cMET:结合CAR-T技术与mRNA疫苗,靶向MET阳性肿瘤细胞,在乳腺癌和黑色素瘤中展现初步疗效。
六、当前挑战与未来方向
1.肿瘤异质性与抗原逃逸
同一肿瘤内不同细胞的基因突变可能导致抗原丢失,解决方案包括多抗原疫苗开发及动态监测突变谱。
2.免疫抑制微环境的调控
肿瘤相关巨噬细胞(TAMs)和调节性T细胞(Tregs)抑制免疫活性,联合TLR激动剂或表观遗传药物可重塑微环境。
3.生产与可及性瓶颈
mRNA疫苗的低温存储要求(-20°C至-80°C)限制了资源匮乏地区的应用,新型冻干技术和常温稳定载体正在研发中。
4.生物标志物的探索
寻找预测疗效的标志物(如肿瘤突变负荷TMB或特定miRNA)是优化治疗的关键。
七、未来展望
随着CRISPR基因编辑、单细胞测序及纳米技术的进步,mRNA疫苗将迈向更高层次的个性化与精准化:
- 预防性疫苗:针对遗传性癌症高风险人群(如BRCA突变携带者);
- 通用型疫苗平台:快速适配新发突变(如流感疫苗模式);
- 全球可及性提升:低成本生产与分布式制造网络(如非洲本地化mRNA生产中心)。
八、总结
mRNA肿瘤疫苗不仅代表技术突破,更象征着医学从“一刀切”到“量身定制”的范式转变,尽管挑战犹存,但其在临床试验中的卓越表现已为无数患者点燃希望;未来,随着科研与产业的协同创新,mRNA技术有望彻底改写癌症治疗的历史,让“治愈”不再是遥不可及的梦想。
如果您或家人正面临癌症挑战,欢迎随时咨询全球肿瘤医生网医学部,了解mRNA疫苗的最新进展与适用性,科学的力量,终将照亮生命的希望!
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

【BTK抑制剂】新一代靶向药奥布替尼终于
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

从轮椅到独立行走:硼中子俘获疗法以67%
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
刚刚!首个国产PD-1单抗,获批晚期黑色
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
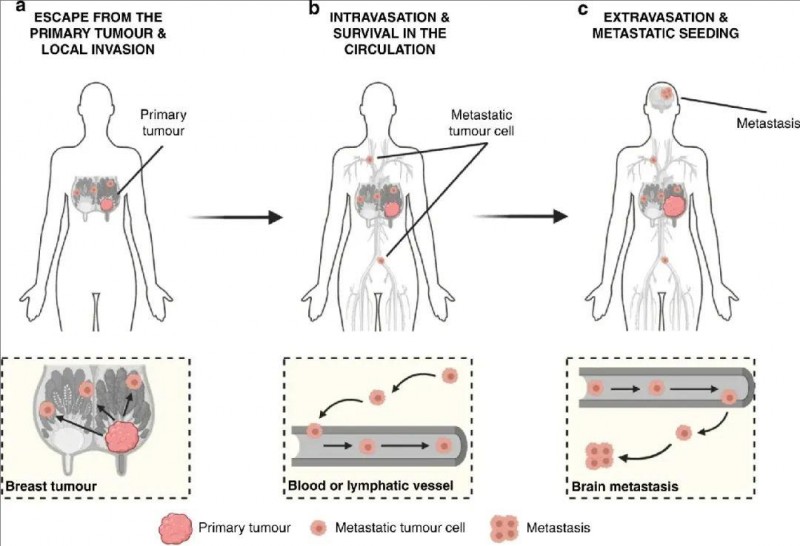
癌症复发的"头号凶手"
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

停药4年仍无癌!TIL细胞联合伊匹单抗,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

《CAR-T三人行》第十五期|魏双教授:
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




