肿瘤缩小超七成,病毒全清!星汉德TCR-T新药IND国内获批,降维打击肺癌、肝癌、宫颈癌等实体瘤
TCR-T细胞疗法治疗肺癌、肝癌、宫颈癌等实体瘤肿瘤缩小超七成,病毒全清
2025年1月2日,星汉德生物宣布,国家药品监督管理局药品审评中心(NMPA)已批准其全新一代TCR-T细胞疗法——SCG142的新药临床试验申请,主要用于HPV感染相关恶性肿瘤的治疗。
人乳头瘤病毒(HPV)是极为常见的性传播病原体,HPV感染可导致90%以上的肛门癌和宫颈癌、约70%的阴道癌和外阴癌、60%的阴茎癌和口咽癌。据估算,全球范围内,每年有63万例新发癌症病例以及35万例死亡病例,均与HPV感染有关。
而SCG142的问世,将为这类实体瘤的治疗提供了新的选择。SCG142是一款具有高亲和力的全天然HPV特异性TCR-T细胞治疗产品。研发团队成功筛选出全天然的HPV特异性TCR,并将其与星汉德生物自主研发的新型嵌合开关受体多能T细胞增强模块相结合。该产品能够有效克服恶劣的肿瘤微环境,将抑制信号转化为共刺激信号,这一关键特性对实现实体肿瘤的有效免疫治疗至关重要!
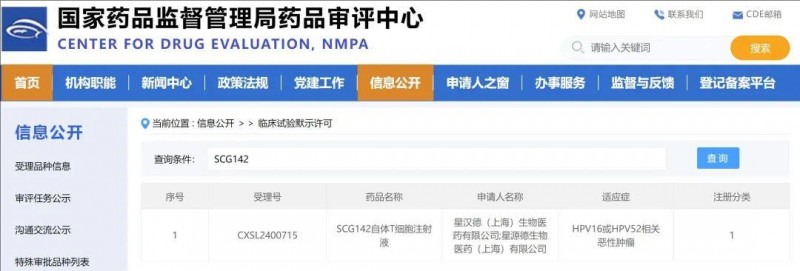
▲截图源自“NMPA”
TCR-T疗法强势出击病毒感染相关癌症,实现抗癌与抗病毒"双杀"
某些癌症的发生可能与病毒感染有关,如人乳头瘤病毒(HPV)相关上皮癌(如HPV感染相关宫颈癌等)、乙型肝炎病毒(HBV)相关肝细胞癌(HCC)等。这些病毒感染相关癌症晚期通常无法治愈且对化疗有耐药性,因此迫切需要寻求新的治疗方法。而兼具抗癌和抗病毒双重功效的TCR-T疗法的出现,为这类患者带来了新的希望!
星汉德SCG101 TCR-T暴击乙肝病毒相关肝细胞癌,肿瘤缩小74.5%,乙肝感染100%清除
除了开篇提到的新药IND获中国NMPA批准的SCG142 TCR-T细胞疗法外,星汉德生物还有一款在研的TCR-T疗法——SCG101一经问世就引起了巨大轰动!
肝癌是全球第六大常见癌症,每年新发病例超过90万。乙型肝炎病毒感染是导致肝癌的主要原因,乙肝病毒相关肝细胞癌占中国肝癌病例超过80%。乙肝病毒感染后,病毒DNA会整合进宿主基因组,可导致宿主细胞基因组不稳定性,表达病毒相关致癌基因,并诱发炎症、氧化应激等反应,引起肝细胞异常再生,最终多种机制共同导致肝细胞癌。
而SCG101是一种乙肝抗原特异性的TCR-T细胞疗法,可以特异性靶向HBV抗原相关T细胞表位,有效清除HBV-HCC肿瘤细胞、HBV-DNA整合的癌前病变细胞和HBV感染细胞,回输后还可形成特异性记忆T细胞亚群,实现SCG101长期自我更新能力和功能性,维持持续的抗肿瘤和抗病毒效应。临床数据显示,SCG101具有显著的抗肿瘤和抗病毒活性,其最新突破临床数据已在法国巴黎举行的国际细胞与基因治疗大会(ISCT)上公布。一位确诊HBV相关肝细胞癌的患者,在接受单剂SCG101治疗后,获得部分缓解(PR),肿瘤缩小74.5%,乙肝感染100%清除。
1、肿瘤显著缩小:该患者在接受单剂SCG101输注第28天,肿瘤靶病灶相比基线缩小66%,达到部分缓解(PR),并在治疗第4个月,肿瘤进一步缩小74.5%;另一处病灶完全消失。值得一提的是,试验期间该患者未接受任何其他抗肿瘤治疗。截至数据统计时止,该患者肿瘤未进展时间已超过6.9个月,且保持持续的缓解状态。
▼该患者在回输SCG101前后的影像学变化
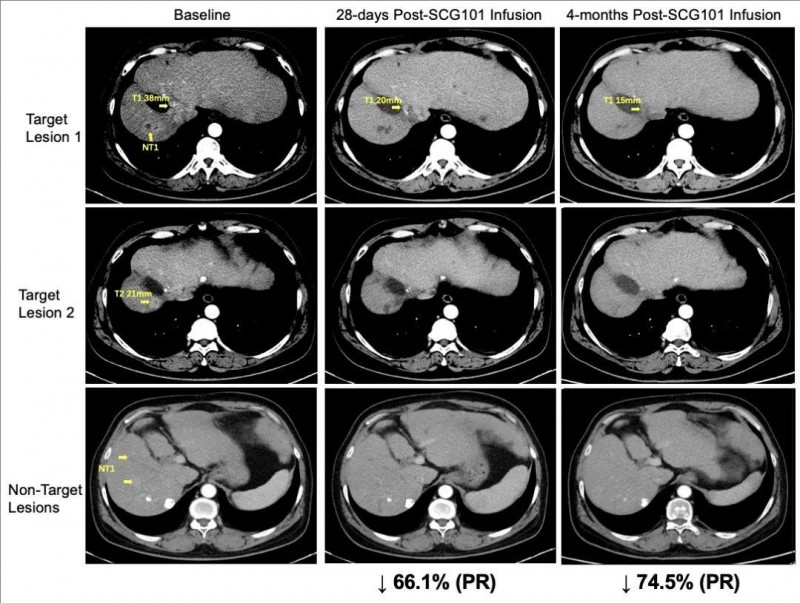
▲图源“SCG”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2、HBV感染缓解:基于回输前后的肝脏免疫组化分析显示,乙肝表面抗原阳性肝细胞实现100%清除,HBV血清学标志HBsAg从SCG101输注前的557.96 IU/mL,在输注后第7天降至1.3 IU/mL,第28天进一步降至0.08 IU/mL(详见下图)。
▼该患者在回输SCG101前后的HBsAg水平变化
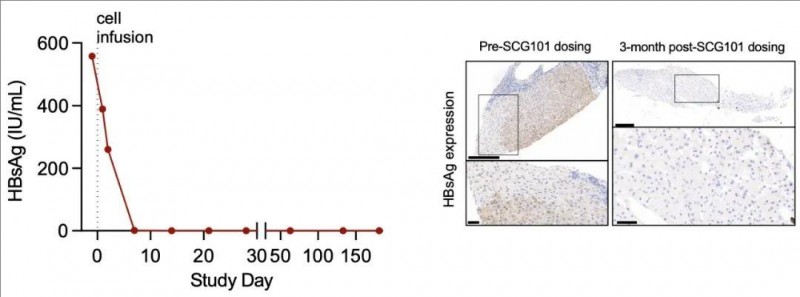
▲图源“SCG”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
中国患者如何寻求TCR-T疗法帮助
好消息是,目前正有几款在研的TCR-T疗法,针对妇科恶性肿瘤(宫颈癌、子宫内膜癌、卵巢癌)、头颈部肿瘤、乙型肝炎病毒相关肝细胞癌等,开展相关临床试验。中国患者也有机会获得实体瘤新利器:TCR-T疗法的帮助!
想参加的癌友,可将治疗经历、近期病理检查、影像学及血液检查、出院小结等资料,提交至医学部,进行初步评估或了解详细的入排标准!
TCR-T治疗HPV相关上皮癌首次人体I/II期临床惊艳,1例肿瘤完全消退且3年未复发
人乳头瘤病毒(HPV)相关上皮癌包括宫颈、口咽、肛门、外阴、阴道和阴茎的鳞状细胞癌及腺癌等。这些癌症表达E6和E7癌蛋白,它们是驱动恶性肿瘤的病毒抗原,在健康组织中不存在,使其成为研究上皮癌基因工程T细胞疗法(TCR-T)的有吸引力的靶点。
美国国立癌症研究所开展了一项“应用TCR-T治疗HPV相关上皮癌的首次人体I/II期临床研究(NCT02858310)”,本次研究共入组12例中位年龄为50岁(范围32~70岁)的转移性HPV16阳性上皮癌患者,包括6例宫颈癌、4例肛门癌、1例口咽癌、1例阴道癌(其中三种宫颈癌肿瘤为腺癌,所有其他肿瘤均为鳞状细胞癌),并且之前均接受过铂类疗法,入组接受E6 TCR-T细胞治疗。
结果显示:大多数患者的肿瘤均消退,尽管消退深度和持续时间各不相同。其中2例患者均在最高剂量组中,达到客观肿瘤反应(详见下图)。
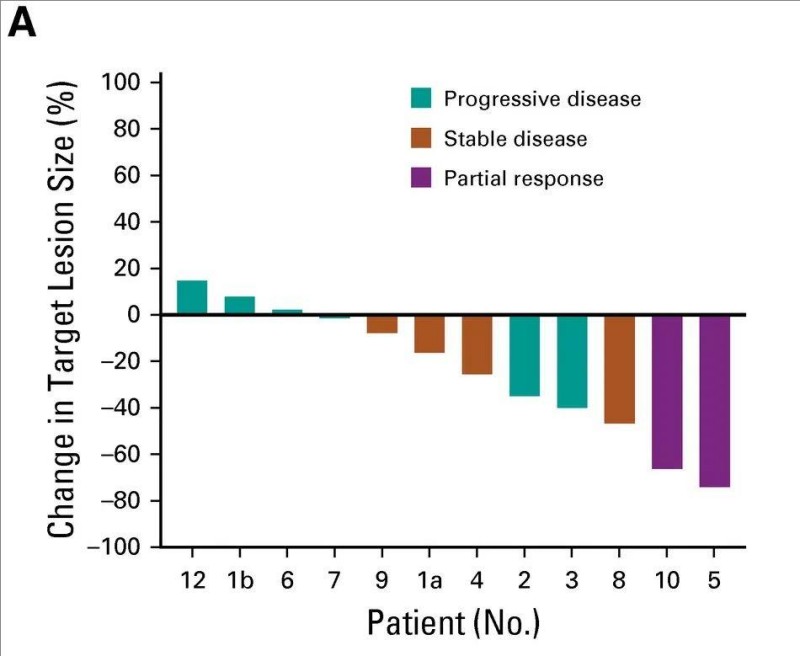
▲图源“JCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
值得一提的是,其中1例48岁患有三处转移的肛门鳞状细胞癌女性患者(患者5),在接受E6 TCR-T细胞治疗后,一个肿瘤病灶完全消退,2个肿瘤部分消退。该患者既往接受过放疗、氟尿嘧啶+丝裂霉素、顺铂+卡培他滨等治疗,但效果均不理想,双肺病情出现进展。遂入组接受E6 TCR-T细胞治疗,治疗后结果显示,她的病情奇迹般获得部分缓解(PR),具体表现为1个肺肿瘤完全消退,2个肺肿瘤部分消退,均在进展时予以切除。更为惊喜的是,在TCR-T治疗3年后,该患者依然没有疾病复发迹象(详见下图)。
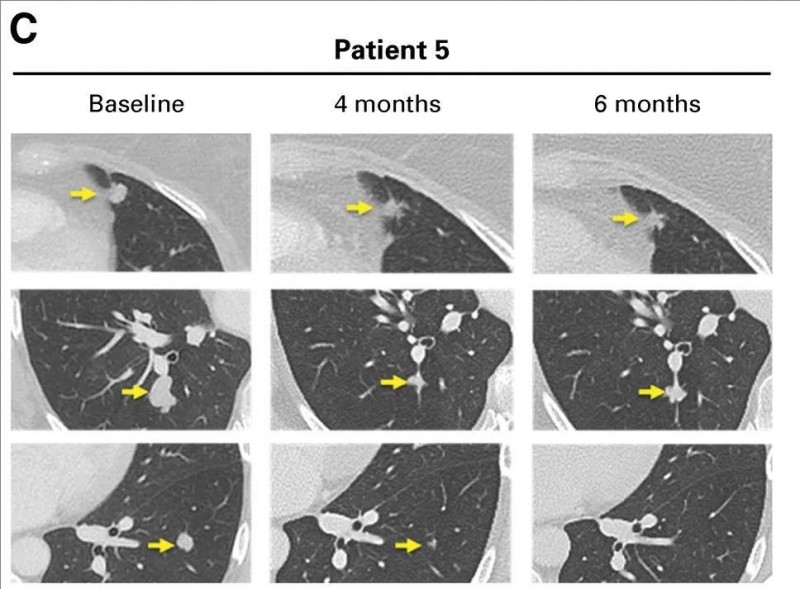
▲图源“JCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:增强计算机断层扫描显示患者5的肿瘤反应。两个病变部分消退(顶行和中间行),一个病变完全消退(底行)。
实体瘤的"劲敌"登场,TCR-T疗法重拳出击十大常见癌种
基于基因工程改造的免疫疗法TCR-T细胞疗法是一种很有前景的治疗方法,通过对患者的T细胞进行基因工程改造,使其表达特异性的TCR,而这些TCR可识别癌细胞上的主要组织相容性复合体(MHC)呈递的肿瘤相关抗原,利用天然的TCR-MHC相互作用来靶向更广泛的细胞内抗原,包括来自突变蛋白质的新抗原,这在治疗实体肿瘤方面具有显著优势。
TCR-T细胞疗法的三大优势
与传统癌症疗法相比,TCR-T细胞疗法具有以下几个显著的优势:
1、TCR-T细胞疗法具有高度特异性,因为它旨在针对患者特异性肿瘤抗原,从而最大限度地减少对正常组织的附带损害。
2、TCR-T细胞疗法可提供持久的免疫反应,修饰后的 T 细胞能够在体内存活并发挥作用很长时间。
3、TCR-T细胞疗法有可能克服某些对常规治疗无反应的肿瘤的耐药性,并且在治疗血液系统恶性肿瘤和某些实体肿瘤方面均表现出显著的疗效。
TCR-T细胞疗法临床研究遍地开花
近年来,TCR-T细胞疗法在癌症治疗领域的应用得到了广泛关注并取得了重大进展,其中临床试验数量从2006年到2024年逐年增加,在2019年至2024年期间达到顶峰。截至2024年8月1日,全球共注册了417项介入性临床试验。北美洲进行了84项试验(48.3%),亚洲进行了62项试验(35.6%),欧洲进行了8项试验(4.6%)(详见下图)。
2024年8月2日,更是迎来了全球首款针对于实体肿瘤的TCR-T疗法——afami-cel(TECELRA®)获批上市的好消息,主要用于成人不可切除或转移性滑膜肉瘤的治疗。
▼TCR-T细胞疗法在癌症治疗中的临床试验的全球分布
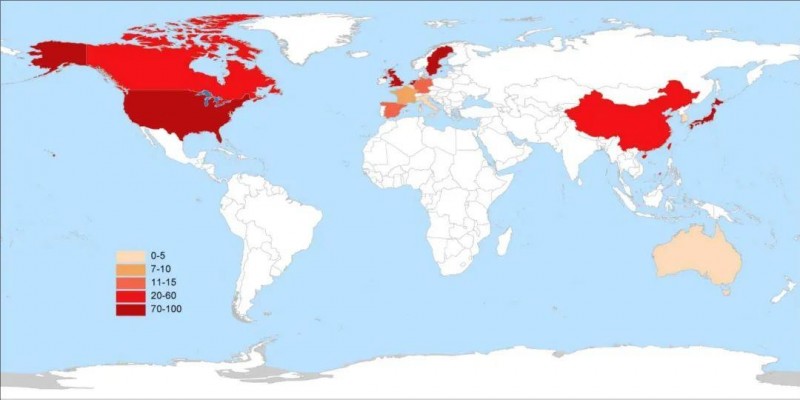
▲图源“Front Immunol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
TCR-T细胞疗法针对的主要癌种及靶点
针对的癌种
目前在研的TCR-T细胞疗法主要针对10种最常研究的癌症类型,包括:软组织肉瘤(STS)、黑色素瘤、食道癌、非小细胞肺癌(NSCLC)、肝癌、结直肠癌、卵巢癌、胃癌、急性淋巴细胞白血病(ALL)、非霍奇金淋巴瘤(NHL)。
针对的靶点
目前在研的TCR-T细胞疗法主要针对的靶点如下:
1、NY-ESO-1:即癌症-睾丸抗原1B(CTAG1B),是软组织肉瘤的主要靶标,并与非小细胞肺癌、食道癌、黑色素瘤、肝癌和卵巢癌等癌症具有显著的相关性。
2、MAGE:MAGE家族成员,尤其是 MAGE-A4,在软组织肉瘤和食道癌中,表现出很高的靶向潜力。
3、IL2RA(即白细胞介素-2 受体 α 链):主要靶向黑色素瘤,在其他癌症中也有中等程度的靶向性。
4、CD19:主要针对急性淋巴细胞白血病(ALL)、非霍奇金淋巴瘤(NHL)。
5、KRAS:主要针对结直肠癌。
6、其他靶标:包括 TNF 受体超家族成员 17 (TNFRSF17)、CD22、CD38、CD33、含有 14A 的 C 型凝集素结构域 (CLEC14A)等,在各种癌症中表现出一致但较低的靶向潜力(详见下图)。
▼TCR-T细胞治疗癌症临床试验的疾病和靶点分布
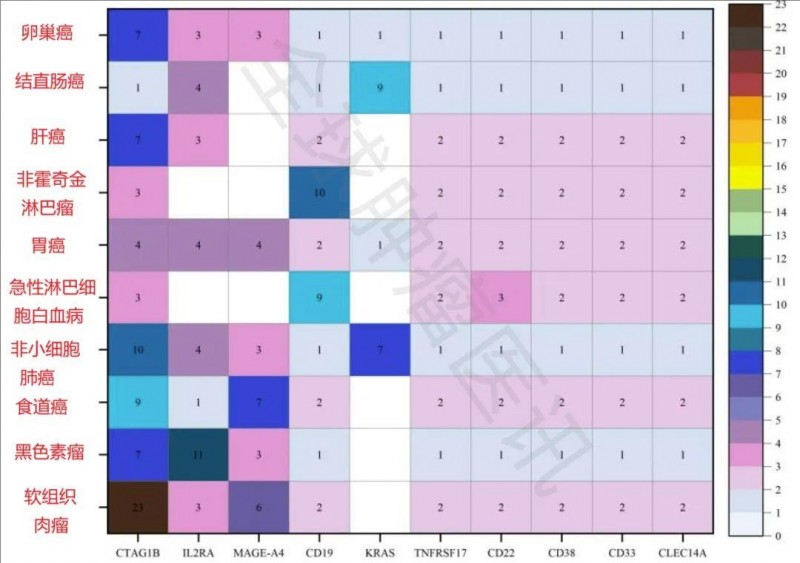
▲图源“Front Immunol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2025《Nature》重磅:转移性黑色素瘤BNT221 TCR-T细胞治疗仅6周,肿瘤显著缩小20%
对免疫检查点阻断 (ICB) 或 BRAF 靶向治疗有耐药性的晚期黑色素瘤患者,有必要采用新的治疗方法,而BNT221的出现为这类患者带来了新的希望!BNT221是一种源自外周血的个性化新抗原特异性自体 T 细胞产品,全球知名期刊《Nature Medicine》近期报道了一项“应用BNT221 TCR-T疗法,治疗对ICB耐药的不可切除或转移性黑色素瘤的1期临床研究(NCT04625205)”的惊艳数据!
本次共入组9例对ICB耐药的不可切除或转移性黑色素瘤患者,入组接受BNT221 治疗。其中,3例患者接受BNT221 剂量水平 (DL) 1,6 例患者接受DL2治疗。
结果显示:接受治疗的 9 名患者中,6 名的最佳总体反应为病情稳定 (SD),其中 4例病情稳定的患者(NAC03、NAC07、NAC08 和 NAC09)在输注 BNT221 后,出现肿瘤消退,根据实体肿瘤疗效评估标准 (RECIST) 1.1评估,消退高达-20%。2例患者(NAC08 和 NAC09)自觉肿瘤相关症状有所改善,包括活动范围改善、患肢水肿减少、基本日常生活活动能力增强。
▼基于 RECIST 1.1 的临床反应瀑布图
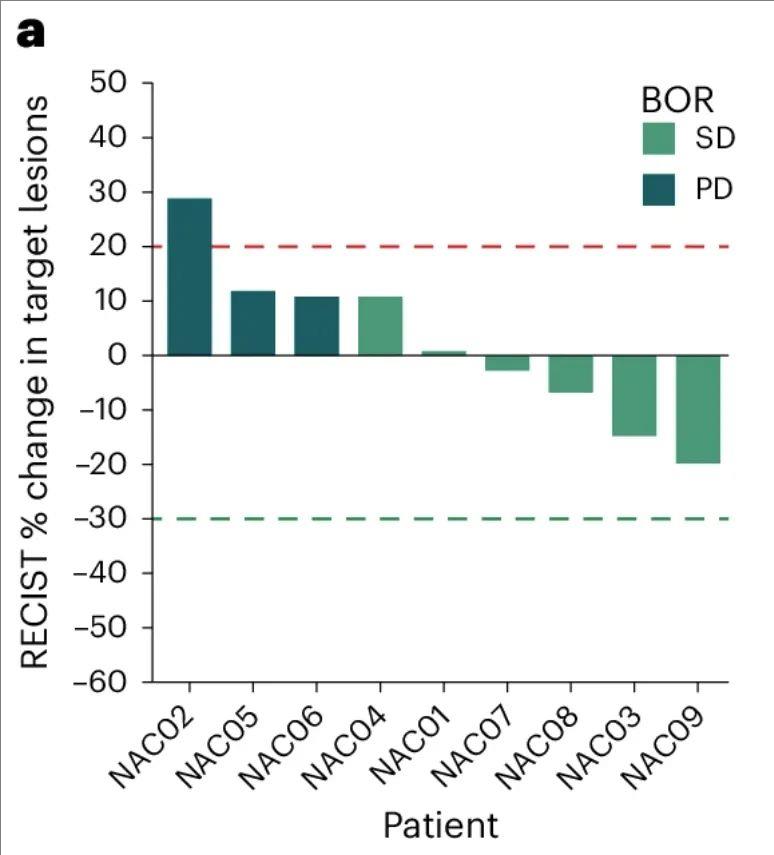
▲图源“SCG”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
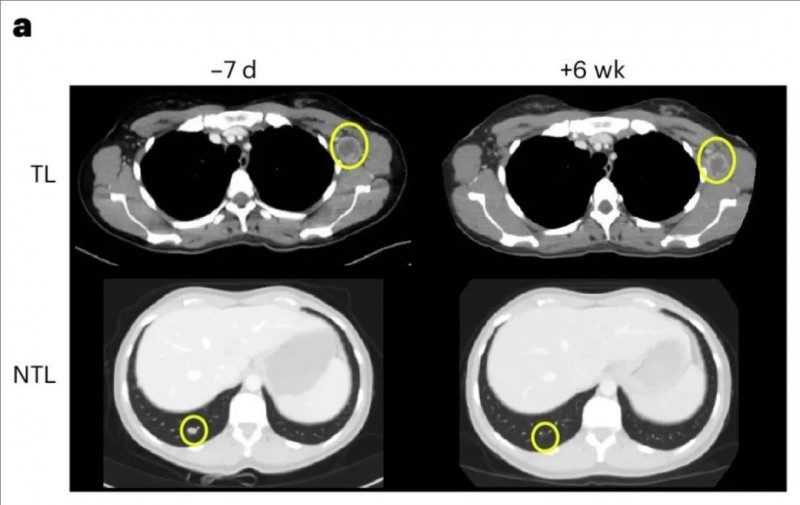
值得一提的是,NAC09号患者的肿瘤缩小幅度最大,该患者在输注BNT221 TCR-T细胞6周后,进行计算机断层扫描 (CT)显示,左腋窝靶病变减少了 20%,非靶病变(包括继发性腋窝淋巴结和毫米级肺病变)显著减少(详见下图)。此外,免疫组织化学分析显示,该患者肿瘤中 T 细胞浸润增加。
▼NAC09号患者TCR-T治疗前后的CT扫描对比
▲图源“SCG”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:
①圆圈区域突出显示目标病变(顶部)和非目标病变(底部),在第-7天和第+6周之间观察到消退。
②NTL——代表非目标病变;TL——代表目标病变。
NY-ESO-1 TCR-T细胞疗法,助晚期无药可用的肺腺癌患者奇迹般获得部分缓解,肿瘤显著缩小
非小细胞肺癌(NSCLC)约占所有肺癌病例的 80% 以上,NSCLC又可细分为三种主要组织学亚型,即肺腺癌(LADC)、肺鳞状细胞癌(LSCC)、大细胞肺癌(LCLC),其中,LADC 是最常见的亚型。对于晚期 NSCLC(IIIb 期和 IV 期)患者,通常没有可用的手术治疗选择,主要以放射治疗、化疗、靶向治疗和免疫治疗等全身治疗为主。然而,化疗和放疗的严重副作用发生率很高;而靶向治疗可能存在耐药性;此外,部分肺癌患者对检查点免疫疗法没有反应。因此,对于对免疫检查点疗法没有反应的患者,迫切需要新的免疫治疗策略。而近年研究发现,NY-ESO-1是癌症免疫治疗的一个有希望的靶点,具有良好的安全性和有效性,在11.8%~21% 的 非小细胞肺癌中表达。
近期知名期刊《oncology letters》报道了一个“应用NYESO1特异性TCR-T细胞疗法,治疗晚期非小细胞肺癌肿瘤明显缩小至部分缓解”的经典案例!该研究共入组4例HLA-A2 阳性的 NY-ESO-1转移性非小细胞肺癌(NSCLC) 患者,入组接受淋巴细胞清除化疗,以及过继转移 NY-ESO-1 TCR-T 细胞+全身性 IL-2 治疗。
结果显示:2例接受三次(患者1)和两次(患者2)NY-ESO-1 TCR-T 细胞输注治疗的患者获得了临床反应。根据实体肿瘤疗效评价标准(RECIST) 1.1 标准,患者 1 在过继移植 NY-ESO-1 TCR-T 细胞后近 3 个月病情稳定 (SD)(表 I )。患者 2 在治疗后 4 个月达到部分缓解(PR)(NCT02457650)。
值得一提的是,其中1例44岁HLA-A2 阳性的 NY-ESO-1晚期肺腺癌 (LADC)女性患者(患者2),该患者还携带EGFR 突变,既往曾接受过六个周期的联合化疗(多西他赛和卡铂),但效果不理想,疾病持续进展。之后还曾接受吉非替尼、厄洛替尼治疗,但效果均不理想,2015 年 9 月的随访 CT 扫描显示,该患者右肺门、纵隔、右胸膜、右肝叶和肝包膜出现病情进展(PD),此时临床已经没有适合她的治疗方法了。但天无绝人之路,右肺肿瘤支气管镜活检显示,标本免疫组化染色呈强NY-ESO-1,遂入组接受NY-ESO-1 TCR-T 细胞治疗。
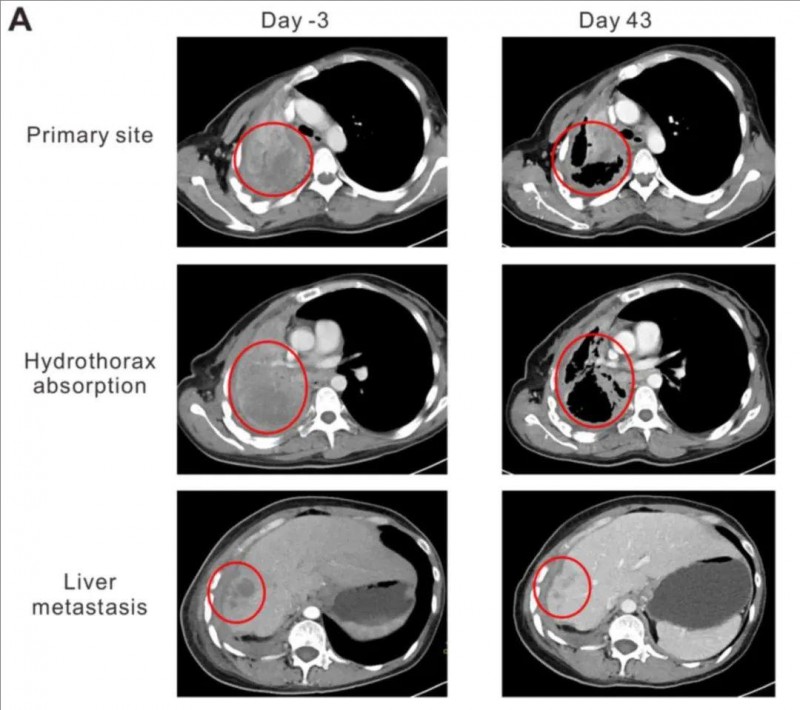
令人惊讶的是,首次TCR-T细胞输注后第43天CT扫描显示,该患者肺原发灶及肝转移灶消退,胸水吸收,肺复张(详见下图),肺原发灶由95×86×54 mm缩小至64×44×54 mm,肝转移灶由19.8×19.6×20 mm缩小至10×10×10 mm,根据RECIST 1.1评价疗效,该患者奇迹般达到部分缓解(PR)。
▲图源“oncology Letters”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:
①CT 扫描显示:原发性肿瘤位于右肺门,在 T 细胞输注前已转移至纵隔、右胸膜、右肝叶和肝包膜。
②2016 年 1 月(第 43 天),首次 T 细胞输注后 2 个月进行的 CT 扫描显示:原发性肺肿瘤和肝转移客观消退,以及胸水吸收和肺再扩张。
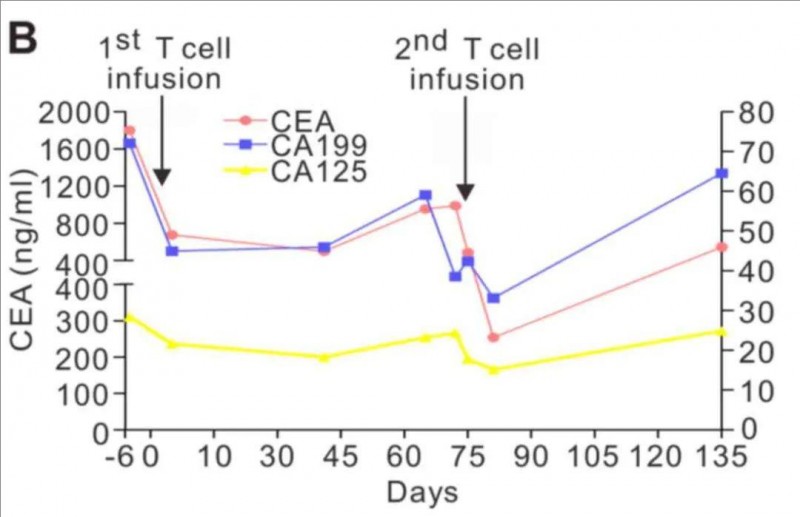
此外,肿瘤标志物(CEA、CA125、CA199),在初次输注TCR-T细胞后降低,随后(首次输注 TCR-T 细胞后 4 周)升高,第二次输注NY-ESO-1的TCR-T细胞后也出现类似变化(详见下图)。
▲图源“oncology Letters”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
值得注意的是,该患者的卡氏功能状态评分(KPS)在输注后有所改善,由50分提高到90分,咯血和胸痛症状得到缓解,这些结果均表明TCR-T细胞治疗改善了患者的临床症状。
小编寄语
TCR-T疗法与CAR-T同属于T细胞疗法,但TCR-T疗法具有更广泛的靶抗原,被认为在对抗实体瘤方面更具潜力。更值一提的是,TCR-T疗法开创了一种“一箭双雕”的新型治疗方案,即在同时针对癌症和病毒感染方面,具有效性、安全性和可行性。故而,近年来,研究人员尝试将TCR-T疗法应用于治疗宫颈癌[主要与人乳头瘤病毒(HPV)感染有关]、乙肝病毒相关肝细胞癌等癌种,并展现出了不俗的成绩。
想寻求TCR-T、CAR-T、TILs疗法或国内外其他抗癌新技术帮助的病友,可将治疗经历、近期病理报告及影像学检查结果等资料,提交至全球肿瘤医生网医学部,进行初步评估或申请国内外抗癌会诊,以寻求适合自己的个体化治疗方案。
参考资料
[1]Borgers J S W,et al.Personalized, autologous neoantigen-specific T cell therapy in linkstatic melanoma: a phase 1 trial[J]. Nature Medicine, 2025: 1-13.
https://www.nature.com/articles/s41591-024-03418-4
[2]Li J,et al.Clinical advances and challenges associated with TCR-T cell therapy for cancer treatment. Front Immunol. 2024 Oct 8;15:1487782.
https://pmc.ncbi.nlm.nih.gov/articles/PMC11493697/
[3]Xia Y,et al.Treatment of linkstatic nonsmall cell lung cancer with NYESO1 specific TCR engineeredT cells in a phase I clinical trial: A case report[J]. oncology letters, 2018, 16(6): 6998-7007.
https://www.spandidos-publications.com/10.3892/ol.2018.9534
[4]Doran S L,et al.T-cell receptor gene therapy for human papillomavirus–associated epithelial cancers: a first-in-human, phase I/II study[J]. Journal of Clinical Oncology, 2019, 37(30): 2759-2768.
https://ascopubs.org/doi/10.1200/JCO.18.02424
[5]https://www.cde.org.cn/main/xxgk/listpage/4b5255eb0a84820cef4ca3e8b6bbe20c
[6]https://www.scgcell.com/newsinfo/6283011.html
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

奥希耐药有救啦!沃利替尼联合疗法获突破治
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
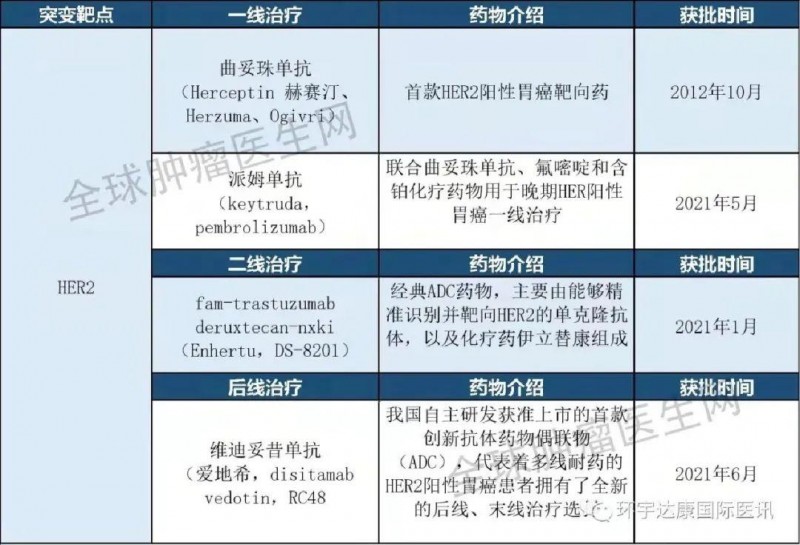
胃癌《2025抗癌宝典》出炉!多款新药,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
1.13 愈见大"CAR&qu
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【CAR-T细胞疗法免费招募】RD06-
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
速查!肺癌化疗哪家强?国内前十医院排行榜
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2025年度重磅!《肺癌患者必看指南》,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




