国内第3款CAR-T有望获批!更多晚期患者将获益,新疗法固守血癌,进击实体瘤!
国内第三款CAR-T疗法西达基奥仑赛(Cilta-cel、LCAR-B38M、JNJ-4528)有望获批,CAR-T细胞免疫疗法将让更多晚期患者获益
免疫疗法已然成为人类对抗癌症新的希望,而CAR-T疗法则是近年来最有前景的肿瘤免疫疗法之一。这项技术在治疗各种恶性肿瘤方面取得了巨大进展,已成功应用于多种血液恶性肿瘤的治疗。
特别是今年我国正式开启细胞免疫治疗元年,分别于6月份迎来首款CAR-T疗法——阿基仑赛注射液;9月3日,迎来第二款获批的CAR-T产品——瑞基奥仑赛注射液,这也是中国首款1类生物制品的CAR-T产品。
目前,随着阿基仑赛注射液、瑞基奥仑赛注射液前后在中国获批上市,癌症治疗领域火速掀起一阵“CAR-T热”。
据公开资料显示,在国内,进入临床阶段的CAR-T疗法多达36款,除了复星凯特阿基仑赛、药明巨诺瑞基奥仑赛以外。诺华的Kymriah正处于III期临床阶段,传奇生物BCMA CAR-T正处于II期临床阶段。而在CAR-T疗法市场,这种你追我赶的背后,也使得竞争进入白热化阶段,中国CAR-T细胞治疗行业必将迎来崭新的竞争格局。
其中,传奇生物的靶向BCMA(B细胞成熟抗原)CAR-T疗法西达基奥仑赛(LCAR-B38M/JNJ-4528,下称cilta-cel)一直备受关注,已经在治疗多发性骨髓瘤的临床试验中表现出卓越的抗癌活性。此前cilta-cel曾在5月26日被美国FDA授予优先审评资格,预计在今年11月29日之前做出回复。

也就是说,如果一切顺利,cilta-cel将有望成为国内第3款获批上市的CAR-T产品,也是首个靶向BCMA的CAR-T疗法!
总缓解率98%!BCMA CAR-T疗法cilta-cel疗效强劲!
6月1日,传奇生物公布了BCMA导向CAR-T细胞疗法cilta-cel(LCAR-B38M CAR-T细胞自体回输制剂/JNJ-4528)的最新研究数据。结果表明,在先前接受过多种疗法(过度预治疗)的复发/难治性多发性骨髓瘤(RRMM)患者中,cilta-cel显示出持续的疗效和持续缓解!

cilta-cel是一种研究性B细胞成熟抗原(BCMA)导向的CAR-T疗法,用于治疗复发或难治性多发性骨髓瘤(RRMM)。这些患者在治疗前平均接受过5种前期疗法,76%的患者接受过5种治疗,86%的患者对5种疗法耐药,其中包括CD38治疗,而且对蛋白酶抑制剂PI和免疫调节剂IMiD双重耐药。简单说就是复发难治、后续缺乏有效的疗法。
此款CAR-T疗法的原理与目前的PD-1/L1不同,它是直接利用患者体内的T细胞,将其在体外进行改造,大量复制后再会输到患者体内,以达到杀灭癌细胞的目的。
来自1b/2期CARTITUDE-1研究(n=97)的最新结果显示,中位18个月的长期随访,客观缓解率(ORR)达到了98%,80%的患者达到严格的完全缓解(sCR),强调随着时间的推移缓解加深(sCR从2020年ASH年会上报告的67%增加到80%)。在18个月时,有66%的患者存活且疾病无进展。在2021年ASCO年会上将要公布的最新研究结果显示,中位随访18个月,总生存(OS)率为81%,缓解率在全部预先指定的亚组和不同治疗线数患者中具有可比性。
其实早在今年3月27日,FDA就批准了首款以BCMA为靶点的CAR-T疗法,用于接受过4种以上疗法后复发/难治性多发性骨髓瘤(r/r MM)成年患者。
【传奇生物西达基奥仑赛(cilta-cel)所获国际认可概览】
●2017年12月,申报国内首个细胞治疗产品的药物临床试验申请(IND),并于2018年3月获得药物临床试验批件。
●2018年5月,获得美国FDA的IND许可
●2019年2月,FDA授予JNJ-4528孤儿药资格
●2019年4月,欧洲药品管理局( EMA)授予优先药物(PRIME)资格,成为中国首个获得欧洲药品管理局(EMA)优先药物(PRIME)资格的CAR-T产品
●2019年12月,美国FDA授予突破性疗法认定
●2019年12月,获国家“重大新药创制”科技重大专项支持
●2020年8月,纳入中国突破性治疗品种名单
●2020年12月,向美国食品和药物管理局(FDA)滚动提交生物制品许可申请
●2021年1月,欧洲药品管理局(EMA)的人类用药品委员会(CHMP)已接受对其上市许可申请(MAA)进行加速审评的请求
●2021年5月,欧洲药品管理局(EMA)接受关于申请批准西达基奥仑赛(cilta-cel)用于治疗复发或难治性多发性骨髓瘤成人患者的上市许可申请
●2021年5月,Cilta-cel获得美国食品药品监督管理局优先审查
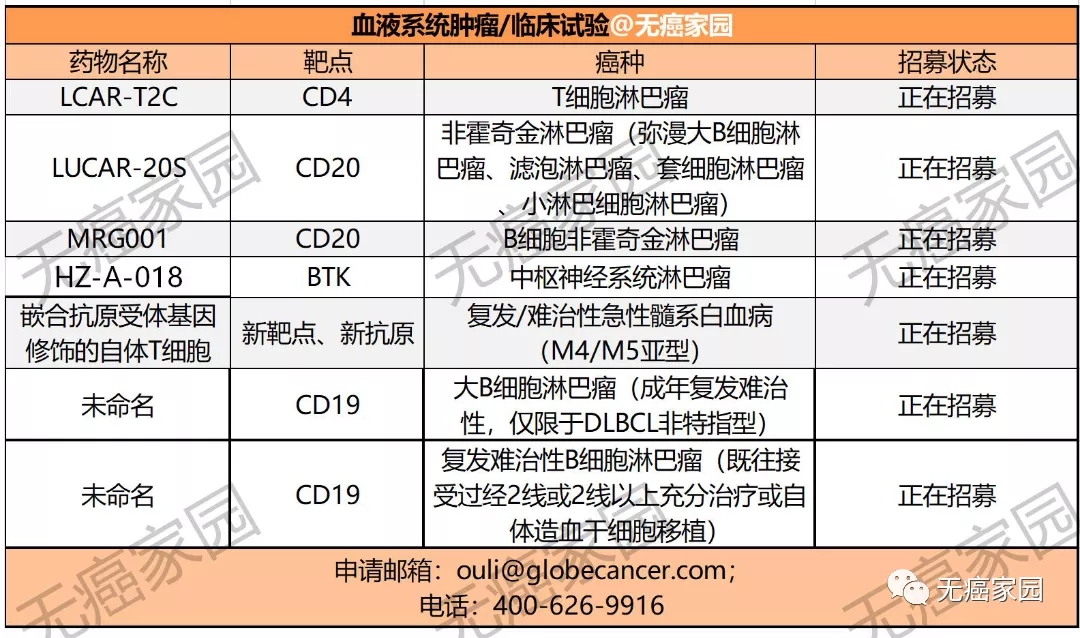
目前,无癌家园有多款血液肿瘤的CAR-T临床试验正在进行招募,有意向者可咨询医学部具体评估病情!
火爆的CAR-T疗法到底是何方神圣
CAR-T疗法说起来其实并不陌生,美国早在2012年就已开展CAR-T细胞疗法的临床试验,当时年仅6岁的Emily成为第一个吃螃蟹的受益者!
作为一种“活的”药物,CAR-T疗法与传统药物有着很大的区别。它与PD-1类似,是一种治疗肿瘤的新型免疫疗法,只不过机制比PD-1更复杂。
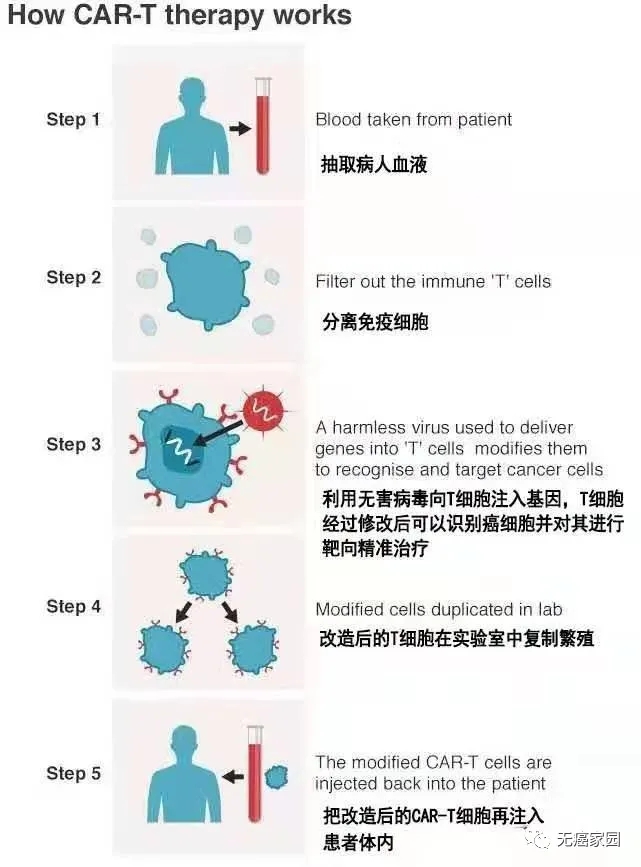
首先,该疗法需要从患者体内分离出T细胞,并在体外利用嵌合抗原受体(CAR)进行修饰,相当于装了个GPS系统,使其能够特异性识别癌细胞,将T细胞这个普通“战士”改造成“超级战士”,最后再将改造后的T细胞扩增、回输至患者体内。
无癌家园专家科普:CAR-T免疫疗法是如何工作的?
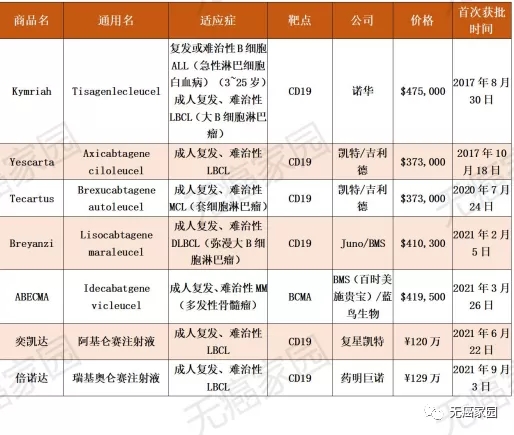
目前全球获批上市的所有CAR-T产品
新型CAR-T疗法固守血癌,进击实体瘤,不断突破瓶颈
10月19日,传奇生物在研发日活动上,介绍了最新的细胞疗法布局及动态,除了大家熟悉的cilta-cel外,而且还谈及在治疗实体瘤方面的重要研发项目及构建的同种异体CAR-T疗法技术平台方面的突破。
01、惊喜!首例CAR-T治愈的多发性骨髓瘤患者生存超5年!
国外的Emily在2021年成功迎来了无癌生存的9年,俨然成为全球CAR-T疗法的“代言人”。在中国也存在这样一位被CAR-T疗法彻底改变了命运的幸运儿。闵先生在54岁被确诊患有一种特殊的罕见病——多发性骨髓瘤。家庭经济贫困的他当时没有药物可用,有幸参加了CAR-T疗法的临床试验。虽然治疗的过程不是一帆风顺的,但经过3次的治疗后,闵先生身上的包块全部消失,疼痛没有了。
惊喜的是,截至2021年6月4日,闵先生无癌生活整整5年了,这才癌症治疗领域,就是理论上所说的临床治愈。
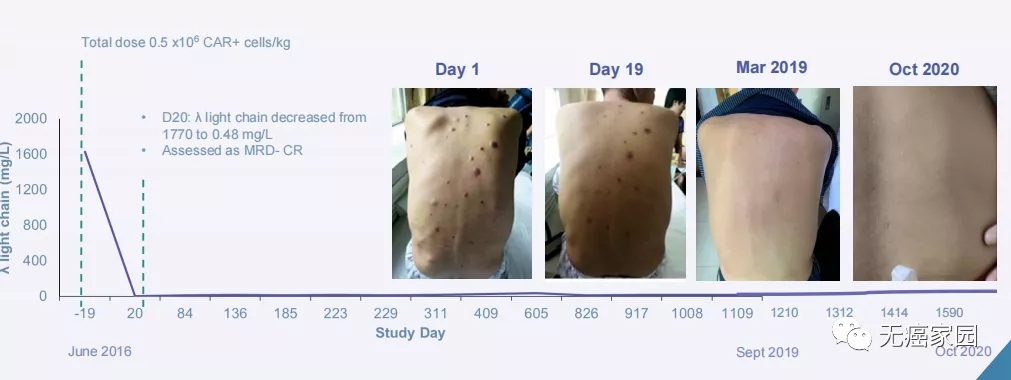
闵先生治疗前后对比图
02、治疗30天后,复发/难治性非霍奇金淋巴瘤患者病灶几乎完全消失
利用不依靠基因编辑阻断TCR信号的同种异体CAR-T技术平台,开发的CAR-T疗法LUCAR-20S已经进入1期临床试验。目前已经有5名复发/难治性非霍奇金淋巴瘤患者接受给药。其中3名患者(60%)获得部分缓解,尚未发现剂量限制毒性。其中一名患者在接受治疗30天后,放射性成像检测显示所有病灶几乎完全消失,骨髓活检仍为阳性,因此被判定为部分缓解。
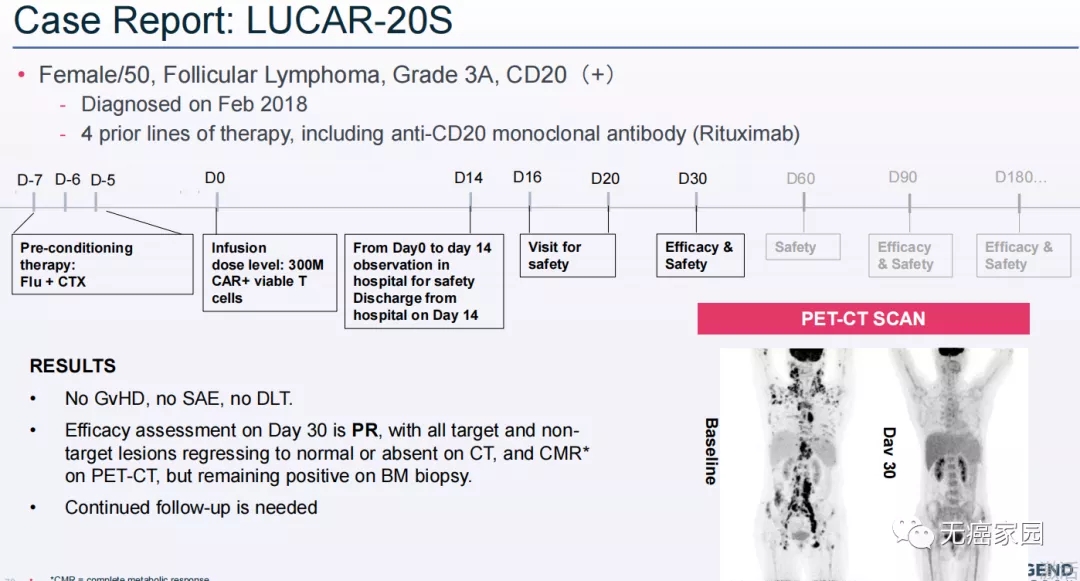
接受LUCAR-20S治疗的案例报告
克服治疗实体瘤障碍,新型CAR-T经多种优化,不断突破
虽然,CAR-T疗法在实体肿瘤方面如肝癌、胃癌、胰腺癌等消化系统肿瘤中也取得了一定的疗效,但是少之又少,这主要是碍于靶点选择困难、CAR-T细胞进入肿瘤组织困难、CAR-T细胞进入肿瘤组织后容易被其他免疫抑制性的分子或细胞所阻挡无法发挥作用等。
但国内外的学者针对CAR-T进行了多种改造,不断地发现新靶点,以用于治疗多种实体肿瘤。
01、CAR-T疗法治疗胃癌和胰腺癌
传奇生物的LB1908是一款靶向Claudin18.2(CLDN18.2)的CAR-T疗法。CLDN18.2在胃癌、胰腺癌等癌症类型中表达,是目前抗癌药物开发的热门靶点。然而与它同源性很高的CLDN18.1在人体的肺组织中表达。这意味着,CAR-T疗法需要对CLDN18.2具有高度特异性,否则有可能攻击健康肺组织,导致严重毒副作用。
LB1908利用了VHH抗体设计(这种抗体因为没有传统的轻链,比人体产生的抗体更为小巧,但是可以和传统抗体一样与抗原紧密结合)确保了它对CLDN18.2具有高度的特异性。在临床前胃癌和胰腺癌的动物模型中,它都表现出强力的抗癌活性。
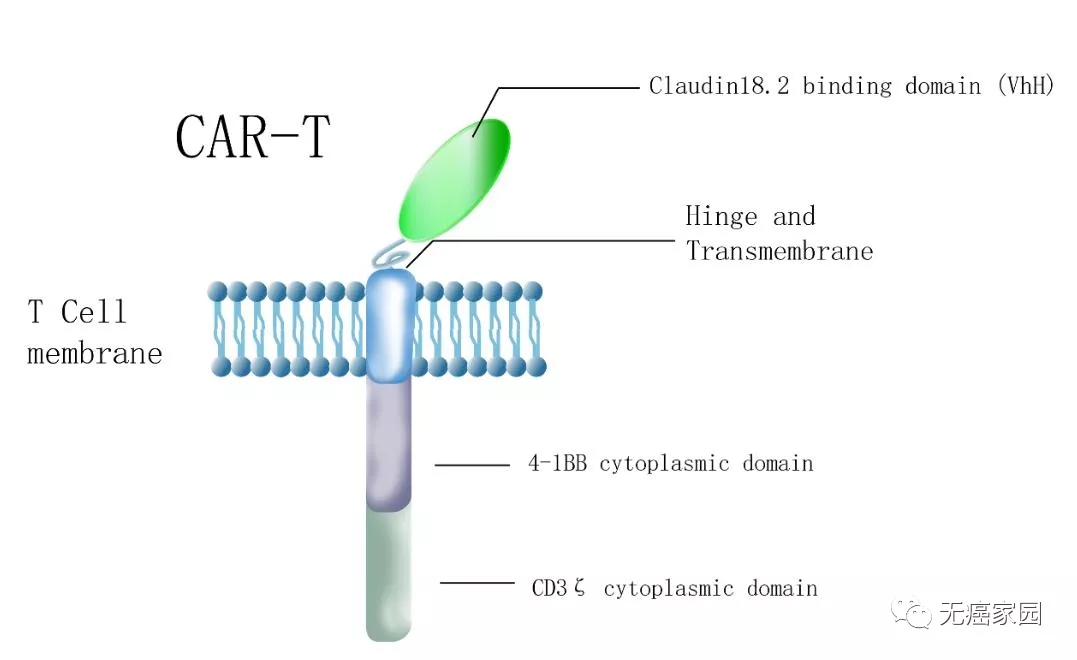
LB1908简介(图源传奇生物官网)
目前,这款在研CAR-T疗法已经进入剂量递增1期临床试验。在首例接受最低剂量LB1908治疗的患者中,它表现出良好的安全性和初步抗癌活性。在接受治疗180天后,患者疾病稳定,而且在骨盆的肿瘤缩小15%,位于身体其它部位的病灶显著缩小,患者的生活质量也获得显著提高。

接受最低剂量LB1908治疗患者表现出临床缓解征兆
02、CAR-T疗法治疗肝癌、肺鳞癌、生殖细胞癌
LB2101是一款靶向GPC-3的“武装”CAR-T疗法。它在表达靶向GPC-3的嵌合抗原受体(CAR)以外,还同时表达着一个被肿瘤微环境中的信号激活的跨膜蛋白。因此,它不会影响CAR-T细胞特异性,还能改善细胞的浸润、增殖和持久性。
在动物实验中,这款疗法与没有“武装”起来的CAR-T疗法相比,显示出更高的抗癌活性,而且在动物体内的细胞扩增幅度更大。
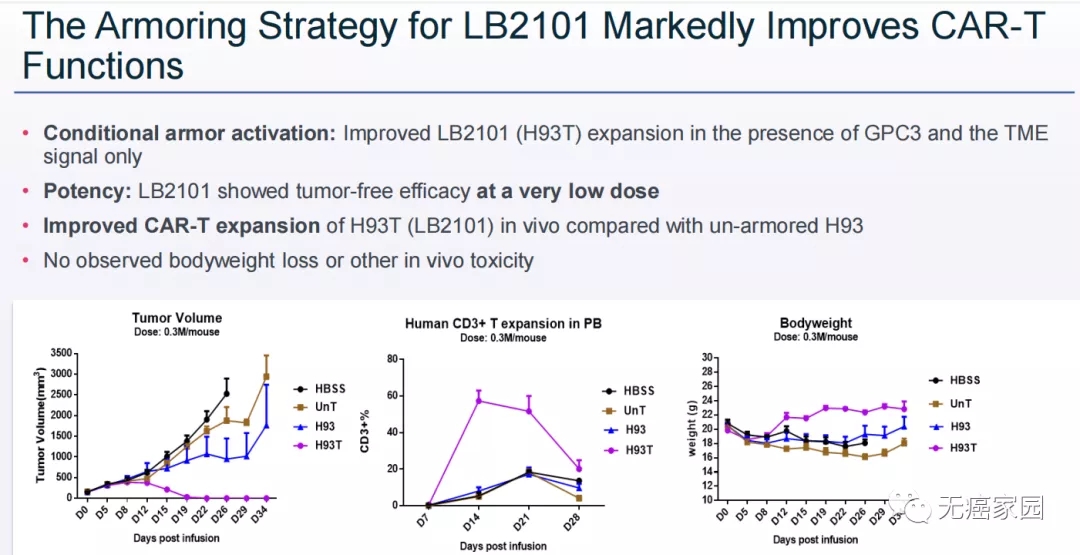
LB2101(紫色)显著改善CAR-T疗法功能
03、CAR-T疗法治疗小细胞肺癌
LB2102是一款靶向DLL3的CAR-T疗法。DLL3是一种在小细胞肺癌(SCLC)和某些神经内分泌肿瘤中广泛表达的潜在靶点。LB2102使用了VHH抗体技术和克服肿瘤微环境抑制因素的“武装”CAR-T技术。
临床前体内研究显示,这一疗法与传统CAR-T疗法相比,更有效地缩小肿瘤,而且外周血中的CAR-T细胞和浸润肿瘤的CAR-T细胞数目都显著提升。
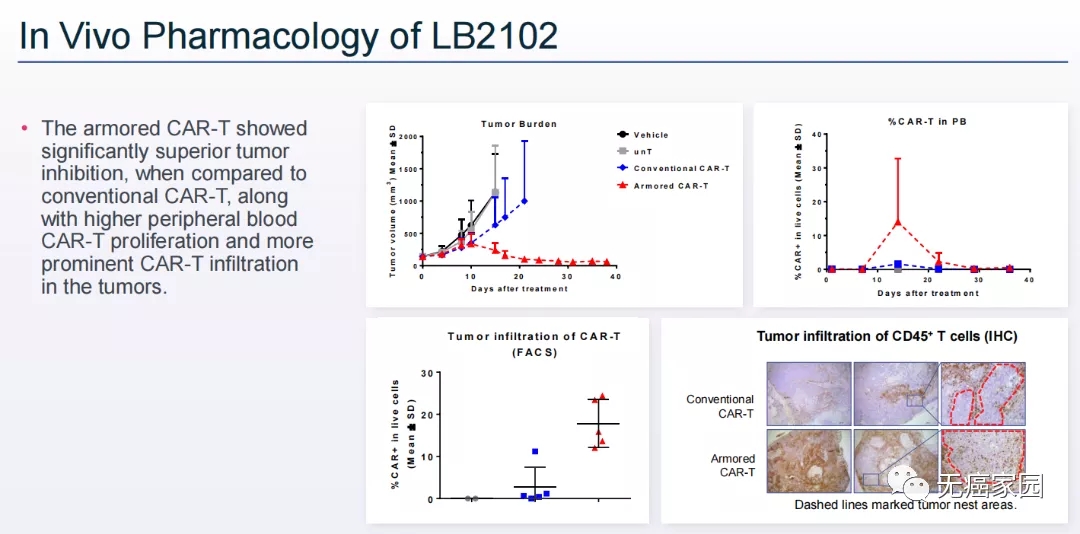
LB2102(红色)的体内动物实验结果
目前,无癌家园有多款实体瘤的CAR-T临床试验正在进行招募,有意向者可咨询医学部400-626-9916具体评估病情!
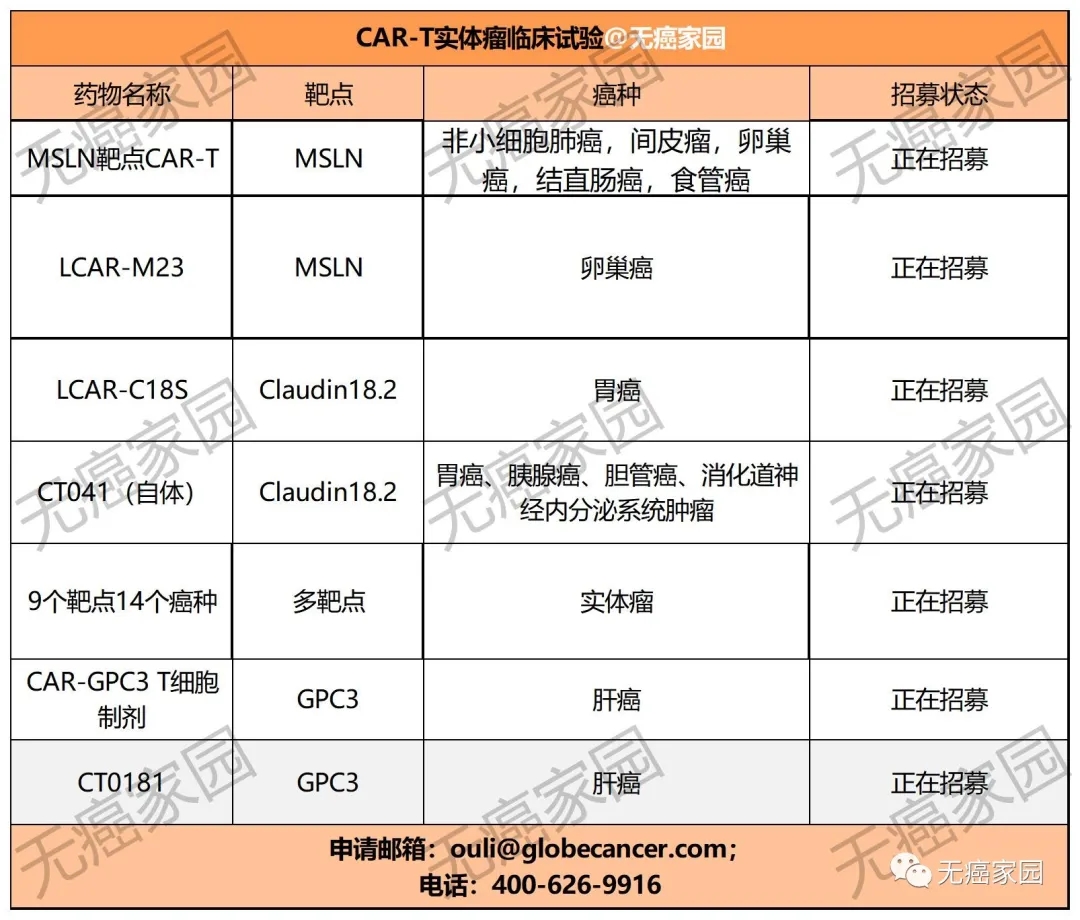
CAR-T疗法的获批将为中国患者带来更多临床获益
阿基仑赛注射液、瑞基奥仑赛注射液的纷纷获批上市,首先对符合其适应症的患者又增加了一种新的治疗选择,也就多了一份治愈的希望。
其次,这两次的获批意味着CAR-T疗法已经被国内环境所接纳,未来更多CAR-T产品或适应症的研发及审批都将得到提速。
经过近30年的发展,CAR-T细胞疗法已然兴起,该领域不会孤立的发展。目前已经有一些试验表示,很可能最好的肿瘤响应需要特异性的CAR-T疗法结合小分子治疗、免疫调节、化疗和基于抗体的治疗等多种治疗的协同作用,这些试验不提供特定的CAR,而是针对一些可能的抗原靶点设计CAR,这些抗原靶点取决于病人疾病的免疫表型。
在个性化医疗的时代,无论是单一疗法还是联合疗法,CAR-T无疑是医药领域火热的研究对象,希望今后能够取得更多突破,在血液肿瘤和实体瘤的治疗上展现其独特的实力!
参考文献
1.https://www.businesswire.com/news/home/20210526006114/en/
2.https://investors.legendbiotech.com/events/event-details/legend-biotech-rd-day-presentation
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
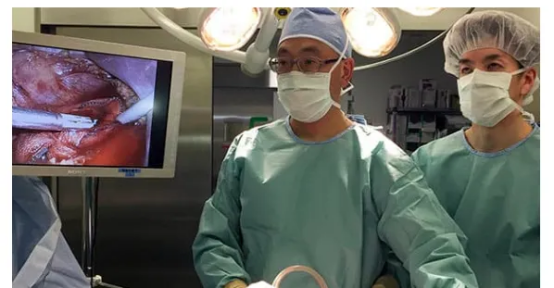
早期膀胱癌术后五年生存率高达90%,这五
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

警惕!乳腺癌复发偏爱这3大人群!术后一定
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【实体瘤溶溜病毒免费招募】溶瘤病毒Ml(
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
从多处转移到完全缓解!新型CAR-T细胞
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
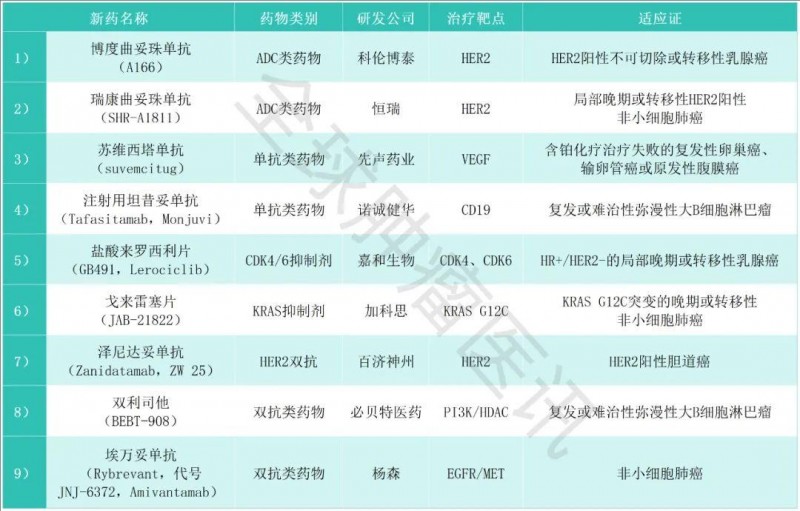
救命药加速入场!2025第二季度9款抗癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




