2025获批在即!六大ADC药物重磅来袭,精准狙击乳腺癌、肺癌等,疾病控制率高达81.0%
六大抗体偶联(ADC)药物2025年获批在即,精准狙击乳腺癌、肺癌等,疾病控制率高达81.0%
相较于化疗药物,ADC药物被誉为“魔法子弹”,其具备靶点识别精准以及对非癌细胞影响轻微等显著优势。它精妙地削减了小分子细胞毒素给正常组织带来的毒副作用,并且能够精确地锁定癌细胞并发起攻击,大幅提升了药物的综合疗效,在肿瘤治疗领域的重要性与日俱增,被广泛应用于血液系统恶性肿瘤以及实体瘤的治疗当中。
在2024岁末之际,多款ADC药物已做好充分准备,预计在2025年获批上市。小编悉心梳理并汇总了当前国内外处于研发阶段且有希望获批的ADC药物,旨在为众多癌症患者点燃战胜疾病的希望之火,早日冲破癌症阴霾!(以下信息仅供参考,具体用药方案需遵医嘱)。
"魔法子弹"ADC药物:开启精准抗癌的奥秘之门
抗体偶联药物(Antibody Drug Conjugates,ADC)是一类新型强效抗肿瘤药物,由由三部分组成,即选择性mAb(相当于细胞毒药物的“眼睛”)、稳定的连接子(相当于mAb与细胞毒药物的“桥梁”)、强效细胞毒药物(相当于杀伤癌细胞的“子弹头”)(详见下图),它们共同通过创建一种具有增强治疗效果的“新”化合物,来确保肿瘤特异性靶向和恶性细胞的有效消融。截至目前,全球已有多款ADC药物获批上市。阅读原文了解详情:【速览】2024年全球15款获批ADC药物大汇总,一文掌握!
▼ADC药物的组成
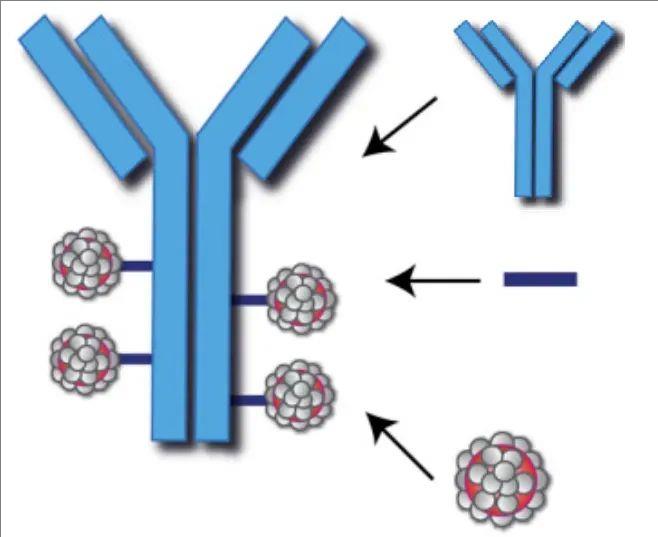
▲图源“Front Pharmacol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:ADC药物主要由三部分组成:即单克隆抗体(蓝色)、连接子(蓝线)、细胞毒性药物(灰色/红色)。
展望2025:六款ADC药物即将问世,深度盘点抢先看
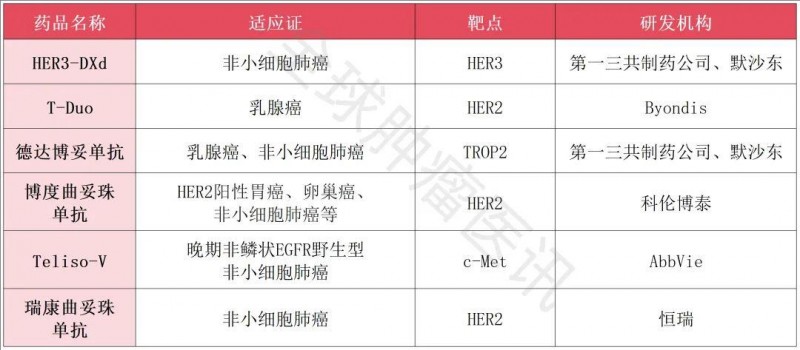
博度曲妥珠单抗
药品简介
①药物名称:博度曲妥珠单抗(A166,KL-A166,舒泰来)。
②研发公司:科伦博泰。
③治疗靶点:HER2。
药物介绍
博度曲妥珠单抗(KL-A166,A166)是一种HER2靶向的ADC药物,能够将高活性有效载荷递送至靶细胞,其显著优势是负载活性高,即使在相对较低的DAR下也能展现出优异的疗效,并且在循环中具有出色的稳定性。在美国首次人体研究(NCT03602079)的结果显示,该药物对复发或难治性晚期HER2突变的实体瘤(主要包括HER2阳性胃癌、HER2表达卵巢癌、HER2突变非小细胞肺癌),具有初步抗肿瘤活性。2023年5月,该药向国家药品监督管理局(NMPA)递交了上市申请,用于治疗晚期HER2+乳腺癌(3L+)。
临床试验数据
我国开展的一项A166治疗HER2表达局部晚期或转移性实体瘤的I期临床试验,共入组81例晚期实体瘤患者,包括73例乳腺癌、6例结直肠癌、2例胃癌或胃食管连接部癌。
结果显示:对于以4.8或6.0mg/kg治疗的58名HER2阳性乳腺癌患者,客观缓解率(ORR)达到70.7%(41/58;95%CI,57.3–81.9),疾病控制率(DCR)高达81.0%(47/58;95%CI,68.6–90.1)。中位无进展生存期(PFS)分别为12.3个月(4.8mg/kg组) vs 9.4个月(6.0mg/kg组)。
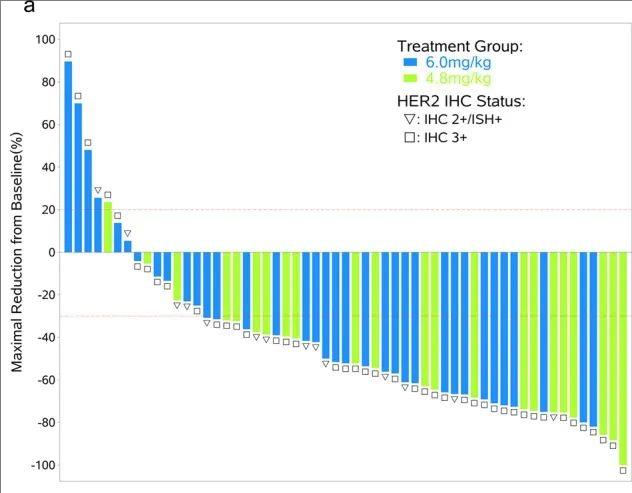
▲图源“NPJ Breast Cancer”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:使用RECIST v1.1评估,至少进行过一次治疗后放射学评估的患者,肿瘤靶病灶大小相对于基线的最大变化。条形图的长度表示靶病灶的最大减少量或最小增加量。
值得一提的是,其中1例激素受体阴性、HER2阳性乳腺癌且伴有淋巴结转移的患者,在接受4.8mg/kg剂量博度曲妥珠单抗治疗后,反应持续时间约为2年,治疗仍在继续。更为惊喜的是,经过6个疗程的治疗后,CT扫描显示靶病灶完全消失(详见下图)。
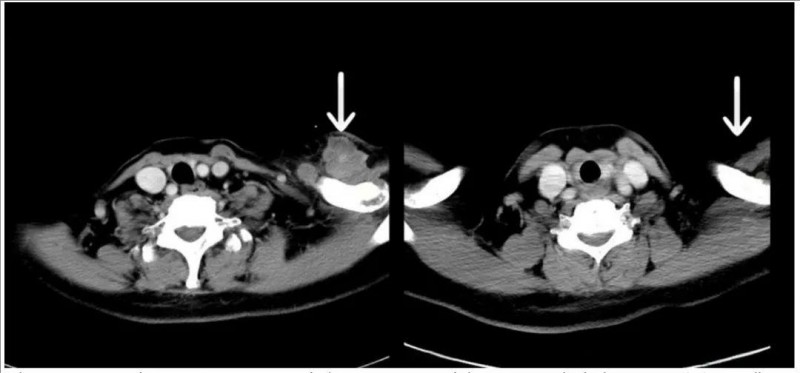
▲图源“NPJ Breast Cancer”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
HER3-DXd
药品简介
①药物名称:HER3-DXd(Patritumab deruxtecan,代号:U3-1402)。
②研发公司:第一三共制药公司、默沙东。
③治疗靶点:HER3。
药物介绍
HER3-DXd(Patritumab deruxtecan,代号:U3-1402)是一种针对人类表皮生长因子受体 3 (HER3) 的抗体-药物偶联物(ADC),2021年12月被美国食品药品监督管理局(FDA)授予突破性疗法认定,用于EGFR的局部晚期或转移性非小细胞肺癌(NSCLC)的治疗。
临床试验数据
HER3-DXd的Ⅱ期HERTHENA-Lung01临床研究(NCT04619004),共入组277例晚期EGFR突变的非小细胞肺癌(NSCLC) 患者,既往接受过EGFR 酪氨酸激酶抑制剂 (TKI) 治疗、铂类化疗(PBC) 治疗。
结果显示:BIC(盲法独立中央审查)确认的客观缓解率(ORR) 为 29.8%(95% CI,23.9~36.2);中位缓解持续时间(DOR)为 6.4 个月;中位无进展生存期(PFS)为 5.5 个月(详见下图);中位总生存期为 11.9 个月。
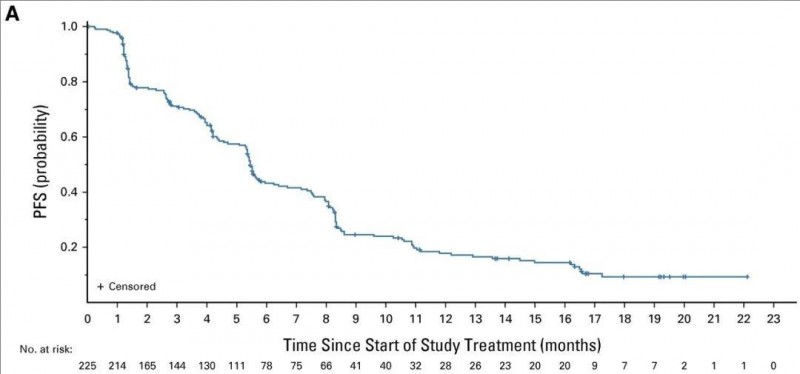
▲图源“J Clin Oncol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
值得一提的是,对疗效人群中 30 名基线时(HER3-DXd治疗前),患有脑转移(根据 CNS BICR)且之前未接受过脑部放射治疗的患者进行了颅内反应分析。基于CT成像结果显示:5例患者奇迹般获得完全缓解(CR)、1例患者达到部分缓解(PR)。下图显示了具有可测量靶病灶且已确认颅内完全缓解的患者的增强CT系列图像(详见下图)。
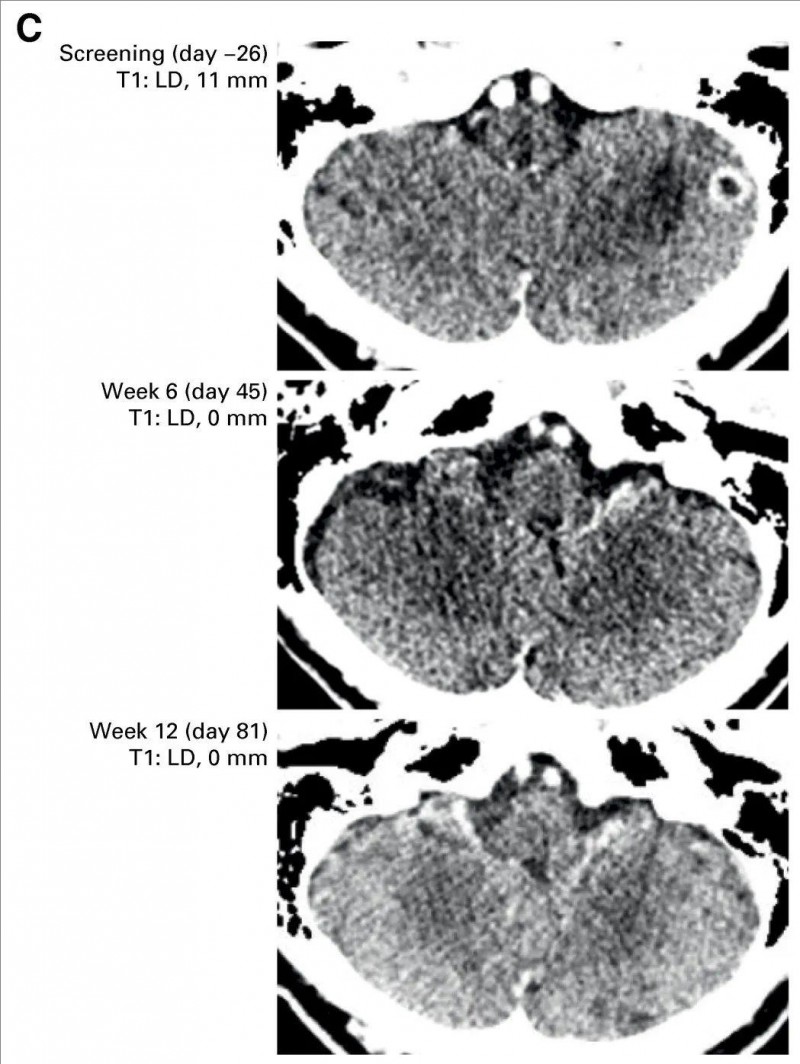
▲图源“J Clin Oncol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
T-Duo
药品简介
①药物名称:T-Duo(T-Duo,Trastuzumab duocarmazine,SYD985)。
②研发公司:Byondis。
③治疗靶点:HER2。
药物介绍
T-Duo是一种新型HER2靶向的抗体-药物偶联物,由曲妥珠单抗与含有二甲肼的连接药物共价结合而成。
临床试验数据
全球知名期刊《柳叶刀》公布了T-Duo的首次人体研究结果,根据RECIST,结果显示:
1、在乳腺癌剂量扩展队列中:
①48名可评估疗效的HER2阳性乳腺癌患者中有16名(33%,95%CI 20.4–48.4)获得了客观缓解。
②32名HER2低、激素受体阳性乳腺癌患者中,9名(28%,95%CI 13.8–46.8)达到了客观缓解。
②15名HER2低、激素受体阴性乳腺癌患者中有6名(40%,16.3–67.6)获得了客观缓解。
2、在其他队列中:
①16例胃癌患者中1例(6%,95%CI0.2-30.2)出现部分缓解;
②16例尿路上皮癌患者中4例(25%,7.3-52.4)出现部分缓解;
③13例子宫内膜癌患者中5例(39%,13.9-68.4)出现部分缓解。
▼可评估疗效患者目标病变中肿瘤大小相对于基线的最佳百分比变化
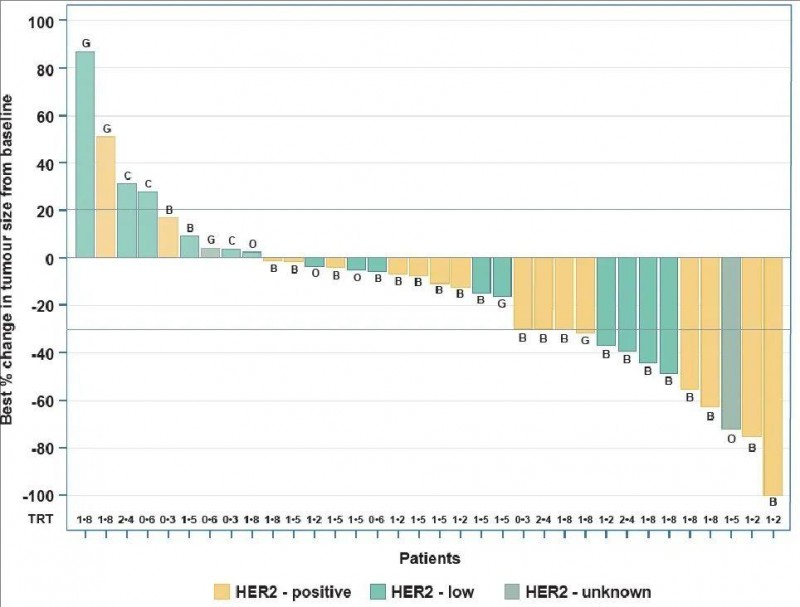
▲图源“Lancet”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
Teliso-V
药品简介
①药物名称:Telisotuzumab vedotin(Teliso-V,ABBV-399)。
②研发公司:AbbVie公司。
③治疗靶点:c-Met。
药物介绍
Teliso-V是一种针对c-Met的抗体-药物偶联物(ADC),具有单甲基 auristatin E 细胞毒性有效载荷,主要用于非小细胞肺癌(NSCLC)的治疗。
临床试验数据
Teliso-V第二阶段LUMINOSITY临床试验(NCT03539536)共入组172例I期和Ⅱ期非鳞状EGFR野生型非小细胞肺癌(NSCLC)患者,接受Teliso-V治疗。
结果显示:总客观缓解率(ORR)达到28.6%(95%CI,21.7~36.2)。其中,c-Met高表达的ORR达到34.6%(95%CI,24.2至46.2),c-Met中表达的ORR达到22.9%(95%CI,14.4至33.4)。大多数患者的肿瘤大小均有所缩小(详见下图)。
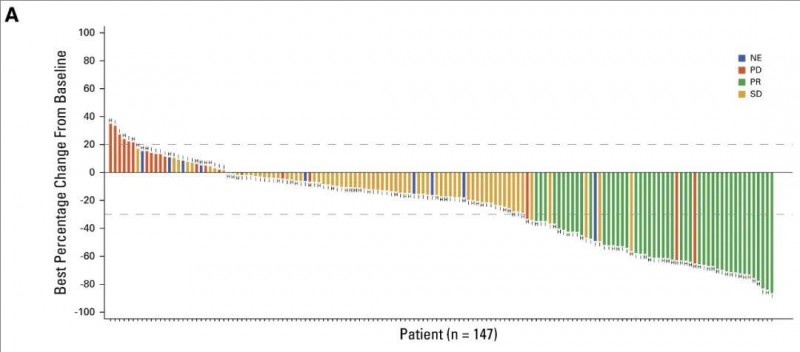
▲图源“ASCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
此外,全部入组患者的中位总生存期(PFS)达到5.7个月(95%CI,4.6至6.9)。其中,c-Met高表达组每ICR的中位PFS为5.5个月(95%CI,4.1至8.3),c-Met中度组为6.0个月(95%CI,4.5至8.1)。
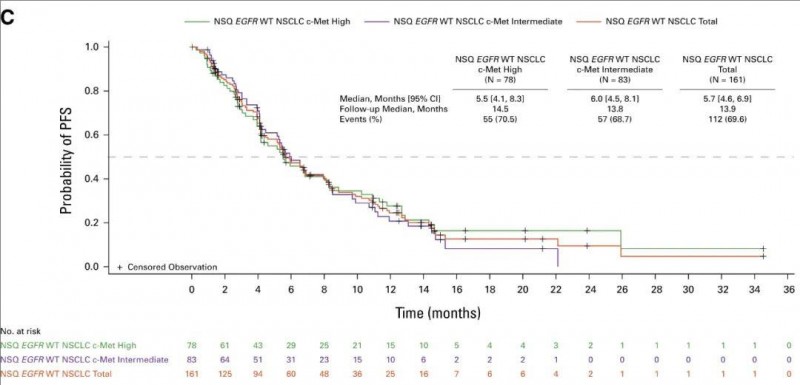
▲图源“ASCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
德达博妥单抗
药品简介
①药物名称:德达博妥单抗(Dato-DXd,datopotamab deruxtecan,代号:DS-1062a)。
②研发公司:第一三共制药公司、默沙东。
③治疗靶点:TROP2。
药物介绍
德达博妥单抗是一款靶向Trop-2的DXd抗体偶联药物(ADC),用于治疗不可切除或转移性激素受体(HR)阳性、HER2阴性乳腺癌、非小细胞肺癌等。
临床试验数据
德达博妥单抗的Ⅲ期TROPION-Lung01临床研究,总入组604例患者,将其分为两组,即德达博妥单抗组(Dato-DXd,299例)、多西他赛组(305例)。结果显示如下:
1、中位无进展生存期(PFS):中位PFS分别为4.4个月(Dato-DXd组,95%CI,4.2~5.6)vs 3.7个月(多西他赛组,95%CI,2.9至4.2)(详见下图)。
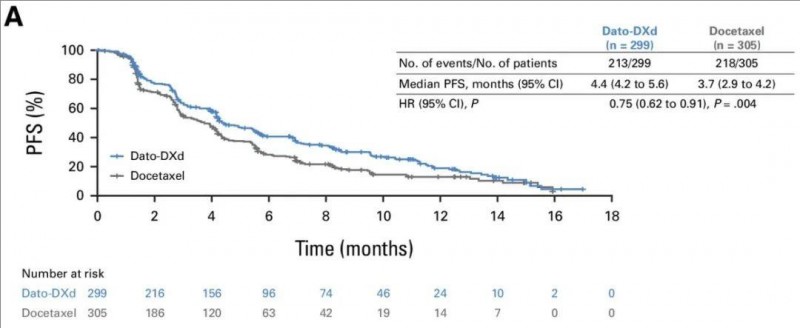
▲图源“ASCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
2、中位总生存期(OS):中位OS分别为12.9个月(Dato-DXd组,95% CI,11.0~13.9) vs 11.8 个月(多西他赛组,95% CI,10.1~12.8)。
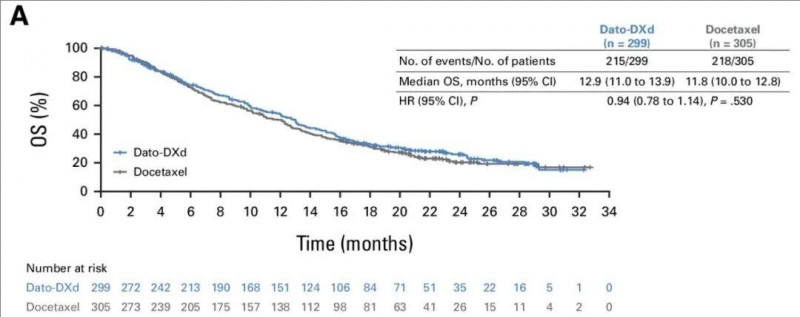
▲图源“ASCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
瑞康曲妥珠单抗
药品简介
①药物名称:瑞康曲妥珠单抗(SHR-A1811)。
②研发公司:恒瑞。
③治疗靶点:HER2。
药物介绍
瑞康曲妥珠单抗(SHR-A1811)是一款HER2靶向的ADC药物,2024年9月13日,该药的上市许可申请,或中国药监局受理并被纳入优先审评程序。
临床试验数据
瑞康曲妥珠单抗的1/2 期临床研究(NCT04818333)共入组63例既往接受过治疗的HER2突变的晚期非小细胞肺癌 (NSCLC) 患者。
结果显示:在所有 63 名患者中,客观缓解率(ORR)达到38.1%(95% CI 26.1–51.2)(详见下图),中位PFS 为9.5个月(95% CI 7.1–11.7)。
▼个体患者靶病变随时间变化的百分比
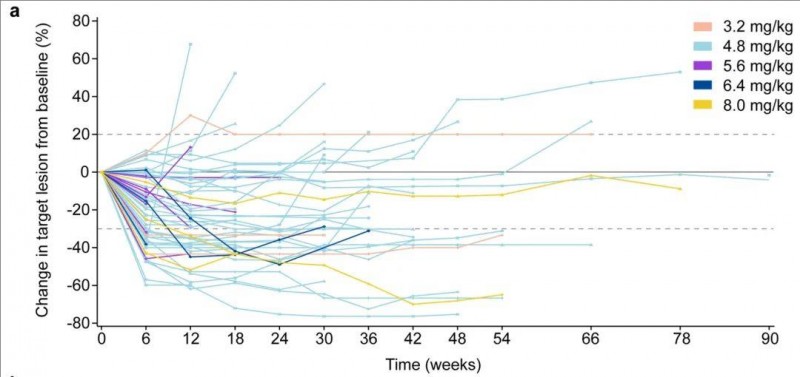
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
更多ADC药物上市在即,国内多中心启动临床
除了上文所提及的ADC药物之外,当前我国还有诸多处于研发进程中的ADC药物正蓄势待发并积极开展临床研究,值得一提的是,已有相当数量的患者借助全球肿瘤医生网抗癌新药招募中心这一桥梁,顺利入组并得以接受ADC抗癌新药的前沿治疗,开启了与病魔抗争的新征程。就拿针对Claudin18.2的ADC药物——TQB2103来说,近期就在针对胃癌以及胆道恶性肿瘤开展临床研究,,这无疑为相关患者群体带来了新的希望曙光与治疗契机。
新药简介
①药品名称:TQB2103。
②靶点:Claudin18.2。
③适应症:晚期恶性肿瘤(二线及以上)胃癌、胆道恶性肿瘤。
招募信息(部分)
1)经组织学或细胞学确认的晚期恶性肿瘤患者,经充分标准治疗后疾病进展或不耐受,或缺乏标准治疗方案,或目前不适用标准治疗,(标准治疗定义为:国内已有共识的标准治疗指南(如适用)或符合国内诊疗现状的标准治疗)。
2)年龄:18-75周岁(包含边界值、签署知情同意书时);ECOG PS评分:0-1分;预计生存期超过3个月。
3)优先入组能够提供新鲜采集或2年内采集保存的肿瘤组织标本以供进行Claudin18.2表达水平检测的患者,在剂量递增阶段无法提供标本的受试者也可以参加本研究,剂量扩展阶段需入组Claudin18.2表达阳性的受试者,具体阳性界值根据研究实际开展过程中的表达水平与疗效相关性确定。
4)根据RECIST v1.1标准,剂量递增阶段至少有一个可评估的肿瘤病灶,剂量扩展期至少有一个可测量病灶(接受放疗的病灶,根据RECISTv1.1标准评估后明确进展可作为靶病灶)。
申请流程
想申请抗癌新药临床试验的患者,需将近期病理报告、基因检测报告等资料汇总后,提交至医学部进行初步评估。
我们的专家将为您全面分析解读检测报告,预计一个工作日内电话联系推荐用药方案,并匹配适合患者入组的临床试验项目。注:作为国内权威的肿瘤患者服务平台,我们承诺对所有受试者的个人信息保密,并保证在整个过程中,遵循国家临床研究相关的法律法规。
小编寄语
ADC 药物在历经三代技术的革新演进后,已然具备了较为卓越的特性,既能精准且有选择性地把强效的抗肿瘤化学物质运输至靶细胞所在之处,并促使靶细胞被高效消除,同时巧妙地规避了严重的毒性脱靶效应。这般独特的优势使得它在向癌细胞发起猛烈攻击之时,还能周全地保护周围的正常细胞免受损伤。可以毫不夸张地讲,ADC 药物的应用正逐步重塑实体瘤以及血液肿瘤的治疗格局,为肿瘤治疗领域注入了全新的活力与希望。
好消息是,目前我国已有多款 ADC 药物相继获批上市,并且还有众多的临床试验正如火如荼地开展之中,这些试验广泛覆盖多个关键靶点,为无药可用的患者提供了一线转机。对此感兴趣的患者,可将过往的治疗经历、近期病理及影像学检查报告,提交至全球肿瘤医生网医学部,初步评估病情或了解详细的入排标准,初步评估是否有机会参与方舟计划获得免费用药的机会。
参考资料
[1]Zhang J,et al.Phase I study of A166, an antibody‒drug conjugate in advanced HER2-expressing solid tumours. NPJ Breast Cancer. 2023 Apr 18;9(1):28.
https://pmc.ncbi.nlm.nih.gov/articles/PMC10113253/
[2]Yu HA,et al.HERTHENA-Lung01, a Phase II Trial of Patritumab Deruxtecan (HER3-DXd) in Epidermal Growth Factor Receptor-Mutated Non-Small-Cell Lung Cancer After Epidermal Growth Factor Receptor Tyrosine Kinase Inhibitor Therapy and Platinum-based Chemotherapy. J Clin Oncol. 2023 Dec 10;41(35):5363-5375.
https://ascopubs.org/doi/10.1200/JCO.23.01476
[3]Banerji U,et al.Trastuzumab duocarmazine in locally advanced and linkstatic solid tumours and HER2-expressing breast cancer: a phase 1 dose-escalation and dose-expansion study[J]. The Lancet Oncology, 2019, 20(8): 1124-1135.
https://www.thelancet.com/journals/lanonc/article/PIIS1470-2045(19)30328-6/abstract
[4]Camidge D R,et al.Telisotuzumab Vedotin Monotherapy in Patients With Previously Treated c-Met Protein–Overexpressing Advanced Non-Squamous EGFR-Wildtype NSCLC in the Phase 2 LUMINOSITY Trial[J]. Journal of Clinical Oncology, 2024: JCO. 24.00720.
https://ascopubs.org/doi/10.1200/JCO.24.00720
[5]Ahn M J,et al.Datopotamab deruxtecan versus docetaxel for previously treated advanced or linkstatic non–small cell lung cancer: The randomized, open-label phase III TROPION-Lung01 study[J]. Journal of Clinical Oncology, 2024: JCO-24-01544.
https://ascopubs.org/doi/10.1200/JCO-24-01544
[6]Li Z,et al.SHR-A1811 (antibody-drug conjugate) in advanced HER2-mutant non-small cell lung cancer: a multicenter, open-label, phase 1/2 study[J]. Signal Transduction and Targeted Therapy, 2024, 9(1): 182.
https://www.nature.com/articles/s41392-024-01897-y
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
里程碑!mRNA-4157联合派姆单抗让
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

刚刚!"双免王炸"纳
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2025肺癌生存新希望:六大"
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
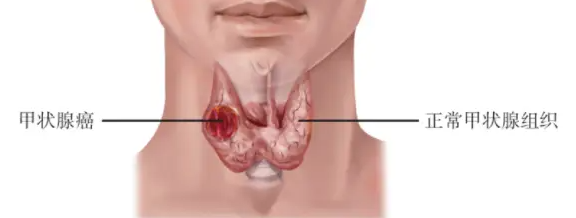
早期甲状腺癌术后五年生存率超99%,但要
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
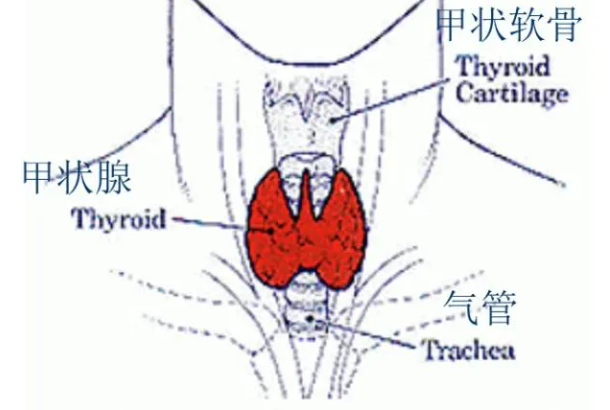
早期甲状腺癌术后五年生存率超99%!但忽
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




