陈明教授:放疗联合免疫,值得期待的小细胞肺癌新策略
陈明教授:小细胞肺癌放疗联合免疫治疗,值得期待的新策略
陈明教授解读小细胞肺癌的放射治疗
肺癌是中国发病率与死亡率最高的癌种,近年来中国肺癌发病率呈现增长趋势。根据病理类型,肺癌可以分为非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC),其中SCLC约占肺癌的15%-20%。
SCLC是一种侵袭性强、增殖迅速的恶性肿瘤。患者预后很差,多数患者疾病发现时已出现了远端器官或淋巴结转移。化疗是SCLC常用治疗手段,但患者往往很快出现耐药,五年生存率很低。今年获国家药品监督管理局批准的免疫药物阿替利珠单抗给SCLC患者带来了30年来前所未有的突破,患者死亡风险明显降低。
除化疗、免疫治疗外,放疗在SCLC中的发展如何呢?其联合免疫治疗是否会给患者带来更多获益呢?医学界肿瘤频道有幸邀请到中国科学院大学附属肿瘤医院常务副院长、胸部肿瘤放疗科陈明教授,就放疗手段在SCLC的应用现状和进展进行了全方位解答。
问:局限期SCLC一般采用化疗+放疗的手段,放疗的靶区该如何选择?推荐的放疗剂量是怎样的?
答:多年来,SCLC的治疗仍然是最难啃的骨头,但好在免疫治疗让它曙光初现。上世纪90年代,在局限期SCLC的治疗中,我们发现局限期SCLC患者单纯化疗失败概率高达75%-90%,这时候化疗联合放疗就逐渐引起了人们的重视。虽然当时联合治疗取得了一些成就,但放射治疗技术相对粗糙,随着加速器技术、计算机技术应用之后,放射治疗进入了三维适形放疗和调强放疗的时代,其技术取得了长足的进步。
一般而言,SCLC患者就诊时肿瘤较大,同期放化疗往往照射范围较大,所以建议患者诱导化疗1程后开始同期放化疗。但对于多程化疗的患者,诱导化疗后局限期SCLC放疗靶区的勾画面临一个问题:按原发病灶化疗前范围照射还是照射化疗后残留病灶?
我们经过长达15年的研究证实,只照射化疗后肿瘤范围不会增加患者复发风险,对总体生存无明显影响,并且还减轻了放疗的毒副作用。同时,我也不建议患者做纵膈淋巴结引流区的预防性放疗。
关于放射治疗的剂量一直存在争议。放疗技术进步了,我们可以比较安全地将剂量从45Gy加到60Gy再加到70Gy,那疗效有所改善吗?研究结果是令人失望的,从45Gy提高到66-70Gy之后并没有带来疗效的提高,所以目前的标准的剂量仍然是45Gy-60Gy。
问:对于广泛期SCLC患者来说,胸部放疗效果如何?广泛期SCLC患者脑转移发生几率较高,脑预防性照射(PCI)真的能够达到预防的作用吗?
答:广泛期SCLC患者2年内脑转移的概率非常高,化疗药物无法入脑。早在1999年,研究者就发现了胸部放疗在广泛期SCLC中的价值,化疗后远处转移灶完全缓解的患者联合胸部照射后中位无进展生存期(PFS)明显延长,五年生存率也显著提高。目前,化疗后有效患者的患者胸部放疗已经成为广泛期SCLC的标准治疗方案。
但化疗后完全缓解患者的转移淋巴瘤区域需要给与照射吗?这点要具体情况具体分析,结合患者的病变转移情况和患者耐受情况选择照靶区和剂量。比如70岁以上老年患者应慎用PCI,对PCI产生血液学毒性的患者建议禁用PCI。
2007年《新英格兰医学杂志》发表了一项多中心研究,研究显示化疗有效的广泛期SCLC患者接受PCI后中位PFS明显提高。该研究也使得PCI成为当时化疗有效的广泛期SCLC的标准治疗。可后来一项日本研究推翻了这一结论,虽然接受PCI患者的脑转移情况有所降低,但是患者生存率却不乐观。那么广泛期SCLC患者还做不做PCI呢?目前,国外指南中对于广泛SCLC患者的PCI推荐级别为Ⅱ级,建议临床中根据患者具体情况实施PCI。
问:放射和免疫之间的关系,几十年前就受到了放射肿瘤学界的关注。在出现了PD-L1/PD-1抑制剂之后,放射跟它们之间的联合迅速成为了热点。那么在SCLC领域,免疫治疗联合放疗,能否达到事半功倍的效果?
答:我参加了近两年美国的放疗年会,去年还担任了免疫放疗分会场的共同主席,热点研究都是探讨如何将免疫治疗与放射联合在一起提高疗效。一般而言,放射线在照射肿瘤后,可以产生新的抗原,增加抗原递呈的效率和程度。从这一点出发,放射治疗与免疫治疗之间是一对天然的好“搭档”。
我们看到在IMpower133研究中,阿替利珠单抗联合化疗给广泛期SCLC带来前所未有的获益。阿替利珠单抗联合化疗可以显著降低疾病恶化和死亡风险(PFS:5.2 vs 4.3个月;HR=0.77,95% CI: 0.62-0.96;p=0.017);在13.9个月的随访中,试验组疾病持续缓解的患者比例是化疗组的3倍(15% vs. 5%);在更长时间的随访中,接受阿替利珠单抗联合化疗组,有1/3的患者生存超过18个月,对比化疗组的21%有明显的升高。目前阿替利珠单抗已经在中国上市,它是30年来我国广泛期SCLC一线治疗的首次重大突破。
免疫联合放疗的机制是什么呢?事实上,放疗可以诱导肿瘤和宿主细胞的免疫原性死亡,刺激肿瘤和自身抗原释放,从而导致向T细胞的抗原递呈增加。放疗后PD-L1表达增加,阻断PD轴再次活化CD8+T细胞,此时联合PD-L1抑制剂,可升高肿瘤坏死因子-α(TNF-α),改善T细胞功能。同时,放疗可增加肿瘤细胞对MHC-1和应激诱导的NK细胞刺激配体表达,肿瘤细胞上的MHC-1结合NK细胞上的KIR2DL,降低NK细胞活性。
如果在阿替利珠单抗联合化疗的治疗基础上,引入放疗,我们应注意什么呢?事实上,许多患者仍然对放疗的副作用心存疑虑,尤其是放射性肺炎。对此,放射医生和患者都应对放射治疗有信心,目前放射治疗总体的安全是可控的。同时放射科医生也应与内科医生紧密合作,掌握放疗、化疗以及免疫治疗序贯的经验。
问:在SCLC领域,放疗和免疫治疗未来发展的趋势和挑战有哪些?
答:目前的探索热点是将放疗直接与免疫检查点抑制剂同步或序贯使用,去掉化疗,这是否比传统的同步放化疗效果更好,毒性更低呢?非常值得我们期待,“去化疗”也是未来的趋势和挑战。
目前正在进行局限期SCLC患者中同步放化疗后,序贯使用阿替利珠单抗,对比单独同步放化疗的临床II期研究(ACHILES研究),以及局限期SCLC患者中同步放化疗,同步联合使用阿替利珠单抗及后续维持治疗,对比单独同步放化疗的II/III期(NRG LU005研究),期待它们的结果。此外,还有一些值得我们关注的免疫联合化疗的研究,例如STIMULI研究,探索了双免疫联合在局限期SCLC肺癌患者中放化疗后维持治疗的效果。这几个研究都是我比较关注的。
相信放疗结合免疫治疗,会给早期到晚期的SCLC带来治疗方式和疗效的改变。目前,越来越多的临床试验正在启动和进行的过程中,我们也期待有更多更好的结果。
专家介绍

陈明教授
中国科学院肿瘤与基础医学研究所/中国科学院大学附属肿瘤医院常务副院长,浙江省放射肿瘤学重点实验室主任,浙江省肺癌诊治研究中心主任,中华医学会放射肿瘤治疗学分会秘书长,中国临床肿瘤学会(CSCO)肿瘤放疗专委会副主任委员。
内容来源:医学界肿瘤频道
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
早期膀胱癌术后五年生存率高达90%,这五
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

警惕!乳腺癌复发偏爱这3大人群!术后一定
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【实体瘤溶溜病毒免费招募】溶瘤病毒Ml(
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
从多处转移到完全缓解!新型CAR-T细胞
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
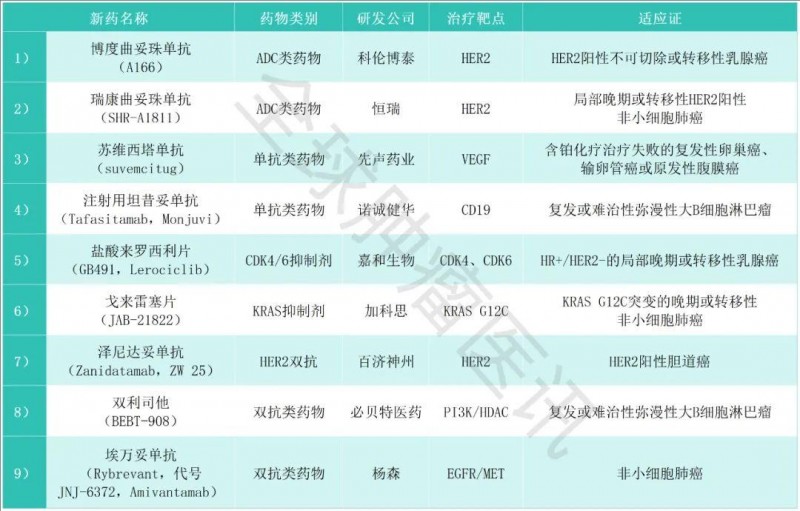
救命药加速入场!2025第二季度9款抗癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




