2024上半年,我国28款重磅抗癌新药获批上市!肺癌、肝癌、胃癌等终于有新药可用了!
肿瘤新药,2024年上半年中国有28款抗癌新药获批上市,肺癌、肝癌、胃癌等终于有新药可用了
癌症患者尤其是对现有抗癌药物耐药的患者,往往面临着“无药可用”的困境。在十年前,一种抗癌新药从开始申请、纳入医保目录,到最终应用于患者,可能需要数年的时间,很多患者在苦苦等待中绝望离去。
近年来,随着我国医学技术的不断发展,我国自研的抗癌新药、新技术不断涌现,逐渐打破癌症患者无药可用的僵局。在2024年上半年,我国就有35款抗癌新药获得国家药品监督管理局(NMPA)批准上市,为肺癌、肝癌、胃癌、肾癌、乳腺癌等多款癌症患者带来希望的曙光!
全球肿瘤医生网医学部每年年中及年终,都会参照国家药品监督管理局(NMPA)官网的药品获批信息,为大家整理、汇总所有新获批的癌症靶向药物,助癌症患者重拾斗争的决心!
2024上半年,中国NMPA获批药物汇总
非小细胞肺癌
1、非小细胞肺癌-特瑞普利单抗
药物名称:特瑞普利单抗(Toripalimab,LOQTORZ,拓益®)
研发公司:君实生物
上市时间:2024年1月2日
药物介绍:特瑞普利单抗是君实生物自主研发的一款抗PD-1单抗药物,也是我国批准上市的首个以PD-1为靶点的国产单抗药物。2024年1月2日,特瑞普利单抗的新适应症获得国家药品监督管理局(NMPA)批准上市,特瑞普利单抗联合化疗围手术期治疗,用于成人可切除的IIIA-IIIB期非小细胞肺癌(NSCLC)。这是特瑞普利单抗在中国获批的第7个适应症,同时也是我国首个、全球第二个获批的肺癌围手术期疗法。
2、非小细胞肺癌-伊鲁阿克
药物名称:伊鲁阿克(代号为WX-0593)
研发公司:齐鲁制药
上市时间:2024年1月16日
药物介绍:伊鲁阿克是国研的新一代ALK抑制剂,可通过抑制ALK和ROS1激酶的磷酸化,进而阻断AKT、STAT5、ERK等下游信号通路蛋白的激活,从而诱导肿瘤细胞的死亡/凋亡。2024年1月16日,伊鲁阿克的新适应症的上市申请正式获得国家药品监督管理局(NMPA)的批准,用于治疗间变性淋巴瘤激酶(ALK)阳性的局部晚期或转移性非小细胞肺癌(NSCLC),该适应症覆盖全部ALK阳性局部晚期或转移性的NSCLC患者人群。
3、非小细胞肺癌-安奈克替尼
药物名称:安奈克替尼(unecritinib,代号:TQ-B3101)
研发公司:正大天晴
上市时间:2024年4月24日
药物介绍:安奈克替尼是中国生物制药宣布其下属企业正大天晴自主研发的一款多靶向(ROS1、ALK、c-MET)的小分子抑制剂,可选择性地抑制ROS1阳性等肿瘤细胞的体外增殖,从而诱导肿瘤细胞凋亡。2024年4月24日,安奈克替尼获得中国国家药品监督管理局(NMPA)批准上市,用于治疗ROS1阳性的局部晚期或转移性非小细胞肺癌(NSCLC)成年患者。
4、非小细胞肺癌-瑞普替尼
药物名称:瑞普替尼(Repotrectinib,奥凯乐®,代号TPX-0005)
研发公司:百时美施贵宝公司(Bristol-Myers Squibb Company)
上市时间:2024年5月13日
药物介绍:瑞普替尼是靶向作用于ROS1和NTRK致癌因子的新一代酪氨酸激酶抑制剂。2024年5月13日,瑞普替尼获得中国国家药品监督管理局(NMPA)批准,用于治疗ROS1阳性的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。
5、非小细胞肺癌-瑞齐替尼
药物名称:瑞齐替尼(甲磺酸瑞齐替尼胶囊,瑞必达®)
研发公司:倍而达药业
上市时间:2024年5月20日
药物介绍:倍而达药业自主研发的瑞齐替尼是一款不可逆、高选择性的第三代小分子表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)。2024年5月20日,获国家药品监督管理局(NMPA)批准,用于成人EGFR T790M突变阳性的局部晚期或转移性非小细胞肺癌(NSCLC)的治疗,这些患者既往接受表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)治疗时或治疗后,出现疾病进展。
6、非小细胞肺癌-卡马替尼
药物名称:卡马替尼(Capmatinib,INC280,Tabrecta®,妥瑞达®)
研发公司:诺华制药
上市时间:2024年6月12日
药物介绍:卡马替尼作为一种口服的高选择性小分子MET抑制剂,可有效抑制MET和MET介导的下游信号蛋白的磷酸化,从而抑制肿瘤细胞的增殖和迁移。2024年6月12日,获中国国家药品监督管理局批准上市,用于未经系统治疗的携带间质上皮转化因子(MET)外显子14跳跃突变的局部晚期或转移性非小细胞肺癌(NSCLC)的成人患者。
7、非小细胞肺癌-瑞厄替尼
药物名称:瑞厄替尼(甲磺酸瑞厄替尼片,圣瑞沙®)
研发公司:圣和药业
上市时间:2024年6月17日
药物介绍:瑞厄替尼是一种表皮生长因子受体(EGFR)激酶抑制剂,2024年6月17日,获国家药品监督管理局(NMPA)批准,适用于存在EGFR T790M突变阳性的局部晚期或转移性非小细胞肺癌(NSCLC)的成年患者,这些患者既往接受过EGFR酪氨酸激酶抑制剂(TKI)治疗时或治疗后,出现病情进展。该药的成功上市,为此类非小细胞肺癌患者提供了新的希望与治疗选择!
8、非小细胞肺癌-依奉阿克
药物名称:依奉阿克(Envonalkib,TQ-B3139,安洛晴®)
研发公司:正大天晴
上市时间:2024年6月17日
药物介绍:依奉阿克是一款小分子ALK/ROS1/c-MET抑制剂,通过选择性地抑制ALK/ROS1/c-MET阳性细胞的生长,促使肿瘤消退。该药于2024年6月17日,获国家药品监督管理局批准,用于ALK阳性的局部晚期或转移性非小细胞肺癌(NSCLC),且既往未接受过ALK抑制剂治疗。
9、非小细胞肺癌-依沃西单抗
药物名称:依沃西单抗(Ivonescimab,AK112)
研发公司:康方生物
上市时间:2024年5月24日
药物介绍:依沃西单抗(AK112)是一款国研的新型PD-1/VEGF双特异性抗体,具有独特的“肿瘤免疫+抗血管生成”双靶点协同抗肿瘤作用机制,既可阻断PD-1与PD-L1和PD-L2的结合,还可同时阻断VEGF与VEGF受体的结合。2024年5月24日,获国家药品监督管理局(NMPA)批准上市,依沃西单抗与化疗(培美曲塞+卡铂)联合,用于EGFR突变的局部晚期或转移性非鳞状非小细胞肺癌(nsq-NSCLC)的治疗,这些患者既往经表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)治疗后,病情仍继续进展。值得一提的是,依沃西单抗是全球首个获批上市的“肿瘤免疫+抗血管生成”机制的双特异性抗体新药。
10、非小细胞肺癌-奥希替尼
药物名称:奥希替尼(Tagrisso)
研发公司:阿斯利康
上市时间:2024年6月25日
药物介绍:2024年6月25日,国家药品监督管理局(NMPA)批准奥希替尼联合含铂化疗,用于成人患者具有表皮生长因子受体(EGFR)19号外显子缺失突变或21号外显子置换突变(L858R)的局部晚期或转移性非小细胞肺癌(NSCLC)的一线治疗。在此之前,该药已于2024年2月16日,获得美国食品药品监督管理局(FDA)批准。
小细胞肺癌
1、小细胞肺癌-特瑞普利单抗
药物名称:特瑞普利单抗(Toripalimab,LOQTORZ,拓益®)
研发公司:君实生物
上市时间:2024年6月12日
药物介绍:2024年6月12日,国家药品监督管理局(NMPA)批准特瑞普利单抗新适应症的上市申请,与依托泊苷和铂类联合,用于广泛期小细胞肺癌(ES-SCLC)的一线治疗,这是特瑞普利单抗在中国内地获批的第9项适应症。
2、小细胞肺癌-替雷利珠单抗
药物名称:替雷利珠单抗(tislelizumab-jsgr,TEVIMBRA®,百泽安®)
研发公司:百济神州
上市时间:2024年4月24日
药物介绍:替雷利珠单抗是我国自主研发的一款人源化免疫球蛋白G4(IgG4)抗程序性细胞死亡蛋白1(PD-1)单克隆抗体。2024年4月24日,国家药品监督管理局(NMPA)批准替雷利珠单抗与依托泊苷和铂类化疗联用,作为广泛期小细胞肺癌(ES-SCLC)患者的一线治疗。
3、小细胞肺癌-贝莫苏拜单抗
药物名称:贝莫苏拜单抗(安得卫®)
研发公司:正大天晴旗下南京顺欣制药
上市时间:2024年5月9日
药物介绍:贝莫苏拜单抗注射液是正大天晴药业集团南京顺欣制药自主研发的1类创新药,2024年5月9日,收到国家药品监督管理局(NMPA)核准签发的《药品注册证书》,与安罗替尼及化疗(卡铂、依托泊苷)联用,作为广泛期小细胞肺癌(ES-SCLC)患者的一线治疗。
乳腺癌
1、乳腺癌-特瑞普利单抗
药物名称:特瑞普利单抗(Toripalimab,LOQTORZ,拓益®)
研发公司:君实生物
上市时间:2024年6月25日
药物介绍:2024年6月25日,特瑞普利单抗新适应症的上市申请获得国家药品监督管理局(NMPA)批准,与紫杉醇(白蛋白结合型)联合,用于PD-L1阳性(CPS≥1)的复发或转移性三阴性乳腺癌(TNBC)的一线治疗,这是特瑞普利单抗在中国内地获批的第10个适应症。
2、乳腺癌-帕妥珠曲妥珠单抗注射液
药物名称:帕妥珠曲妥珠单抗注射液(Subcutaneous Injection,赫捷康®,Phesgo®)
研发公司:罗氏制药
上市时间:2024年1月2日
药物介绍:帕妥珠曲妥珠单抗注射液是美国罗氏制药研发的一款将曲妥珠单抗和帕妥珠单抗两药组合的复方制剂。2024年1月2日,获中国国家药品监督管理局(NMPA)批准,用于成人HER2阳性早期和转移性乳腺癌的治疗。值得一提的是,帕妥珠曲妥珠单抗注射液是全球首个复方皮下制剂,突破了肿瘤单抗类药物传统给药方式的技术瓶颈,颠覆了乳腺癌靶向治疗的传统治疗模式!
3、乳腺癌-恩替司他片
药物名称:恩替司他片(恩替诺特,景助达,EDP-103)
研发公司:亿腾景昂
上市时间:2024年4月24日
药物介绍:恩替司他片是一种组蛋白去乙酰化酶(HDAC)抑制剂,可选择性抑制I类和IV类HDACs,抑制细胞增殖、促进终末分化和/或诱导凋亡,发挥抗肿瘤作用。2024年4月24日,获国家药品监督管理局(NMPA)批准上市,与芳香化酶抑制剂联合,治疗激素受体(HR)阳性、人类表皮生长因子受体-2(HER-2)阴性,经内分泌治疗复发或进展的局部晚期或转移性乳腺癌。
肾细胞癌
特瑞普利单抗
药物名称:特瑞普利单抗(Toripalimab,LOQTORZ,拓益®)
研发公司:君实生物
上市时间:2024年4月7日
药物介绍:2024年4月7日,特瑞普利单抗的新适应症获得国家药品监督管理局(NMPA)批准,瑞普利单抗与阿昔替尼联合,用于中高危的不可切除或转移性肾细胞癌患者的一线治疗。这是特瑞普利单抗在中国获批的第八项适应症,也是我国首个获批的肾癌免疫疗法。
胃和胃食管结合部腺癌
1、胃和胃食管结合部腺癌-替雷利珠单抗
药物名称:替雷利珠单抗(tislelizumab-jsgr,TEVIMBRA®,百泽安®)
研发公司:百济神州
上市时间:2024年4月30日
药物介绍:2024年4月30日,替雷利珠单抗的新适应症获国家药品监督管理局(NMPA)批准,与氟尿嘧啶类和铂类化疗药物联合,用于局部晚期不可切除或转移性的胃或胃食管结合部(G/GEJ)腺癌的一线治疗。在此之前,替雷利珠单抗就已于2023年2月,获批用于PD-L1高表达的局部晚期不可切除/转移性G/GEJ腺癌的一线治疗。本次获批进一步验证了,无论PD-L1表达如何,替雷利珠单抗联合化疗,均可作为晚期胃癌的一线治疗手段。
2、胃和胃食管结合部腺癌-舒格利单抗
药物名称:舒格利单抗(择捷美®)
研发公司:基石药业
上市时间:2024年3月15日
药物介绍:2024年3月15日,舒格利单抗的新适应症获国家药品监督管理局(NMPA)批准,与氟尿嘧啶类和铂类药物联合,用于表达PD-L1[综合阳性评分(CPS)≥5]的不可切除的局部晚期或转移性胃和胃食管结合部腺癌的一线治疗,这是舒格利单抗在中国获批的第五项适应症。值得一提的是,舒格利单抗是全球首个在胃/胃食管结合部腺癌适应症获批的PD-L1单抗药物。
3、胃和胃食管结合部腺癌-帕博利珠单抗
药物名称:帕博利珠单抗(派姆单抗,pembrolizumab,Keytruda)
研发公司:默沙东(MSD)公司
上市时间:2024年6月25日
药物介绍:帕博利珠单抗是由默沙东(MSD)公司研发的一款重磅抗PD-1抑制剂,也是中国首个获批上市的PD-1抑制剂。2024年6月25日,帕博利珠单抗又一项新适应症的上市申请,获得国家药品监督管理局(NMPA)批准,与曲妥珠单抗、含氟尿嘧啶类和铂类药物化疗联合,用于表达PD-L1(CPS≥1)的局部晚期不可切除或转移性HER2阳性胃或胃食管结合部腺癌患者的一线治疗。至此,帕博利珠单抗在中国获批的适应证已达到14个。
肝细胞癌
替雷利珠单抗
药物名称:替雷利珠单抗(tislelizumab-jsgr,TEVIMBRA®,百泽安®)
研发公司:百济神州
上市时间:2024年1月2日
药物介绍:2024年1月2日,百济神州自主研发的PD-1抑制剂——替雷利珠单抗的新适应症,获得国家药品监督管理局(NMPA)批准,单药用于不可切除或转移性肝细胞癌(HCC)患者的一线治疗,这也是替雷利珠单抗在中国获批的第12项适应症。
结直肠癌
西妥昔单抗β注射液
药物名称:西妥昔单抗β注射液(恩立妥®,代号CMAB009)
研发公司:先声药业、迈博药业
上市时间:2024年6月25日
药物介绍:2024年6月25日,先声药业与迈博药业合作研发的新一代靶向EGFR的抗体药物——西妥昔单抗β注射液,获国家药品监督管理局(NMPA)批准上市,与FOLFIRI方案联合用于RAS/BRAF基因野生型转移性结直肠癌的一线治疗。值得一提的是,该药的获批填补了我国近20年来,结直肠癌的EGFR靶向抗体药物的空白,弥补了此类患者仅能依靠进口药物的困境!
卵巢癌、输卵管癌或原发性腹膜癌
氟唑帕利
药物名称:氟唑帕利(艾瑞颐®️)
研发公司:恒瑞医药
上市时间:2024年5月15日
药物介绍:氟唑帕利是恒瑞医药自主研发的一款PARP抑制剂,2024年5月15日,获国家药品监督管理局(NMPA)批准上市,用于晚期上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者,在一线含铂化疗达到完全缓解或部分缓解后的维持治疗,这是氟唑帕利获批上市的第3个适应症。值得一提的是,氟唑帕利也成为在一线全人群中第2个获批该适应症的PARP抑制剂,将为晚期卵巢癌患者一线维持治疗提供新的选择!
胆道癌
帕博利珠单抗
药物名称:帕博利珠单抗(派姆单抗,pembrolizumab,Keytruda)
研发公司:默沙东(MSD)公司
上市时间:2024年2月4日
药物介绍:2024年2月4日,国家药品监督管理局(NMPA)批准,帕博利珠单抗与吉西他滨和顺铂联用,用于局部晚期或转移性胆道癌(BTC)患者的一线治疗。
星形细胞瘤或胶质母细胞瘤
伯瑞替尼
药物名称:伯瑞替尼(Vebreltinib,bozitinib)
研发公司:鞍石生物旗下浦润奥生物
上市时间:2024年4月23日
药物介绍:伯瑞替尼是针对c-Met的单靶点小分子靶向药物,2024年4月23日,国家药品监督管理局(NMPA)批准了伯瑞替尼的新适应症,用于既往接受过放疗、替莫唑胺(TMZ)治疗后复发或不可耐受的,具有PTPRZ1-MET(ZM)融合基因的IDH(异柠檬酸脱氢酶)突变型WHO 4级星形细胞瘤、既往有较低级别病史的胶质母细胞瘤(GBM)成人患者。
黑色素瘤
妥拉美替尼
药物名称:妥拉美替尼(科露平®️)
研发公司:科州药物
上市时间:2024年3月15日
药物介绍:妥拉美替尼是选择性丝裂原活化蛋白激酶激酶1和2(MEK1/2)抑制剂,通过抑制MEK1/2激酶的活性发挥抗肿瘤作用。2024年3月15日,中国NMPA通过优先审评审批程序附条件批准妥拉美替尼上市,适用于抗PD-1/PD-L1治疗失败的NRAS突变的晚期黑色素瘤患者,为此类患者提供了新的希望与选择!
头颈部鳞癌
尼妥珠单抗
药物名称:尼妥珠单抗(泰欣生®)
研发公司:百泰生物药业
上市时间:2024年2月4日
药物介绍:尼妥珠单抗是一种抗表皮生长因子受体(EGFR)人源化单抗类药物,2024年2月4日,其新适应症获国家药品监督管理局(NMPA)批准,与同步放化疗联合,治疗局部晚期头颈部鳞癌。此前,尼妥珠单抗已在中国获批用于治疗鼻咽癌、胰腺癌。值得一提的是,尼妥珠单抗也是首个获批用于鼻咽癌治疗的靶向药物。
鼻咽癌
派安普利单抗注射液
药物名称:派安普利单抗注射液(AK105,安尼可®)
研发公司:正大天晴康方生物医药
上市时间:2024年4月30日
药物介绍:由康方生物自主研发,并由正大天晴康方负责后续开发的一款PD-1单抗药物——派安普利单抗注射液,于2024年4月30日,获国家药品监督管理局药品审评中心(NMPA)批准,用于治疗既往接受过二线及以上系统治疗失败的复发/转移性鼻咽癌(NPC)成人患者,这是该药在中国获批的第三项适应症。
多发性骨髓瘤
泽沃基奥仑赛
药物名称:泽沃基奥仑赛(赛恺泽®,Zevorcabtagene Autoleucel,zevor-cel,产品编号CT053)
研发公司:科济药业
上市时间:2024年3月1日
药物介绍:泽沃基奥仑赛是一款自体BCMA靶向的CAR-T细胞产品,2024年3月1日,国家药品监督管理局正式下达通知,批准科济药业研发的泽沃基奥仑赛注射液的新药上市申请(“NDA”),用于治疗复发或难治性多发性骨髓瘤。值得一提的是,泽沃基奥仑赛是国内上市的第五款CAR-T细胞产品,同时也是第二款靶向BCMA的CAR-T产品!
弥漫性大B细胞淋巴瘤
西达本胺
药物名称:西达本胺(Chidamide,爱谱沙®,Epidaza®)
研发公司:微芯生物
上市时间:2024年4月30日
药物介绍:西达本胺是微芯生物研发的一款苯酰胺类组蛋白去乙酰化酶(HDAC)亚型选择性抑制剂,在恢复耐药肿瘤细胞对药物的敏感性,以及抑制肿瘤转移、复发等方面具有潜在的作用。2024年4月30日,中国NMPA批准西达本胺联合R-CHOP方案(阿霉素、强的松、环磷酰胺、长春新碱、利妥昔单抗),用于既往未经治疗的MYC和BCL2表达阳性的弥漫大B细胞淋巴瘤(DLBCL)。值得一提的是,西达本胺是全球首个亚型选择性组蛋白去乙酰化酶(HDAC)口服抑制剂,同时也是我国首个获批上市的原创化学新药!
滤泡性淋巴瘤
泽布替尼
药物名称:泽布替尼(Zanubrutinib,BRUKINSA@,百悦泽®)
研发公司:百济神州
上市时间:2024年5月13日
药物介绍:泽布替尼是百济神州研发的一款BTK抑制剂,其补充新药申请于2024年5月13日,获得中国国家药品监督管理局(NMPA)附条件批准注册,新增以下适应症:泽布替尼联合奥妥珠单抗,适用于既往接受过至少二线系统性治疗的复发或难治性滤泡性淋巴瘤(FL)成人患者。在此之前,泽布替尼已于2023年11月,获欧盟委员会(EC)批准,用于治疗复发或难治性滤泡性淋巴瘤。并于2024年3月,获美国食品药品监督管理局(FDA)加速批准。
外周T细胞淋巴瘤
戈利昔替尼
药物名称:戈利昔替尼(golidocitinib,DZD4205)
研发公司:迪哲医药
上市时间:2024年6月19日
药物介绍:戈利多替尼是同类首创的Janus激酶1(JAK1)抑制剂,2024年6月19日,获得中国国家药品监督管理局批准,用于治疗成人复发或难治性(r/r)外周T细胞淋巴瘤(PTCL),这些患者既往在接受≥1种全身疗法后病情进展或产生耐药性。值得一提的是,戈利昔替尼是全球首个也是目前唯一一个获批用于r/r PTCL的JAK1抑制剂。
骨巨细胞瘤
地舒单抗
药物名称:地舒单抗注射液(鲁达欣®)
研发公司:齐鲁制药
上市时间:2024年4月30日
药物介绍:地舒单抗注射液(鲁达欣®)是齐鲁制药研发的一款地舒单抗生物类似药,可通过高亲和力结合RANKL,抑制破骨细胞活化,降低骨巨细胞瘤的复发。2024年4月30日,正式获得中国NMPA批准上市,用于治疗不可手术切除或手术切除可能导致严重功能障碍的骨巨细胞瘤,包括成人和骨骼发育成熟(至少1处成熟长骨且体重≥45kg)的青少年患者。
实体瘤
恩曲替尼
药物名称:恩曲替尼胶囊(Rozlytrek,Entrectinib,RXDX-101)
研发公司:罗氏制药
上市时间:2024年2月6日
药物介绍:恩曲替尼是一款具有中枢神经系统(CNS)活性的TRK/ROS1酪氨酸激酶抑制剂(TKI),能穿过血脑屏障,它也是目前临床唯一一款被证明针对原发性和转移性脑疾病均有疗效的TRK抑制剂,且无不良的脱靶活性。2024年2月6日,中国国家药品监督管理局(NMPA)批准了恩曲替尼新适应症的上市申请,用于儿童(1月龄以上)NTRK融合实体瘤的治疗。
小编温馨提示
上述信息仅供参考,具体的用药方案需遵循医嘱。小编上文提到的抗癌新药,仅为我国众多研发热点中的一小部分,还有更多的新药、创新技术纷纷在研发的路上,相信2024年将有更多的抗癌药物获批上市!“用药如用兵”,只要不放弃希望,未来办法总比困难多,相信随着越来越多的抗癌新药、新技术的不断问世,将帮助更多的癌症患者,摆脱“无药可用”的困境!对目前治疗方案不满意的患者,可致医学部,进行初步评估。此外,“方舟援助计划”也可为患者提供上市新药和未上市新药免费治疗的机会。
参考资料
[1]美国FDA官网
https://www.fda.gov/
[2]中国NMPA官网
https://www.nmpa.gov.cn/
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
里程碑!mRNA-4157联合派姆单抗让
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

刚刚!"双免王炸"纳
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2025肺癌生存新希望:六大"
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
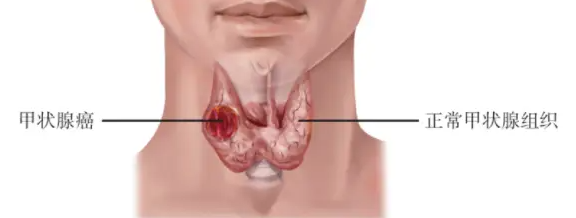
早期甲状腺癌术后五年生存率超99%,但要
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
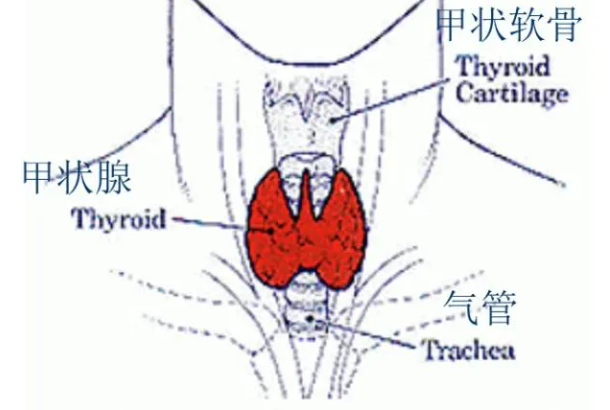
早期甲状腺癌术后五年生存率超99%!但忽
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




