最快48小时抗癌?人工智能强势介入癌症疫苗,能否颠覆肺癌、卵巢癌等实体瘤治疗格局?
人工智能强势进入癌症疫苗领域,最快48小时制备完成,能否颠覆癌症治疗的格局?
2025年1月23日,据《今日印度》(INDIA TODAY)报道,甲骨文(ORCL)董事长拉里・埃里森(LarryEllison)称:“人工智能有望通过早期癌症检测以及定制mRNA疫苗,彻底变革医疗保健领域”。埃里森表示,借助人工智能,仅需48小时就能生产出基于信使核糖核酸(mRNA)的疫苗。目前,莫德纳(Moderna)正运用其mRNA技术,与默克公司(MRK)合作开发癌症疫苗。另外,特朗普在近期的一次白宫会议上宣布,将投资5亿美元用于人工智能基础设施建设。
埃里森解释道,人体血液中会循环微小的肿瘤碎片,所以能够通过血液检测实现癌症的早期发现。人工智能可用于分析这些检测结果,从而在早期察觉癌症。一旦对癌性肿瘤进行基因测序,就能为每位患者定制个性化疫苗。凭借人工智能,mRNA疫苗可在短短48小时内由机器人完成生产,实现快速且个性化的治疗。
埃里森着重指出了人工智能在推动癌症治疗方面的巨大潜力。他设想未来,指出早期检测、个性化癌症疫苗及其快速生产能在短短两天内成为现实。这一设想体现了人工智能为未来医学带来的广阔前景。那么,癌症疫苗究竟是什么?它真的能治疗癌症吗?埃里森提出的“48小时内设计癌症疫苗”又是否可行呢?接下来,小编将简单介绍癌症疫苗,为大家揭开其神秘面纱。
▲截图源自“INDIA TODAY”
癌症疫苗的"前世今生"
癌症疫苗是一种新型治疗手段,它的作用机制是激活并训练患者的免疫系统,使其能够精准识别并攻击癌细胞,终极目标在于预防肿瘤的生长、复发以及转移。
人类最早尝试利用免疫系统对抗癌症,是在 1891 年,由美国著名外科医生威廉・科利(William Coley)付诸实践。他将活细菌和热灭活细菌注射到患有骨和软组织肉瘤的患者体内,结果观察到部分患者的肿瘤有所缩小。八十多年后,卡介苗(BCG)——一种原本用于预防结核病的疫苗,被应用于非肌层浸润性膀胱癌的治疗,通过膀胱内给药的方式,能够激活局部免疫反应,抑制肿瘤细胞的存活和增殖,临床疗效显著。BCG疗法不仅成为首个获得现代医学认可的癌症免疫疗法,直至今日,依然是膀胱癌治疗的标准疗法之一。
癌症疫苗大盘点:究竟包含哪些常见类型
目前,在临床实践中常见的癌症治疗疫苗,主要分为以下几类:
树突状细胞(DC)疫苗
树突状细胞(DC)是一类多功能抗原提呈细胞,广泛分布于皮肤真皮层、淋巴结等处,在启动机体免疫应答、维持免疫耐受方面发挥着重要作用。而树突状细胞(DC)疫苗作为一种新兴的癌症免疫治疗方案,有望突破免疫检查点抑制剂(ICB)、过继细胞转移疗法(ACT)所面临的局限。
树突状细胞(DC)疫苗的主要治疗流程如下:首先,从血液样本中提取未成熟的DC或单核细胞,提取出的细胞通常会在体外加载肿瘤裂解物、肿瘤相关抗原(TAA)或新抗原;随后,将已成熟的DC注射回同一患者体内,以此激发肿瘤特异性效应T细胞反应(详见下图)。
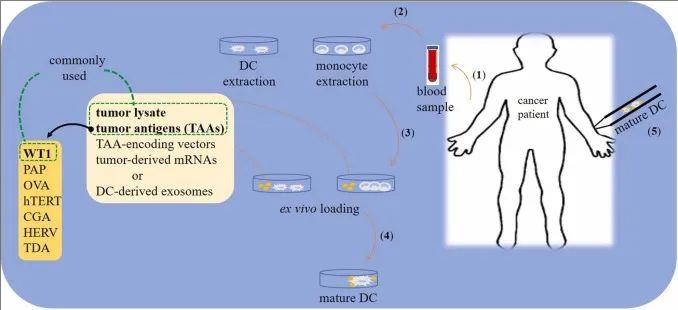
▲图源“ScienceDirect”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
根据《生物医药与药物治疗》的最新研究成果,DC疫苗的临床客观缓解率(ORR)与其他常规抗癌疗法大致相当。例如,接受DC免疫治疗的黑色素瘤患者,其ORR为8.5%,与接受一线药物达卡巴嗪治疗的患者ORR相近。同样,接受DC免疫治疗的前列腺癌、恶性胶质瘤和肾细胞癌患者,其ORR分别为7.1%、15.6%和11.5%,与接受常规化疗的患者ORR相似。
mRNA癌症疫苗
“mRNA癌症疫苗”,全称“信使核糖核酸癌症疫苗”,其作用机制是通过编码表达肿瘤特异性抗原(如肿瘤特异性抗原TSA、肿瘤相关抗原TAA),引导细胞合成特定蛋白质,进而激活人体免疫系统,使其能够有效对抗体内的癌细胞。目前,这款疫苗主要应用于非小细胞肺癌(NSCLC)、结直肠癌(CRC)、黑色素瘤等多种实体瘤的治疗。与传统疫苗平台相比,mRNA疫苗具有显著优势,如制造成本低廉、给药安全性高、效力强劲,以及发展潜力巨大等。
mRNA疫苗的工作原理基于引入编码病毒蛋白或新抗原的单链分子。在完成注射后,mRNA癌症疫苗会被输送至抗原呈递细胞(如树突状细胞DC)的细胞质内,在该环境中,这些疫苗会被翻译为新抗原蛋白。理想状态下的mRNA疫苗应包含多种新抗原,涵盖已验证的新抗原、预测的新抗原以及驱动基因突变,多种成分共同作用,降低肿瘤细胞逃逸免疫系统监测的可能性。经由纳米颗粒递送后,mRNA疫苗会通过与TLR-7或TLR-8相互作用,主动锁定并激活抗原呈递细胞(例如树突状细胞)。紧接着,成熟的树突状细胞迁移至淋巴结,从而启动强大的B细胞和T细胞免疫反应,对癌细胞展开针对性攻击。
▼mRNA 癌症疫苗作用机制示意图
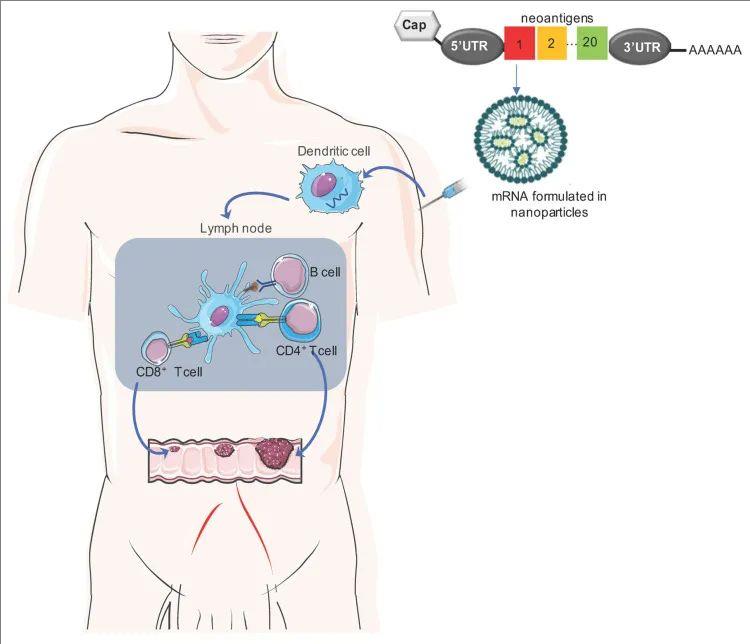
▲图源“Vaccines (basel)”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
DNA癌症疫苗
基于DNA的癌症疫苗传递含有编码肿瘤抗原的遗传物质的质粒,依靠内源性细胞吸收构建体并表达编码的抗原。DNA癌症疫苗对佐剂的依赖程度,略低于基于肽类癌症疫苗;而且不同于mRNA疫苗,DNA疫苗必须进入细胞核,才能启动转录。
其他癌症疫苗
1、肽类癌症疫苗:此类疫苗由特定的肿瘤抗原表位化学或生物合成成分组成,可引发针对特定肿瘤抗原位点的强烈免疫反应,与DC疫苗相比,肽类癌症疫苗的设计、制造和给药更简单,成本也更低,主要用于肝癌、宫颈癌的治疗。为向抗原提呈细胞(APC)提供相关抗原,在肽类癌症疫苗接种方案中,编码肿瘤抗原的肽通常被注射到皮下空间或真皮中。
2、病毒载体类疫苗:病毒载体类疫苗同样旨在将遗传物质,递送到内源细胞中以实现抗原表达,可引发T细胞和B细胞的强烈免疫反应。比如工程化的溶瘤病毒可作为载体,呈递大量的肿瘤抗原,从而产生长期记忆,但生产起来也较复杂。
“我们知道,即使手术成功,癌症有时也会复发。这可能与体内仍残留少量癌细胞有关,但使用针对这些残留癌细胞的癌症疫苗,或许可以阻止这种情况的发生”。
——NHS国家癌症临床主任、教授
彼得·约翰逊(Peter Johnson)
聚焦这几款癌症疫苗,解锁卵巢癌、肺癌等实体瘤治疗新纪元
DC疫苗联合NK细胞疗法,晚期卵巢癌患者癌胚抗原下降、腹水减少、原发灶及转移灶缩小
2024年3月,全球著名开放期刊《Cureus》报道了一个“联合应用WT1-DC疫苗+NK细胞疗法+化疗,让IV期卵巢癌显著缩小”的重磅案例,一时间引爆了抗癌圈!WT1是常见的癌症抗原之一,其临床实用性已得到美国国家癌症研究所研究的高度评价,根据2009年美国国家癌症研究所的一份报告,WT1在75种常见癌症抗原中,在免疫原性、治疗效果、癌症特异性和表达等九个类别的总体评分中排名第一。

▲截图源自“PMC”
这位患者在产后半年,突然出现腹水而就诊,后确诊为IV期双侧卵巢癌,且伴全身多处转移,PET-CT检查发现,存在腹膜播散,肝多发转移、肺转移、骨转移。腹部CT扫描显示大量腹水。患者按常规治疗方案,仅接受化疗(紫杉醇+卡铂AUC5),未进行手术和放疗。但医生判断预后不佳,因此,开始进行WT1树突状细胞疫苗疗法(WT1-DC)、化疗[纳武单抗(Nivolumab)]联合治疗,并同时进行多轮NK细胞疗法。结果显示:
WT1-DC疫苗首次给药当晚,该患者出现发热,体温39.4℃,接种该疫苗后,引起的发热是预后良好的标志,这种反应很可能在所谓的“热肿瘤”中引起。给药后3天免疫反应良好,DTH最大值为35mm,癌胚抗原(CEA)下降,但CA125反而升高,这表明肿瘤的性质随着治疗而发生了变化。
由于WT1-DC疫苗治疗后,血液检测中NK活性较低,因此增加了活化NK细胞治疗。每次注射NK细胞时,发热均高于40℃,这表明注射的NK细胞在体内产生了免疫反应。在第3次NK细胞治疗后,CEA、CA125明显下降;第4和5次NK细胞治疗后,CEA、CA125持续下降。更为惊喜的是,在NK细胞治疗第56天后,腹部CT显示,腹水较确诊时明显减少,这表明NK细胞治疗显著减少了腹膜播散(详见下图)。
▼NK细胞治疗前后腹部CT对比
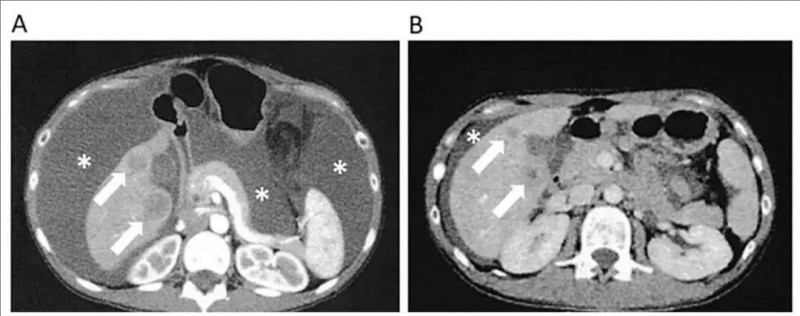
▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:
①图A:确诊时,腹部CT可见大量腹水(*),白色箭头表示肝转移。
②图B:确诊并应用NK细胞治疗第56天,腹部CT示腹水明显减少,肝转移灶也缩小。
此外,该患者治疗前PET-CT显示,存在原发性卵巢癌病灶,以及肝脏、腹膜、肺等多处转移灶(详见下图A)。而在WT1-DC疫苗+NK细胞治疗第142天复查PET-CT显示,该患者原发性肿瘤明显缩小,肺转移灶及腹膜播散灶消失,肝转移灶缩小(详见下图B)。
▼治疗前和治疗142天,PET-CT对比
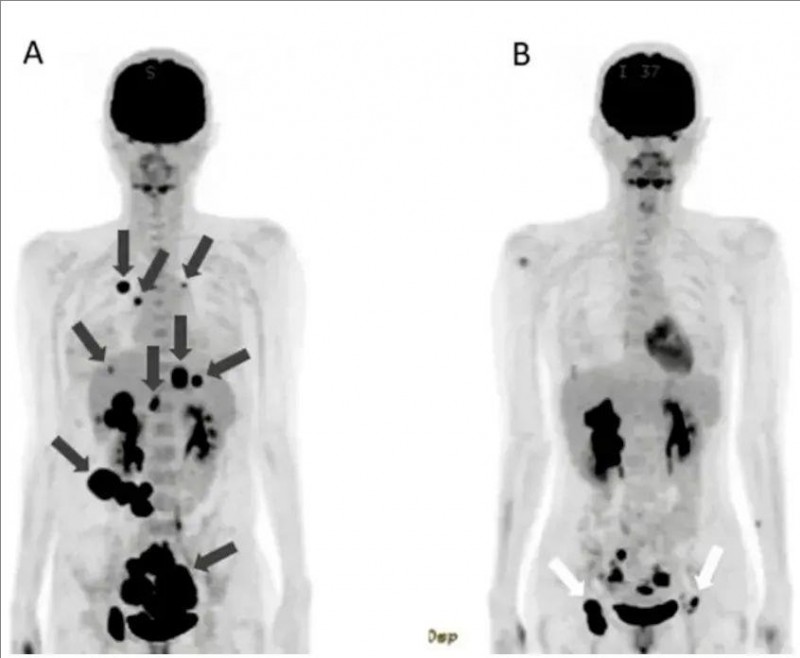
▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:
①图A:黑色箭头代表,原发性及转移灶。
②图B:白色箭头代表,腹股沟区接种树突状细胞疫苗后出现的炎症反应。
综上,WT1-DC疫苗疗法、NK细胞疗法、纳武单抗的联合应用,成功治疗了伴全身多处转移的IV期卵巢癌患者,该患者腹水消失,全身多处癌细胞明显减少。此外,除了免疫细胞给药引起的反应性发热外,未见其他副作用。
中国患者如何寻求癌症疫苗帮助?
目前,癌症疫苗中临床疗效及预防复发效果较突出的是树突状细胞疫苗、个性化新抗原疫苗等,其中,树突状疫苗在日本、德国等,用于临床辅助治疗多种癌症,包括皮肤癌、肝癌、肺癌、肾癌、乳腺癌等,是癌症患者的新希望!值得欣慰的是,如今我国也有多款癌症疫苗正在开展临床研究,这也意味着中国患者也有机会寻求这款抗癌新技术的帮助!
想寻求国内外癌症疫苗或其他治疗新技术帮助的患者,可先将治疗经历、病理报告、出院小结等资料,提交到医学部,详细评估病情。
WT1-DC助终末期肺癌患者,无进展生存期超577天
著名医学杂志《Cureus》发布了一个“应用WT1-DC联合二线化疗治疗终末期肺癌全身转移,并保持长期显著缓解”的经典案例。该患者为一位69岁患右肺中叶IV期鳞状细胞癌的男性,同时伴多发性肝转移、双侧肾上腺转移、多发性骨转移,此时患者的状态已无法耐受手术和放疗。故入组接受WT1-DC(WT1树突状细胞疫苗,共注射8剂)+(紫杉醇+卡铂AUC6)化疗联合治疗。结果显示如下:
▲截图源自“Cureus”
1、癌胚抗原显著下降:该患者诊断时癌胚抗原(CEA)高达66.4,WT1-DC疫苗治疗第121天骤降至3.0。此外,C反应蛋白(CRP)、N/L比(中性粒细胞对淋巴细胞比率)均降低,在治疗第254~577天,患者N/L比值始终保持在低水平,平均为3.27。CEA虽有升高趋势,但在联合多西他赛+雷莫芦单抗治疗后,CEA值降低至5.9。截至数据统计时,该患者无进展生存期(PFS)已超577天,且临床状况良好,体能状态为1。
2、肺癌病灶显著缩小:与治疗开始时(第0天)的胸部CT相比,WT1-DC疫苗治疗第114天胸部CT显示,该患者肺部肿瘤明显缩小(详见下图)。
▼WT1-DC疫苗治疗前后胸部CT图像对比
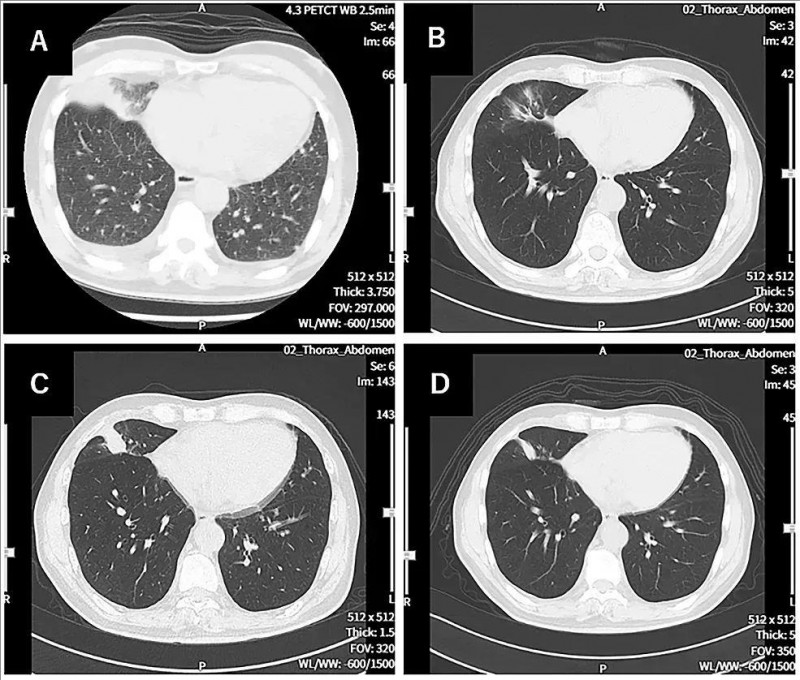
▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:
①图A(诊断时的CT图像):示原发性右下肺癌,伴左右胸腔积液。
②图B(治疗第114天的CT图像):示原发病灶几乎消失。
③图C(治疗第213天的CT图像):示原发病变存在一定程度的复发。
④图D(治疗第338天的CT图像):示原发性、复发性病变缩小。
3、全身转移灶改善:该患者诊断时全身PET-CT显示,除右下肺原发肿瘤外,还存在双侧多发肺内转移、多发肝转移、双侧肾上腺转移和多发骨转移。而在接受WT1-DC+化疗联合治疗后第479天的PET-CT,除右肺直径1.0cm的转移灶、肝脏直径1.7cm的转移灶外,并未见其他异常表现(详见图1)。
▼WT1-DC疫苗治疗前后全身PET-CT对比
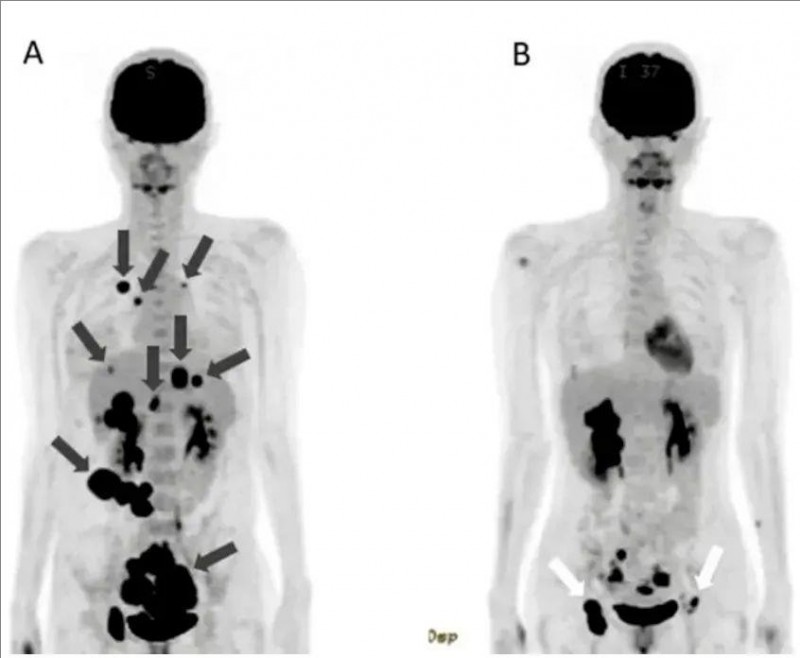
▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:
①图A(诊断时的全身PET-CT):示右下肺原发肿瘤,伴多发性双侧肺内转移、多发性肝转移、双侧肾上腺转移、多发性骨转移。
②图B(治疗第479天的全身PET-CT):示右肺有2个小转移灶(直径约1.0cm),肝脏有1个小转移灶(直径约1.7cm)。
新抗原mRNA——cevumeran疫苗助实体瘤显著缩小,有患者实现完全缓解并存活超3年
自基因cevumeran(BNT122、RO7198457)是一款可编码20余种特异性新抗原的个体化新抗原mRNA疫苗,该疗法根据从每位患者肿瘤组织中获得的肿瘤特异性体细胞突变数据设计,以刺激针对多达 20种新抗原的T细胞反应,以降低肿瘤复发风险、延长患者的生存时间。
近期全球权威期刊《Nature Medicine》发表了“自基因cevumeran疫苗对接受过治疗的晚期实体瘤的1期GO39733临床研究(NCT03289962)”的惊艳数据。本次共入组213例局部晚期、转移性或复发性无法治愈的恶性实体瘤患者(包括肾癌、乳腺癌、黑色素瘤、肾细胞癌、尿路上皮癌、非小细胞肺癌、直肠癌),且在接受至少一种可用的标准疗法后病情进展。入组接受自基因cevumeran疫苗作为单一疗法(n = 30)、与阿替利珠单抗(n = 183)联合治疗。其中,自体基因 cevumeran 的剂量采用标准 3 + 3 设计递增,1a 期从 25 μg 递增至 100 μg,1b 期从 25 μg 递增至 50 μg。

▲截图源自“nature”
结果显示:检查点抑制剂(CPI)初治的黑色素瘤 (n= 9) 、肾细胞癌 (RCC,n= 12)、尿路上皮癌 (UC; n = 11)、非小细胞肺癌(NSCLC,n= 10)扩展队列的客观缓解率(ORR)分别为33.3%、33.3%、18.2%、10.0%。此外,在剂量递增队列中,个别患者表现出持久的临床益处:50 µg 自体基因 cevumeran 单药治疗队列中最佳总体反应(BOR) 为完全缓解 (CR;胃癌),38 µg 组合队列中为部分缓解(PR) 和完全缓解 (CR;乳腺癌和直肠癌)(详见下图)。
▼自基因cevumeran单药治疗对靶病变的影响
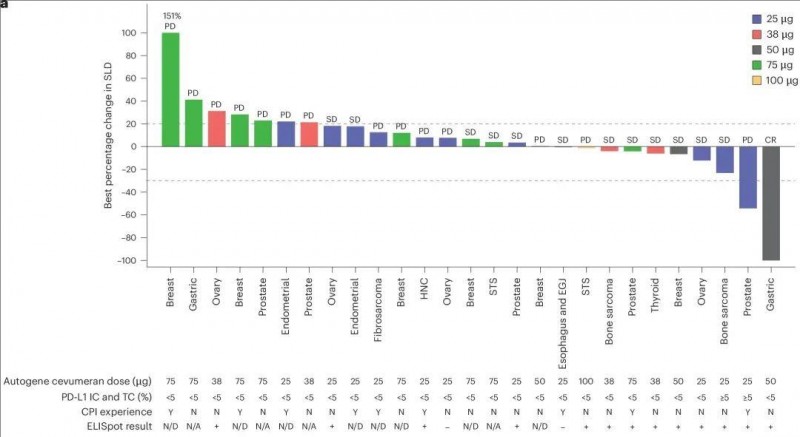
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
▼自基因cevumeran与阿替利珠单抗联合治疗对靶病变的影响
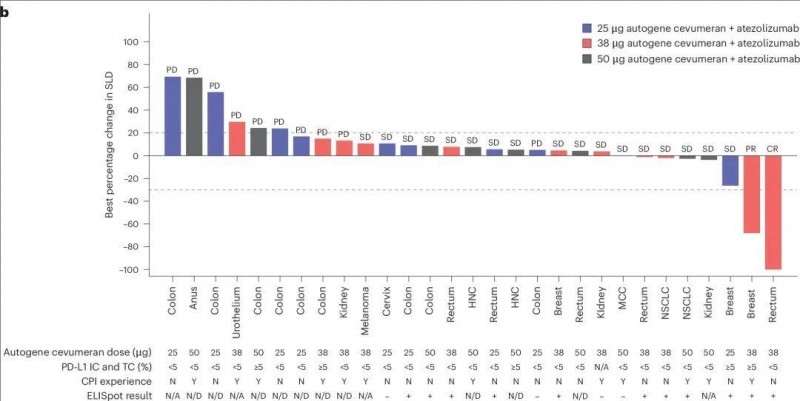
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
案例分析
值得一提的是,其中一例存在PD-L1突变的三阴性乳腺癌(TNBC)患者(患者13),既往经纳武单抗治疗后病情进展。入组接受阿替利珠单抗联合治疗后,该患者达到部分缓解(PR),包括肺转移瘤大小减少,反应持续时间为 9.9 个月(详见下图)。
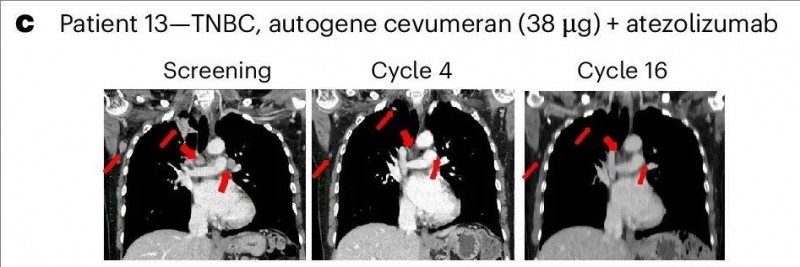
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
另一例患者(21号患者)存在微卫星稳定、PD-L1 低的直肠癌,在接受两线治疗后,肺部存在1.1 cm的靶病灶和非靶病灶。该患者在接受9剂38µg的阿替利珠单抗联合治疗后,奇迹般获得完全缓解(CR),且缓解缓解持续时间达8.2个月。更为惊喜的是,截至临床数据统计时止,该患者已存活超过3年(40.7个月)(详见下图)。
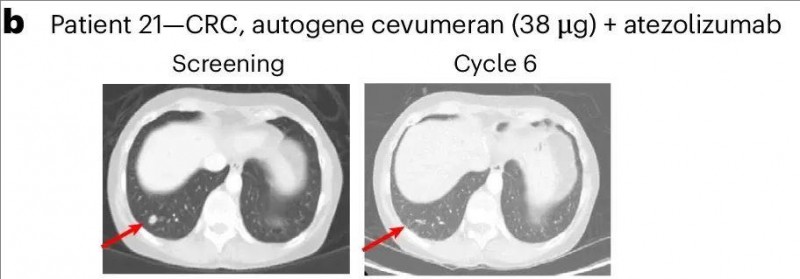
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
还有一例肾癌患者(患者38),在入组前接受了包括纳武单抗在内的4种全身治疗,最初在研究期间病情进展,但随后达到部分缓解(PR)。该患者胸膜靶病变的最长直径总和(基线肿瘤)(SLD)为108mm,在13个月后,缩小到10mm(详见下图),肿瘤显著缩小近10倍。
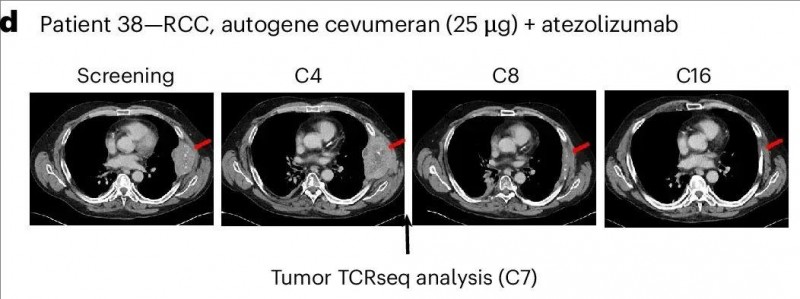
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
我国多款在研癌症疫苗蓄势待发,国内多个中心启动招募
除了上面提到的几款在取得突破性进展的DC疫苗、mRNA疫苗外,我国还有多款在研的疫苗正在蓄势待发,并在国内多家癌症中心启动临床,众多晚期患者已成功入组接受治疗!
1、KSD-101:恒赛生物
KSD-101是恒赛生物自主研发的一款负载EB病毒相关类肿瘤复合抗原的人单核细胞来源自体DC疫苗,2024年3月,该疫苗的新药临床试验(IND)申请获得美国食品药品监督管理局(FDA)批准,KSD-101也成为了我国首个获得美国FDA IND批件的自研DC疫苗产品!
2、MASCT-I:恒瑞源正
MASCT-I是由恒瑞源正自主研发的一款1类细胞治疗产品,其活性成份包括负载多种肿瘤相关抗原的成熟自体树突状细胞(DC细胞)、DC细胞活化扩增的自体效应T淋巴细胞(T细胞)。
在2024年美国临床肿瘤学会(ASCO)年会上,公布了“MASCT-I治疗转移性尿路上皮癌的1期临床研究(NCT03034304)数据”,其2期临床研究已获得国家药品监督管理局药品审评中心(CDE)批准!
3、靶向Survivin DC细胞注射液:启辰生生物
靶向Survivin DC细胞注射液是启辰生生物研发的一款针对原发性脑胶质母细胞瘤的抗原mRNA负载的树突状细胞(DC)产品,同时也是世界首款靶向Survivin的针对脑胶质母细胞瘤的mRNA-DC肿瘤疫苗!其治疗目的在于帮助患者清除术后残留的癌细胞、预防肿瘤的复发及转移、延长患者的生存期。前期临床探索性研究数据显示,1例患者在治疗后,总生存期已超5年!
4、CUD002:康德赛医疗
CUD002是康德赛医疗自主研发的一款针对卵巢癌的个体化mRNA编辑的DC肿瘤疫苗,根据患者独特的突变信息定制设计并制造而成,值得一提的是,它是我国首款用于卵巢癌治疗的新生抗原的mRNA编辑DC肿瘤疫苗!其临床试验默示许可已于2023年9月,获得国家药品监督管理局药品审评中心(CDE)批准,拟用于难治性/耐药复发性卵巢癌的治疗。
5、ZSNeo-DC1.1:中生康元
ZSNeo-DC1.1注射液是中生康元自研的一款新型个性化树突状细胞疫苗,其临床试验默示许可已获得国家药品监督管理局药品审评中心(CDE)批准,用于泛癌种恶性实体肿瘤的治疗。值得一提的是,它是我国首个进入注册临床研究阶段的负载多个肿瘤新生抗原肽的治疗性肿瘤DC细胞产品!
6、CAR-DC癌症疫苗:翊博生物
CAR-DC癌症疫苗是一款利用工程化树突状细胞扩增技术(CelArts-DC),对外周血中的原代DC亚群进行选择性扩增,从而成功攻克了以往在 DC 细胞应用过程中所面临的DC细胞来源少、对免疫系统要求较高等诸多应用难点问题。
小编寄语
癌症治疗正处于一场变革的风口浪尖,各国都希望在抗癌领域取得突破性进展,作为癌症治疗领域新兴力量的癌症疫苗,历经数十载的发展,更是展现出了巨大的潜力和前景。小编上文中已的癌症疫苗,大部分目前都处于早期的临床试验阶段,一些国家的树突细胞疫苗已经正式进入临床应用,早期肿瘤患者可以在手术后考虑使用疫苗联合放化疗辅助治疗,起到杀伤残余癌细胞,产生免疫记忆,预防癌症复发和转移。
但需要提醒大家的是,癌症作为一种高度突变的复杂疾病,很难仅靠单一治疗手段,达到理想的治疗效果。目前比较理想的治疗手段是在权威医院(手术、放化疗等)传统治疗的基础上,结合患者病情、个体情况,突变靶点、经济状况等,辅助靶向药、免疫细胞治疗(如CAR-T、TCR-T、TIL细胞疗法、癌症疫苗)、质子治疗、电场疗法等新型治疗手段,以达到巩固传统治疗效果、降低肿瘤复发风险、提高患者生存质量、延长生存期等目的。想寻求癌症疫苗等新型抗癌疗法帮助的患者,可将治疗经历、近期病理及影像学检查结果等,提交至全球肿瘤医生网医学部,进行初步评估或申请国内外抗癌专家会诊。
参考资料
[1]Najafi S,et al.Advances in dendritic cell vaccination therapy of cancer[J]. Biomedicine & Pharmacotherapy, 2023, 164: 114954.
https://www.sciencedirect.com/science/article/pii/S0753332223007448
[2]Ni L. Advances in mRNA-based Cancer Vaccines. Vaccines (basel). 2023 Oct 16;11(10):1599.
https://pmc.ncbi.nlm.nih.gov/articles/PMC10611059/
[3]Nagai H,et al.Late-Stage Ovarian Cancer With Systemic Multiple linkstases Shows Marked Shrinkage Using a Combination of Wilms' Tumor Antigen 1 (WT1) Dendritic Cell Vaccine, Natural Killer (NK) Cell Therapy, and Nivolumab. Cureus. 2024 Mar 22;16(3):e56685.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10960621/
[4]Nagai H,et al.WT1 Dendritic Cell Vaccine Therapy Improves Immune Profile and Prolongs Progression-Free Survival in End-Stage Lung Cancer[J].Cureus,2023,15(10).
https://www.cureus.com/articles/193305-wt1-dendritic-cell-vaccine-therapy-improves-immune-profile-and-prolongs-progression-free-survival-in-end-stage-lung-cancer#!/
[5]Lopez J,et al.Autogene cevumeran with or without atezolizumab in advanced solid tumors: a phase 1 trial[J]. Nature Medicine, 2025: 1-13.
https://www.nature.com/articles/s41591-024-03334-7
[6]https://www.indiatoday.in/health/story/ai-can-develop-personalised-cancer-vaccine-in-48-hours-oracles-larry-ellison-2668919-2025-01-23
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

【骨髓瘤药物】新一代靶向药BGB-114
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

肺癌患者速收藏!揭秘肺癌免疫治疗十大医院
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【CAR-T细胞疗法免费招募】伊基奥仑赛
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【骨髓瘤药物】新一代靶向药LBL-034
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
收藏|乳腺癌患者《2025抗癌宝典》出炉
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

收藏|宫颈癌患者《2025抗癌宝典》出炉
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




