抗癌突破口:新型DC-T细胞疗法诞生,DC疫苗重锤肺癌、胃癌、脑瘤等!PFS超577天
新型DCT细胞免疫疗法诞生,DC疫苗治疗肺癌、胃癌、脑瘤等实体瘤无进展生存期超577天
树突状细胞(dendritic cell,DC)为一类多功能抗原提呈细胞,在启动机体的免疫应答、维持免疫耐受等方面发挥重要作用;同时还能将抗原信息传递给T细胞,从而激活T细胞发挥抗肿瘤效应。但在这一过程中,T细胞容易耗竭,从而失去杀伤力。研究人员不断尝试新方法,希望能攻破T细胞易耗竭的难题,从而提高抗肿瘤效应。
值得欣慰的是,2024年1月18日,世界权威期刊《Cell(细胞)》上发表了以色列研究人员开发出的一种能同时靶向DC和T细胞的全新免疫治疗方法——DC-T细胞疗法,不仅能提高治疗效果,还可防止肿瘤转移和复发,是癌症免疫治疗起效的关键“突破口”,为肿瘤的治疗提供了新的方向!
DC-T细胞疗法:有效增强抗肿瘤免疫,预防复发和转移
双特异性T细胞衔接器(bispecific T-cell engager,BiTE)是一种能同时结合CD3复合物(CD3ε)和肿瘤相关抗原(TAA)的抗体类抗肿瘤药物,可以将肿瘤组织中的T细胞重定向到癌细胞,用于治疗急性B细胞淋巴细胞白血病等。
该研究构建了一种靶向免疫检验点PD-L1 和CD3ε的双特异性抗体 (PD-L1xCD3),能将DC与T细胞衔接在一起,阻断PD-L1/PD-1通路,并拉近T细胞与肿瘤细胞的距离,最终实现T细胞的持续性激活,增强其杀伤效果,并获得持久的抗肿瘤免疫反应。
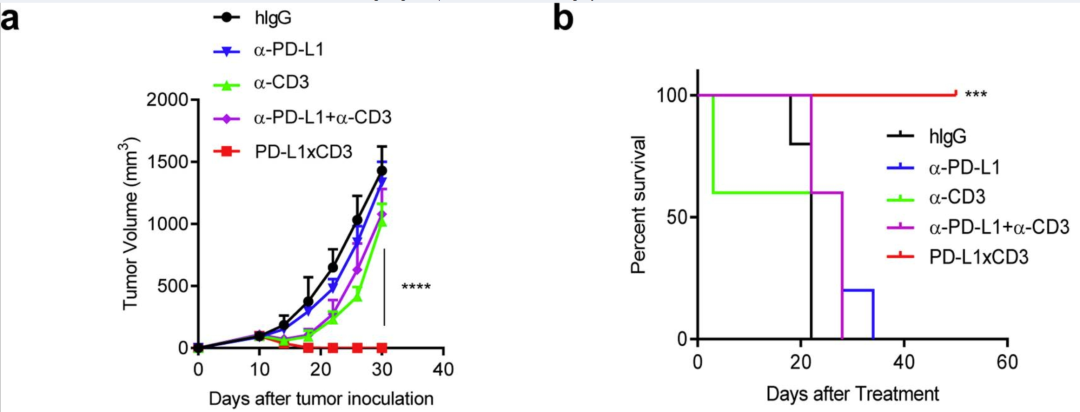
图1 临床前研究显示,PD-L1xCD3可产生比联合治疗更优异的抗肿瘤效果
▲图源“PMC”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:实验模型接受皮下接种MC38肿瘤细胞,并用抗CD3、抗PD-L1、抗CD3+抗PD-L1或PD-L1xCD3处理两次,治疗后第10天和第15天,肿瘤体积(a)和存活百分比(b)。
WT1-DC为终末期肺癌患者带来救赎,无进展生存期超577天
WT1是一种常见的癌症抗原,在多种肿瘤中广泛表达,既可用于治疗血液肿瘤,也可用于治疗肺癌、胃癌、肝癌、乳腺癌等多款实体瘤。研究显示,WT1在鳞状细胞肺癌中的表达率超过90%。美国国家癌症研究所报道,WT1在癌症中的表达比例、免疫原性和临床疗效方面是较为理想的。因此,WT1在日本临床上常用作树突状细胞疫苗治疗的通用抗原,WT1-DC既可缩小肿瘤体积,还能降低肿瘤标志物并延长总生存期。
著名医学杂志《Cureus》发表了一篇“采用WT1-DC联合二线化疗治疗终末期肺癌全身转移,并保持长期显著缓解的病例”。该患者为69岁男性,患右肺中叶IV期鳞状细胞癌,同时伴多发性肝及骨转移、双侧肾上腺转移,此时该患者已无法耐受手术和放疗。故给予WT1-DC(WT1树突状细胞疫苗)联合(紫杉醇+卡铂AUC6)化疗。WT1树突状细胞疫苗治疗从第155天开始,直到第280天共注射8剂。结果显示如下:
1、血液学检查:在接受WT1-DC输注后,白细胞总数减少,中性粒细胞百分比有所降低,淋巴细胞百分比增加,在治疗第254~577天,淋巴细胞百分比保持相对有利,平均为21.0%。
2、癌胚抗原:诊断时癌胚抗原(CEA)高达66.4,治疗第121天降至3.0。C反应蛋白(CRP)降低,N/L比(中性粒细胞对淋巴细胞比率)降低,在治疗第254~577天,患者N/L比值始终保持在低水平,平均为3.27。CEA有升高趋势。不过在联合应用多西他赛+雷莫芦单抗后,CEA值降低至5.9。
3、全身PET-CT:诊断时PET-CT显示该患者除右下肺原发肿瘤外,还显示双侧多发肺内转移、多发肝转移、双侧肾上腺转移和多发骨转移。在接受WT1-DC联合化疗后第479天,全身PET-CT显示,除右肺直径为1.0cm的转移灶、肝脏直径为1.7cm的转移灶外,并未见其他异常表现(详见图1)。
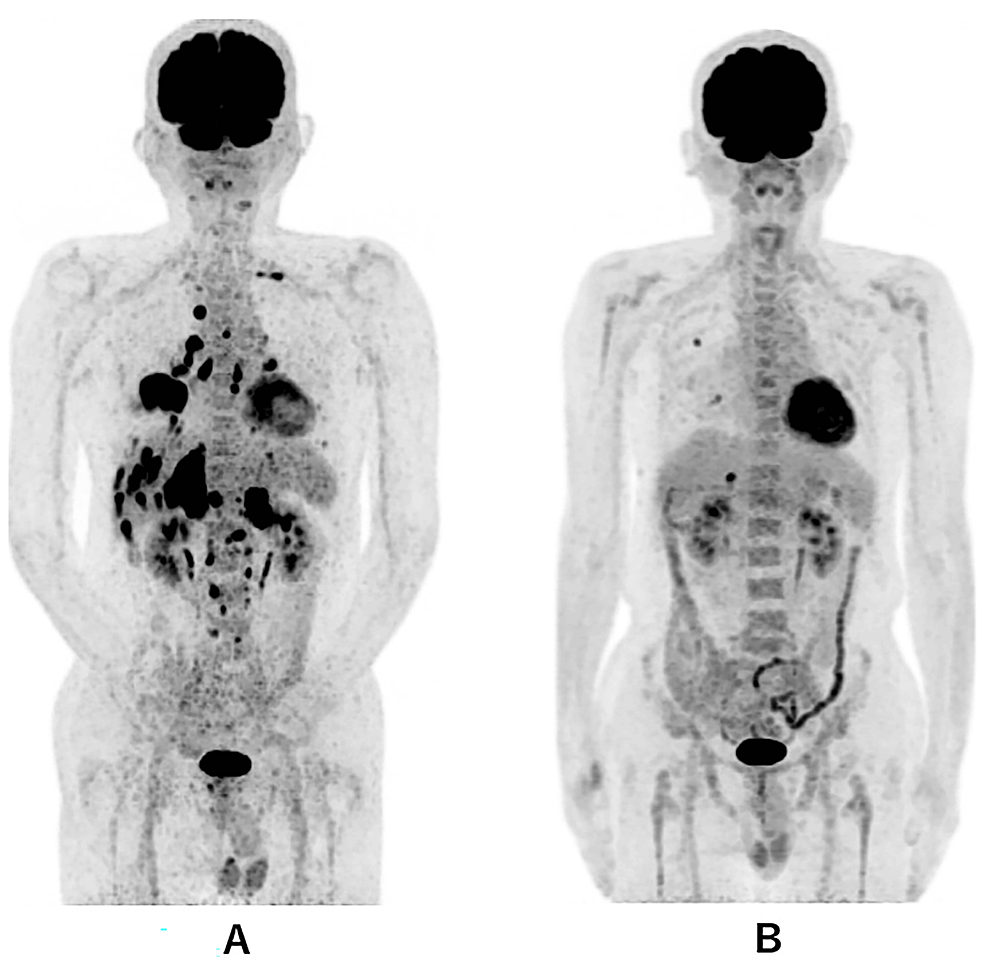
图1 全身PET-CT对比
▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
图1A(诊断时的全身PET-CT):示右下肺原发肿瘤,伴多发性双侧肺内转移、多发性肝转移、双侧肾上腺转移、多发性骨转移。
图1B(治疗第479天的全身PET-CT):示右肺有2个小转移灶(直径约1.0cm),肝脏有1个小转移灶(直径约1.7cm)。
4、胸部CT显示:与治疗开始时(第0天)的胸部CT相比,第114天的胸部CT观察到肿瘤明显缩小(详见图2)。
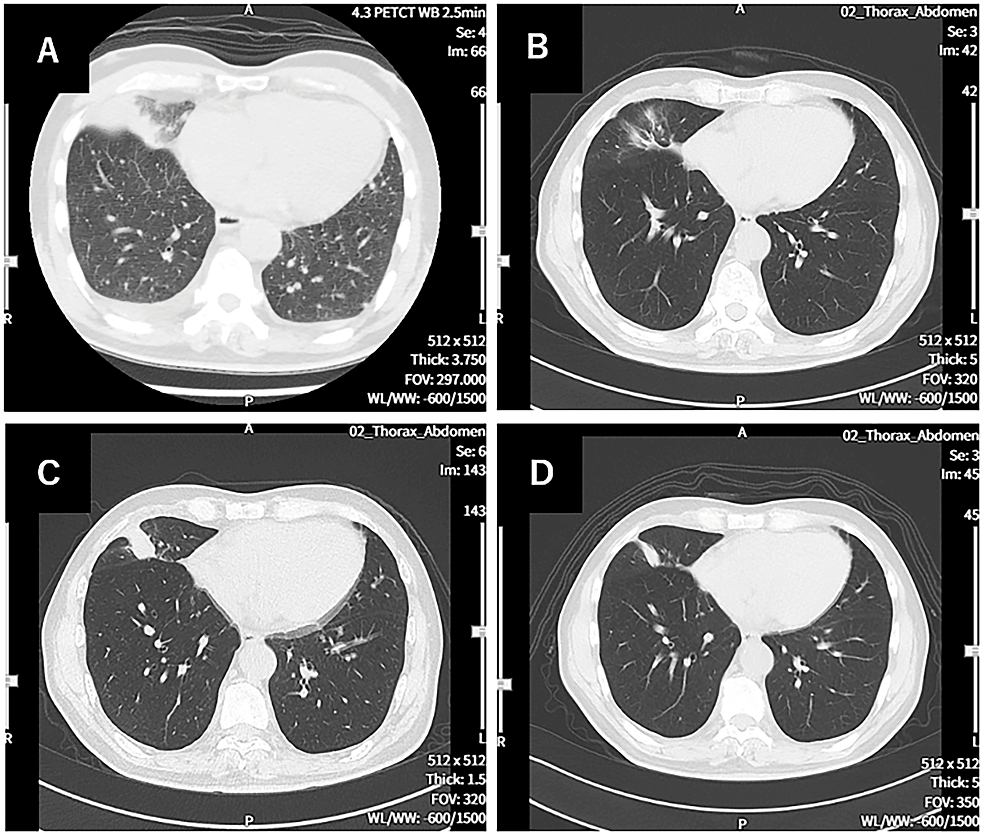
图2 胸部CT图像对比
▲图源“Cureus”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
图片A(诊断时的CT图像):示原发性右下肺癌,伴左右胸腔积液。
图片B(治疗第114天的CT图像):示原发病灶几乎消失。
图片C(治疗第213天的CT图像):示原发病变存在一定程度的复发。
图片D(治疗第338天的CT图像):示原发性、复发性病变缩小。
5、其他:截至数据统计时,该患者无进展生存期(PFS)已超577天,而且临床状况良好,体能状态为1。
综上,虽然IV期肺鳞癌预后较差,五年生存率低于5%。但幸运的是,本例接受WT1-DC联合化疗治疗的患者,其免疫状况持续改善,同时癌症显著缩小,癌症未复发或恶化,患者能够正常生活。这些发现表明WT1-DC改善了患者的免疫状况,有助于长期维持化疗效果。
晚期胃癌全身肿瘤消退!首例接受Neo-MoDC疫苗患者获持久缓解!
国际重磅期刊《Nature》子刊上,报道了一名66岁晚期转移性胃癌(IV期,Bormann III型)患者,在接受Neo-MoDC疫苗联合免疫检查点抑制剂(ICI)治疗25个月后,肿瘤体积迅速减小,全身癌症病灶完全消退的案例,引起了巨大的轰动!
Neo-MoDC(载有新抗原的单核细胞衍生的树突状细胞疫苗)是由中国研发的一款全新的个性化癌症疫苗,可充分调动机体免疫系统,促进T细胞富集,调动T细胞去清除癌细胞,最终对全身癌细胞进行一系列精密而强大的攻击。
该患者于2017年7月被诊断为胃癌,随后接受D2根治性远端胃切除术、FOLFOX治疗,但依然没有阻止病情进展,患者腹膜和淋巴结中出现转移,而且患者已无法忍受化疗。在万念俱灰下,参加了Neo-MoDC临床试验(NCT03185429)。入组后,患者先接受了淋巴细胞清除,随后接受了Neo-MoDC联合免疫检查点抑制剂(ICI)治疗。结果显示:
1、肿瘤标志物CA125(胃癌进展的生物标志物):第一轮纳武单抗治疗后5天,血清CA-125水平从596U/ml,迅速下降至64U/ml。两周后,患者恶性腹水消失。
2、影像学检查:初次接种疫苗后第231天,PET扫描显示病变近乎完全消退(详见图3)。联合治疗第389天的CT扫描显示,卵巢种植转移也完全消失(详见图4)。重新分期CT显示完全消退仍持续25个月(截至2021年10月)。这是首例通过基于新抗原的DC疫苗和ICI疗法,实现胃肿瘤完全且持久消退的研究,在DC疫苗治疗领域具有划时代的意义!
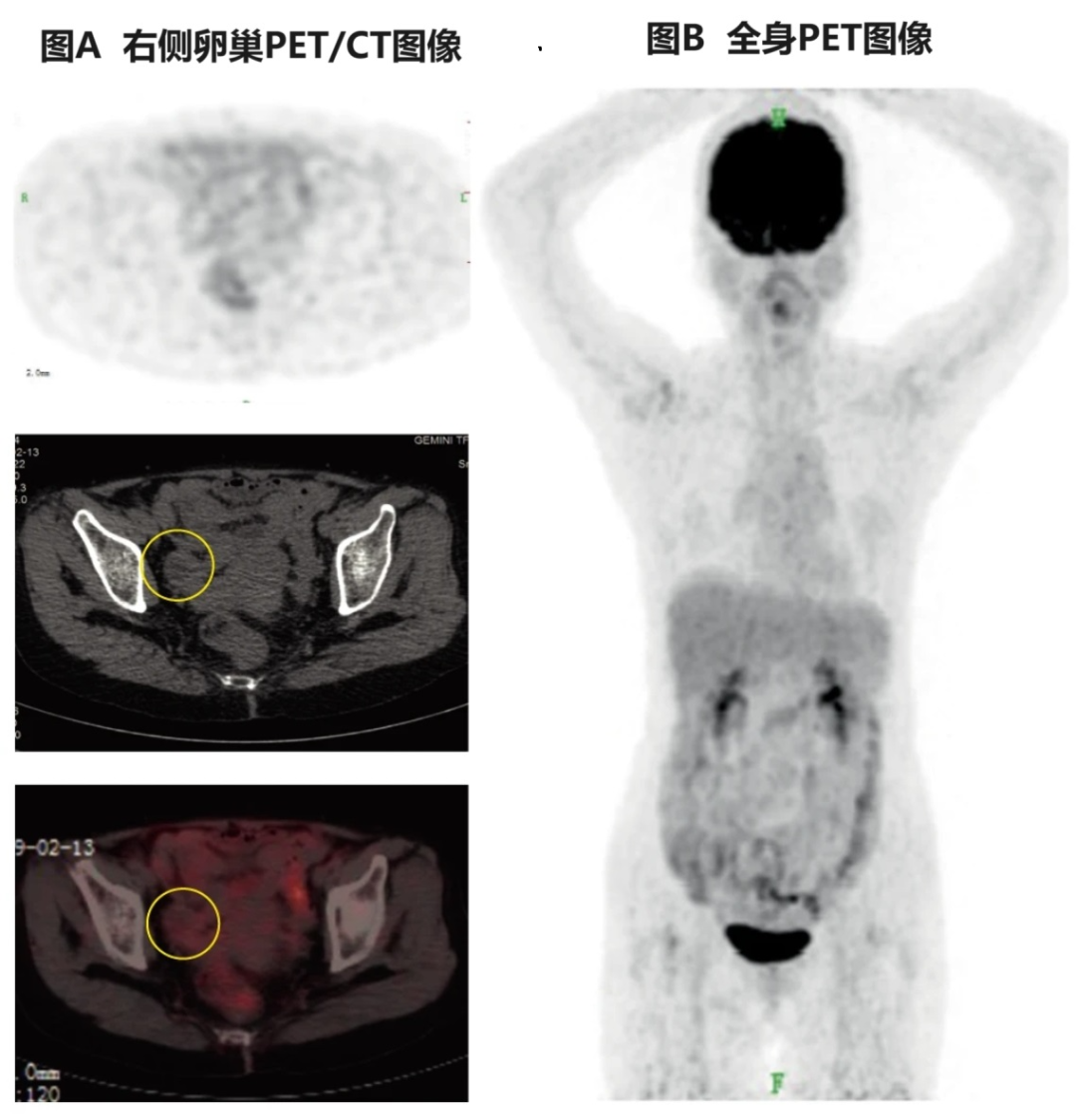
图3 治疗第231天PET/CT图像
▲图源“npj”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:治疗第231天,右侧卵巢病灶完全消退
图4 治疗期间目标肿瘤病变的代表性图像
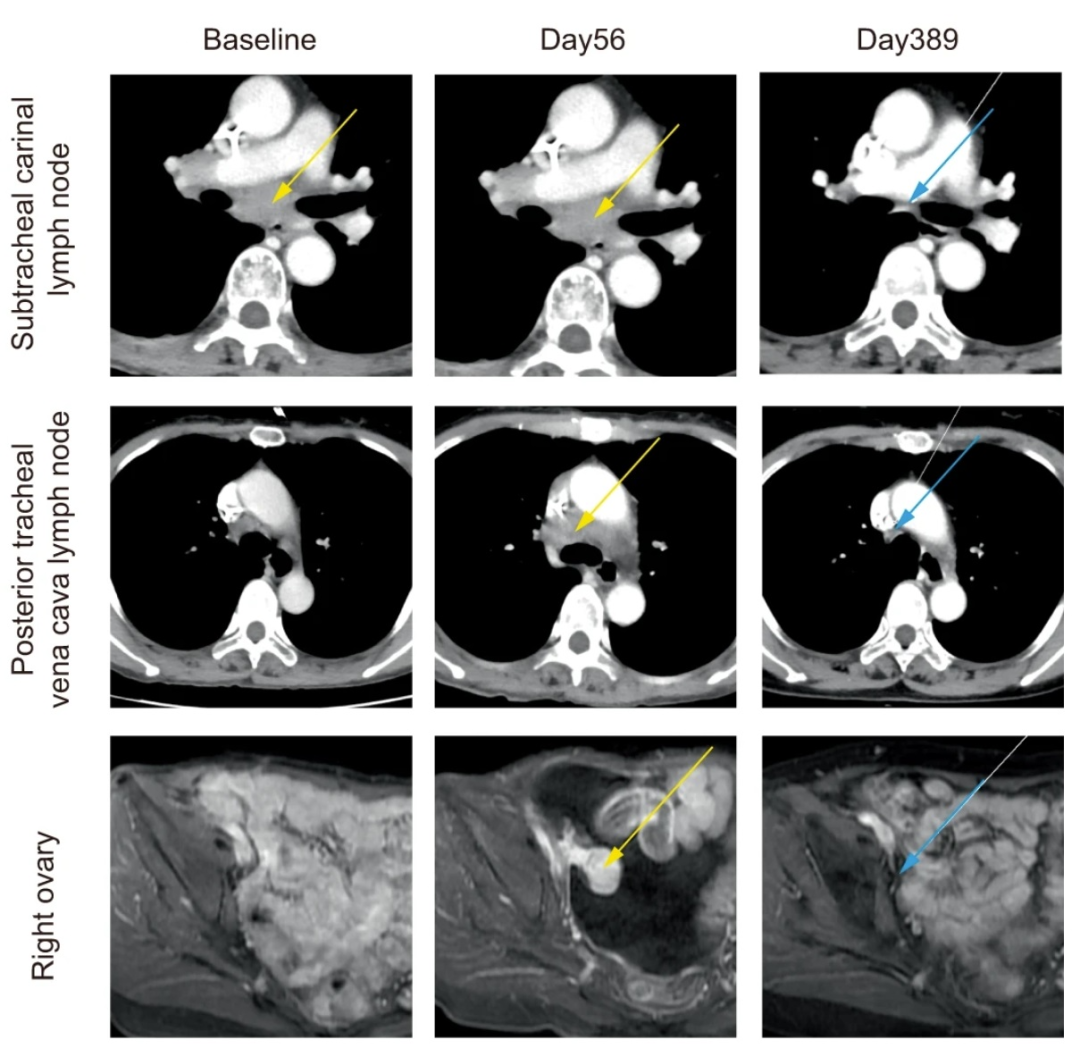
▲图源“npj”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:黄色箭头代表目标肿瘤病变;蓝色箭头代表肿瘤病变完全消退。
5年生存率翻倍!DCVax-L疫苗为脑胶质瘤带来曙光!
胶质母细胞瘤是一种较为凶险的脑部肿瘤,相关研究显示,初次手术后,肿瘤一般会在6~8个月内复发,5年生存率通常低于5%,中位总生存期(mOS)通常为15~17个月。
《美国医学会肿瘤学杂志》报道了一项大型脑瘤树突细胞疫苗(DCVax-L)的Ⅲ期临床试验(NCT00045968),它是近20年来首个针对恶性脑胶质瘤全身性治疗的Ⅲ期临床研究,而且令人惊喜的是研究结果显示,DCVax-L疫苗显著增加了新诊断和复发性脑胶质瘤的长期存活率!
新诊断的脑胶质瘤(nGBM)患者
将入组的331例新诊断的脑胶质瘤患者,随机分为两组,即DCVax-L组(232例)、对照组(99例),结果显示:
1、中位总生存期(OS):19.3个月(DCVax-L组)vs 16.5个月(对照组)。
2、48个月生存率:15.7%(DCVax-L组)vs 9.9%(对照组)。
3、60个月生存率:13.0%(DCVax-L组)vs 5.7%(对照组),这意味着疫苗接种组患者5年生存率翻了一倍多!
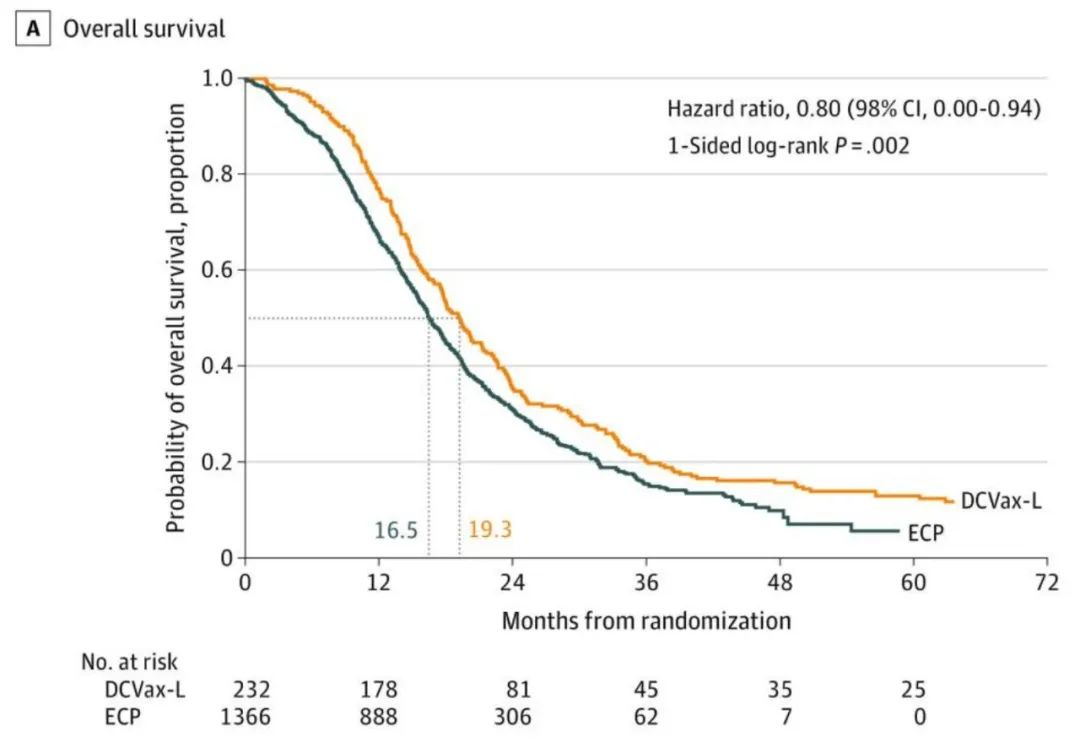
▲图源“JAMA Oncol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
复发的脑胶质瘤(rGBM)患者
在64例接受 DCVax-L 治疗的复发的脑胶质瘤患者中,结果显示如下:
1、复发后的中位总生存期(mOS):13.2个月(DCVax-L组)vs 7.8个月(对照组)。
2、复发后24个月的生存率:20.7%(DCVax-L组)vs 9.6%(对照组)。
3、复发后30个月的生存率:11.1%(DCVax-L组)vs 5.1%(对照组)。
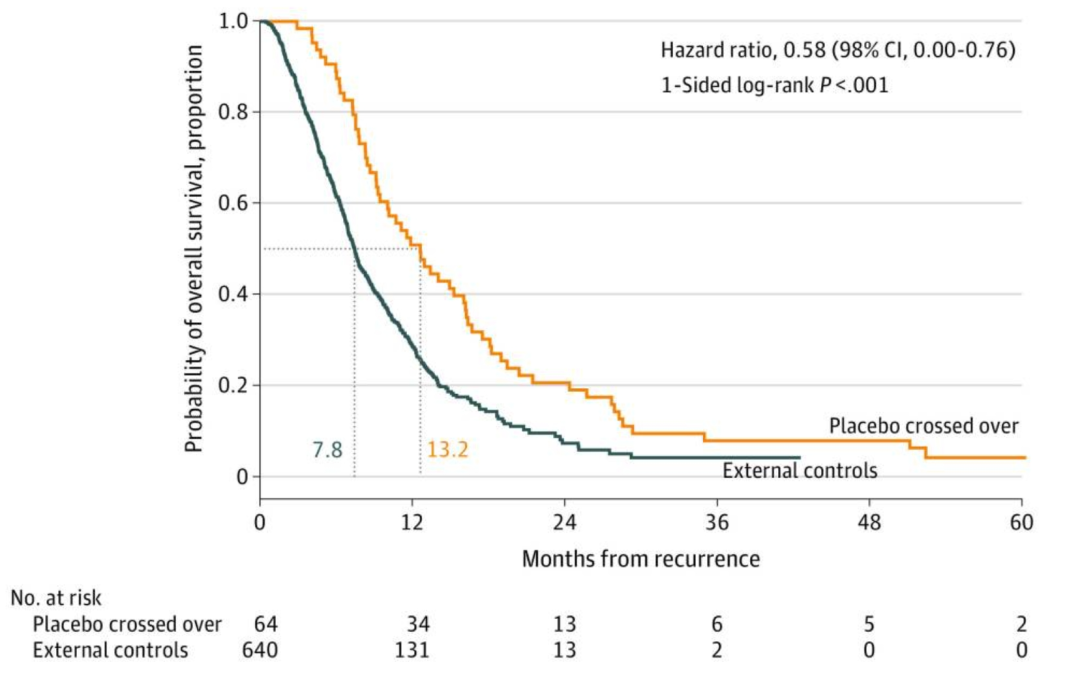
▲图源“JAMA Oncol”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,首次复发时接受DCVax-L治疗的rGBM患者,其死亡风险相对降低了42%,而且这种生存获益随着时间推移,而持续存在。
几款代表性树突细胞疫苗的研究进展
前列腺癌:Provenge疫苗
2010年4月29日,Provenge获美国FDA批准,用于治疗无症状或症状轻微的转移性去势抵抗性前列腺癌(mCRPC),它是首个在美国获批的治疗性疫苗,同时也是FDA批准的唯一一个由患者自身免疫细胞制备而成的治疗前列腺癌的免疫疗法,开创了癌症免疫治疗的新时代!
非小细胞肺癌:DCVac/LuCa疫苗
DCVac/LuCa疫苗是由美国研发的一款针对非小细胞肺癌患者的树突状细胞(DC)疫苗,2022年公布的“DCVAC/LuCa联合卡铂/培美曲塞,治疗晚期非鳞状细胞非小细胞肺癌”的Ⅱ期临床研究结果显示,客观缓解率为31.82%,患者1年生存率达72.73%,2年生存率为52.57%,中位无进展生存期(PFS)为8.0个月。
肾癌:ilixadencel疫苗
ilixadencel(伊利沙定)属于一款同种异体树突状细胞(DC)疫苗。研究显示,与单独应用舒尼替尼(sunitinib,一种靶向抗癌药)相比,“ilixadencel联合舒尼替尼一线治疗”新诊断的晚期转移性肾细胞癌(mRCC),其总缓解率提高近1倍,完全缓解率更高,缓解持续时间更长!
卵巢癌:DCVAC/OvCa疫苗
第50届妇科肿瘤学会(SGO)年会上,公布了一项“DCVAC/OvCa疫苗(基于树突状细胞的免疫疗法)治疗卵巢癌”的Ⅱ期临床研究结果,DCVAC/OvCa联合卡铂+吉西他滨,治疗对铂敏感的晚期复发性上皮卵巢癌,可使患者总生存期(OS)显著延长13.4个月,中位数无进展生存率(mPFS)增加1.8个月,二线治疗的死亡风险降低了62%。
小编寄语
树突状细胞(DC)作为唯一能激活初始T细胞的抗原提呈细胞,在机体免疫过程中发挥重要作用。DC疫苗疫苗既可选择单一表位,也可联合多种表位,还可直接选择肿瘤总mRNA等,进行DC负载,以提高抗癌效果,是一种具有广阔应用前景的新兴免疫治疗方法!
如果您对目前的治疗方案不满意,想寻求日本WT1树突细胞疫苗或其他DC疫苗等抗癌新技术的帮助,可先将病历、近期病理检查结果、出院小结等资料,提交至医学部,进行初步评估。
参考资料
[1]Liu L,et al.Rejuvenation of tumour-specific T cells through bispecific antibodies targeting PD-L1 on dendritic cells. Nat Biomed Eng.2021 Nov;5(11):1261-1273.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9499378/
[2]Shapir Itai Y,et al.Bispecific dendritic-T cell engager potentiates anti-tumor immunity. Cell.2024 Jan 18;187(2):375-389.e18.
https://www.cell.com/cell/abstract/S0092-8674(23)01343-0?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS0092867423013430%3Fshowall%3Dtrue
[3]Guo Z,et al.Durable complete response to neoantigen-loaded dendritic-cell vaccine following anti-PD-1 therapy in metastatic gastric cancer. NPJ Precis Oncol.2022 Jun 3;6(1):34.
https://www.nature.com/articles/s41698-022-00279-3
[4]Nagai H,et al.WT1 Dendritic Cell Vaccine Therapy Improves Immune Profile and Prolongs Progression-Free Survival in End-Stage Lung Cancer[J].Cureus,2023,15(10).
https://www.cureus.com/articles/193305-wt1-dendritic-cell-vaccine-therapy-improves-immune-profile-and-prolongs-progression-free-survival-in-end-stage-lung-cancer#!/
[5]Liau LM,et al.Association of Autologous Tumor Lysate-Loaded Dendritic Cell Vaccination With Extension of Survival Among Patients With Newly Diagnosed and Recurrent Glioblastoma: A Phase 3 Prospective Externally Controlled Cohort Trial. JAMA Oncol. 2023 Jan 1;9(1):112-121.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9673026/
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
早期膀胱癌术后五年生存率高达90%,这五
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

警惕!乳腺癌复发偏爱这3大人群!术后一定
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【实体瘤溶溜病毒免费招募】溶瘤病毒Ml(
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
从多处转移到完全缓解!新型CAR-T细胞
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
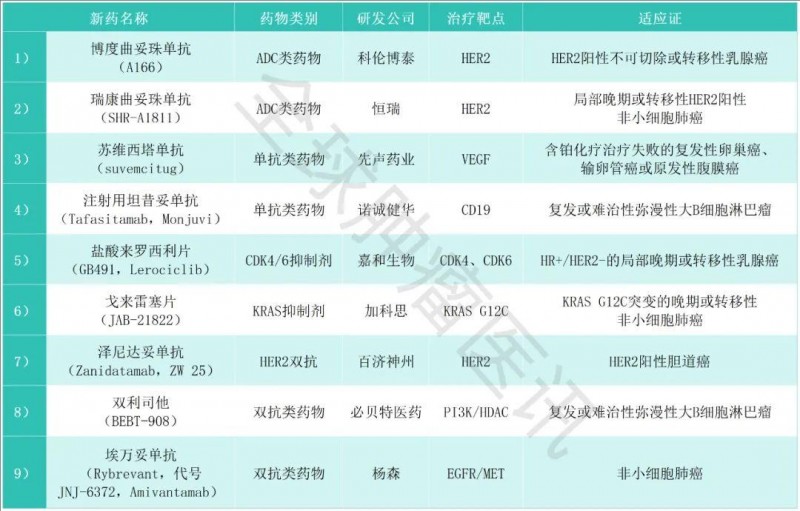
救命药加速入场!2025第二季度9款抗癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




