CAR-T疗法攻克实体瘤再传捷报!瞄准前列腺癌、胰腺癌、肝癌、胃癌,火力全开!
CAR-T细胞疗法攻克实体瘤再传捷报,CAR-T细胞治疗前列腺癌、胰腺癌、肝癌、胃癌,火力全开
CAR-T细胞疗法
多年来,癌症治疗的基本手段是手术、化疗、放疗。在过去的20年里,格列卫(甲磺酸伊马替尼片)和赫赛汀(曲妥珠单抗)这样的靶向药也成为癌症治疗的基本手段。而在过去几年中,免疫治疗异军突起,被科学家们称为癌症治疗的“第五支柱”。
要说近年来最火的癌症疗法,免疫疗法中的CAR-T绝对是被广泛宣传的“抗癌明星”,网络、电视、广播等媒体,铺天盖地,资本市场对此也是趋之若骛,各大机构、各大医院你追我赶,仿佛CAR-T就是攻克癌症的“必杀技”。那么,CAR-T到底是何方神圣呢?
CAR-T疗法就是嵌合抗原受体T细胞免疫疗法,是一种治疗肿瘤的新型精准靶向疗法。通过基因工程技术将T细胞激活,并装上定位导航装置CAR(肿瘤嵌合抗原受体),将T细胞这个普通“战士”改造成“超级战士”,即CAR-T细胞,专门识别体内肿瘤细胞,并高效杀灭肿瘤细胞,从而达到治疗恶性肿瘤的目的。
随着阿基仑赛注射液、瑞基奥仑赛注射液前后在中国获批上市,癌症治疗领域火速掀起一阵“CAR-T热”,中国在2021年正式迎来细胞免疫治疗元年!
这一蜕变或许有望将“抗癌”变为“治癌”,迎来反击癌症的新时代。比起“治标不治本”经常会复发的传统疗法,调用患者体内自身免疫系统的CAR-T可以说是目前最先进的治疗手段。
虽然,CAR-T疗法在实体肿瘤方面如肝癌、胃癌、胰腺癌等消化系统肿瘤中也取得了一定的疗效,但是少之又少。此外,国内外的学者针对CAR-T进行了多种改造,不断地发现新靶点,以用于治疗多种实体肿瘤。
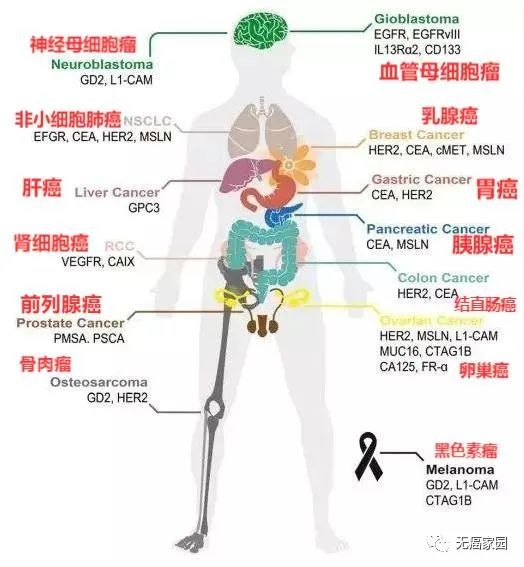
不同癌症的CAR-T靶点分类
攻克实体瘤再传捷报!非病毒载体CAR-T治疗前列腺癌效果喜人
2022年2月17日,在2022年美国临床肿瘤学会泌尿生殖系统癌症专题研讨会(ASCO GU)上,Poseida Therapeutics公司公布了其自体CAR-T细胞疗法P-PSMA-101,在治疗转移性去势抵抗性前列腺癌(mCRPC)患者的1期临床试验的中期结果。

靶向治疗的理想靶点——前列腺特异性膜抗原(PSMA)
P-PSMA-101是一款针对前列腺特异性膜抗原(PSMA)的CAR-T产品,通过对患者自身的T细胞进行基因工程改造,使其可以安全有效地消除肿瘤细胞。P-PSMA-101利用Poseida专有的piggyBac DNA修饰系统开发,该系统能够产出很高比例的干细胞记忆T细胞(Tscm)。
PSMA是一种II型跨膜蛋白,通常在肾小管和十二指肠中表达,并特异性地表达于前列腺癌上皮细胞。在前列腺癌组织中,PSMA的表达明显上调。
研究显示,PSMA在超过90%的前列腺癌细胞表面都出现了过表达(比正常前列腺细胞高100~1000倍),并且在晚期和去势抵抗性前列腺癌患者癌细胞中表达水平更高。因此,PSMA称为前列腺癌诊断及治疗的重要靶点。
治疗前列腺癌,自体CAR-T细胞疗法展现强大潜力
此次公布的1期临床试验中期结果旨在评估P-PSMA-101的安全性、疗效及最大耐受剂量。截止到2021年12月31日,共纳入17例转移性去势抵抗性前列腺癌(mCRPC)患者,其中可评估患者14例。值得一提的是,这些患者平均接受七线治疗,自诊断以来的平均中位时间为6.4年。
在14例患者,分为3组剂量队列进行治疗,具体如下表:
| 剂量队列分组 | 细胞数 | 患者例数 |
| 0.25X106细胞/kg | 平均约2200万细胞 | 6例 |
| 0.75X106细胞/kg | 平均约6100万细胞 | 7例 |
| 2.0X106细胞/kg | 平均约11200万细胞 | 1例 |
试验的关键结果包括:
●71%(10/14)的患者肿瘤标志物前列腺特异性抗原(PSA)水平明显下降;
●36%(5/14)的患者PSA水平下降>50%;
●1例患者显示肿瘤完全消除,并保持10个月以上的持久缓解;
●一些患者的活体组织检查证实,干细胞记忆T细胞(Tscm)这种产品的性质可使CAR-T细胞定向转运到骨骼中,这对前列腺癌等易骨转移的疾病非常重要。
●P-PSMA-101表现出良好的安全性和耐受性。
突破CAR-T疗法局限性,力求更有效,更耐用,副作用更小
在免疫反应中,T细胞发挥着核心作用,能够有效杀死癌细胞,但苦于维持时间短暂(数天或数周不等),这意味着接受CAR-T的患者有复发的可能。
此次P-PSMA-101与一般的CAR-T细胞不同,经非病毒基因递送系统进行工程改造,从而产生很高比例的干细胞记忆T细胞(Tscm)。
Tscm细胞是目前唯一具有自我更新和长寿命的T细胞,会使候选药物更加有效、更耐用,副作用更小。
自体和同种异体CAR-T产品全面开花,覆盖血液肿瘤及实体瘤
此外,该公司全力推进自体和同种异体CAR-T产品,适应症覆盖血液肿瘤及实体瘤。
其中,P-PSMA-ALLO1是该公司首个靶向BCMA的同种异体CAR-T候选产品,正在开发用于治疗复发/难治性多发性骨髓瘤患者。
P-MUC1C-ALLO1是一款同种异体的CAR-T候选产品,用于许多实体肿瘤适应证,包括乳腺癌、结直肠癌、肺癌、卵巢癌、胰腺癌和肾癌,以及其他表达MUC1C的癌症。
此外,还有一款靶向PSMA的同种异体CAR-T候选产品——P-PSMA-ALLO1,正在开发用于治疗mCRPC患者。让我们共同期待这些产品能够获得更多积极进展,早日更更多癌症患者带来新希望。
目前,无癌家园有多款血液肿瘤及实体瘤的CAR-T临床试验正在进行招募,有意向者可咨询医学部具体评估病情!
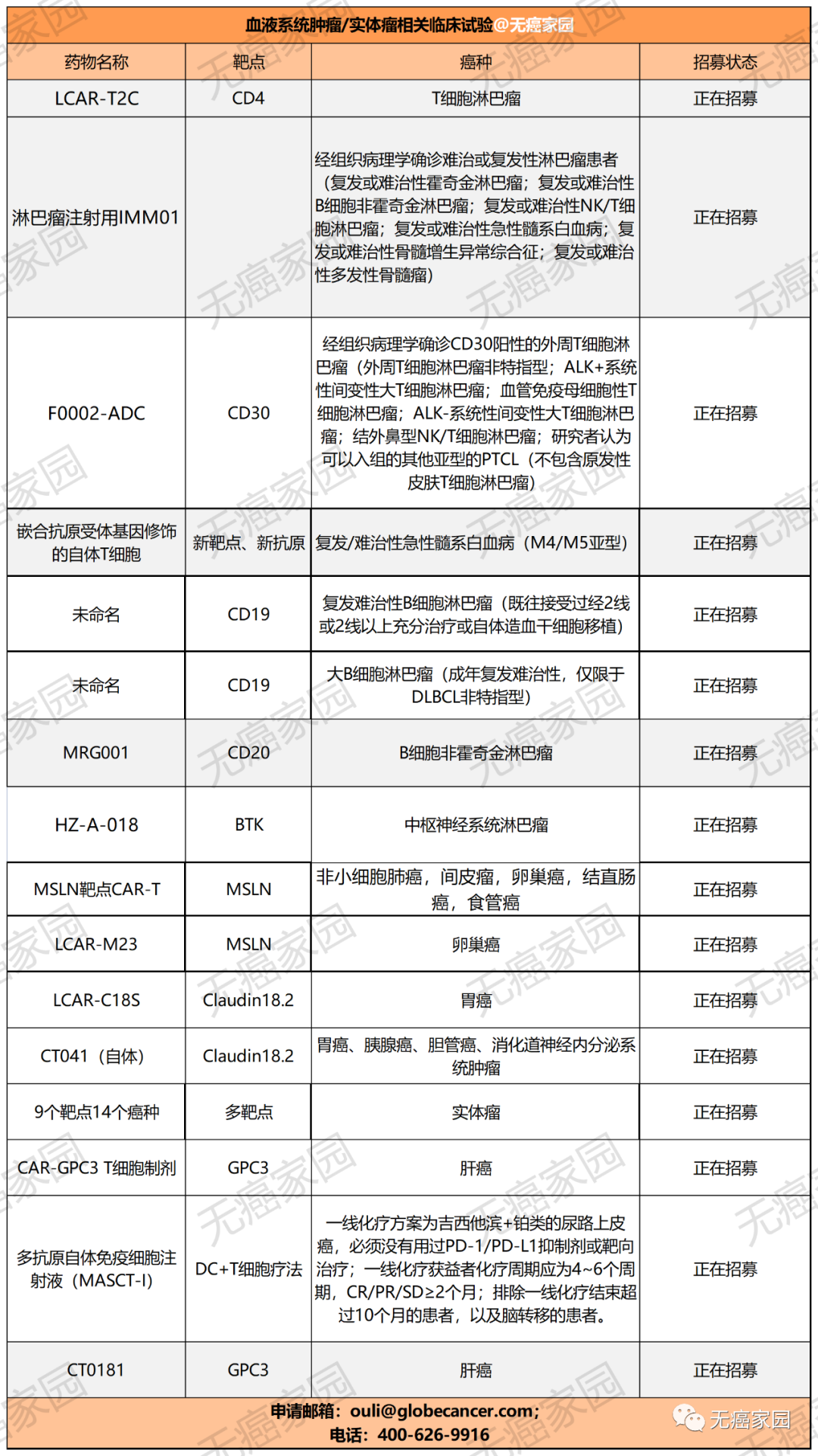
接下来,无癌家园的小编就给大家一一回顾下CAR-T疗法在各癌种中颇为出圈的临床研究,希望为各位癌友们提供新的治疗选择。
CAR-T细胞治疗胃癌及胰腺癌
9月16~21日召开的欧洲肿瘤内科学会(ESMO)年会上,由科济药业开发的靶向Claudin18.2(CLDN18.2)自体CAR-T候选产品CT041展现了其在消化系统肿瘤中的突出疗效,可谓是大放异彩!
Claudin18.2(CLDN18.2)是一种胃特异性膜蛋白,被认为是胃癌和其他癌症类型的潜在治疗靶点。基于此,中国研究人员开发了国际上首个针对 Claudin18.2的CAR-T细胞。
截止到2021年4月8日,纳入的37例CLDN18.2表达阳性的晚期消化道肿瘤患者,其中包括28例胃癌/胃食管结合部癌、5例胰腺癌和4例其他类型的实体瘤,约84%的患者既往接受过至少2线治疗,中位转移器官数量为3个。
研究数据颇为亮眼
1)总疗效:所有患者的客观缓解率达48.6%,疾病控制率达73%;所有胃癌患者总客观缓解率为57.1%。
2)既往接受至少2线治疗失败的胃癌患者:客观缓解率为61.1%,疾病控制率为83.3%。
3)28例胃癌/胃食管结合部癌各亚组:在既往PD-(L)1抑制剂治疗失败、存在腹膜转移、印戒细胞癌等预后差且已无有效治疗手段的患者中,客观缓解率均可维持在50%或以上。
4)安全性:CT041总体耐受性良好,未发生治疗相关死亡或免疫细胞治疗相关神经系统毒性综合征(ICANS)。
除了CT041目前正在开展临床试验外,另外一款针对既往接受过胃全切除术/胃大部切除术后的复发或转移性晚期胃腺癌(包括胃食管结合部腺癌)的靶向Claudin18.2 的CAR-T细胞制剂,名为LCAR-C18S也在临床招募中。
CAR-T细胞治疗肝癌
今年ASCO年会上我国医学研究者们首次公布了靶向GPC3的CAR-T药物(Ori-CAR-001)治疗复发/难治性肝细胞癌的最新临床研究数据。该研究的初步数据显示,Ori-CAR-001在GPC3阳性复发/难治性患者中表现出良好安全性和有效性。
截至2021年3月10日,共纳入11名接受细胞输注的复发受试者。所有受试者均患有晚期肝细胞癌,并且经过化疗、TACE(肝动脉化疗栓塞术)和靶向治疗均无效。9例可评估受试者中,4例达到部分缓解 (PR),3例达到疾病稳定 (SD),2例出现疾病进展 (PD),客观缓解率为44%,疾病控制率达到78%。
在7月29日的国际知名杂志《Journal of Hematology & Oncology》刊登了我国医学研究者们的一项成功改造CAR-T技术的临床研究,研究中提及的CAR-T产品选择的靶点是glypican-3(GPC3)和mesothelin(MSLN)中,报道的治疗结果格外令人惊艳!
其中1例晚期肝癌患者接受了瘤内注射CAR-T治疗,治疗后肝脏病灶代谢基本消失。
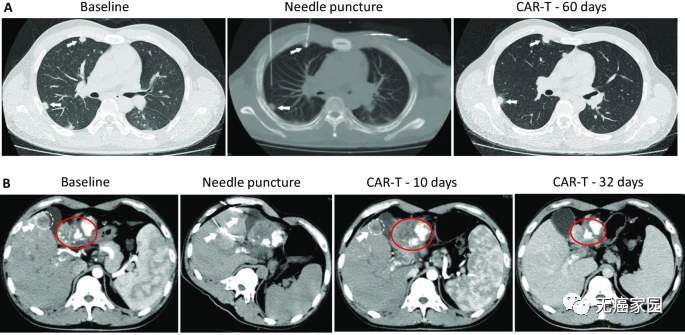
注射60天后,虽然2个肺部结节的尺寸无显著改变;但在第10天时肝脏肿瘤病变显著收缩,注射第32天后则完全消失
更绝的是1例晚期胰腺癌患者,接受的是静脉回输的CAR-T治疗,治疗后全身的病灶,基本都实现了代谢活性完全消失。
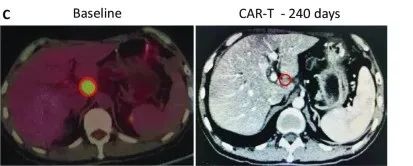
在治疗240天后达到完全缓解,未见其他肿大的淋巴结,患者病灶完全消失
CAR-T细胞治疗卵巢癌
2月18日,国际一流学术期刊《癌症免疫治疗杂志》刊登了关于中国医学研究者采取CAR-T自分泌PD-1抗体用于实体肿瘤治疗的研究成果。临床数据显示,一名晚期难治性卵巢癌患者采用这种治疗手段后,无进展生存5个月,生存达17个月。
结果表明,CAR-T细胞与阿帕替尼的组合将成为治疗晚期/难治性卵巢癌的新治疗方法。
CAR-T细胞治疗甲状腺癌
为了评估抗 TSHR CoupledCAR T 细胞对难治性或复发性甲状腺癌的临床安全性和有效性,我国医学研究人员根据伦理审查委员会批准的方案治疗难治性/复发性甲状腺切除术后甲状腺癌患者。使用抗 TSHR CoupledCAR T 细胞治疗了两名患者,观察到 CAR-T细胞快速扩增并增强了对肿瘤细胞的杀伤。一名患者的最佳反应为完全缓解,另一名患者接近完全缓解。
患者1:男性,64岁,甲状腺乳头状癌。输注后1个月(M1),患者被评估为PR:无法检测到淋巴结转移,并且胸腔气管旁肿瘤结节显著减小。输注后三个月(M3),患者评价为完全缓解,肿瘤组织明显小于M1。
患者2:女性,60岁,甲状腺癌。患者在输注后1个月评估为PR(部分缓解):肺右下叶肿瘤体积缩小约67.51%(从65*55mm减小到42*39mm)。输注后3个月(M3),肿瘤体积较之前缩小约73.54%,SUV max值从14.9降至2.8,因此评估为nCR(接近完全缓解)。
这项研究表明 TSHR 是治疗甲状腺癌的良好靶点,抗 TSHR CoupledCAR T 细胞可安全有效地治疗甲状腺癌。
CAR-T细胞治疗非小细胞肺癌
301医院在国内率先开展CAR-T疗法,成果显著。韩为东教授曾报道过利用EGFR为靶点的CAR-T治疗EGFR表达强阳性(EGFR表达超过50%)的晚期难治性的非小细胞肺癌患者。
研究结果显示,其中11例患者疗效可评价:2例患者肿瘤明显缩小,5例疾病稳定。
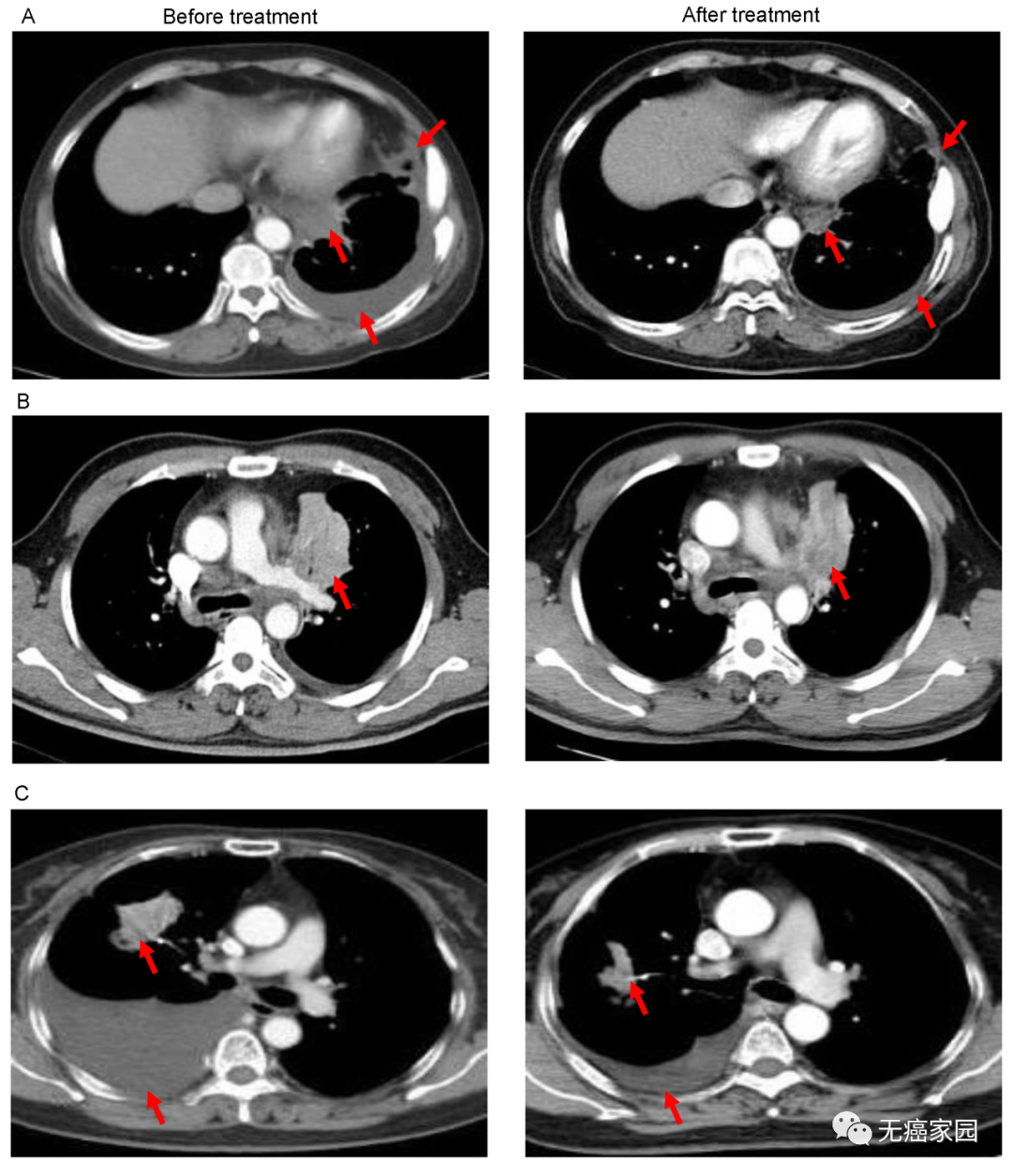
图A中患者1在输注CAR-T细胞后,通过CT扫描显示其胸腔积液减少,转移性肺门淋巴结和胸膜结节轻度缩小(箭头)。
图B中CT图像显示患者8的原发性肿瘤缩小(箭头);
图C中CT检查发现CAR-T治疗后患者9的胸腔积液吸收和肺部病变明显消退。
CAR-T细胞治疗胆道系统肿瘤
在2018年3月,解放军总医院韩卫东教授的团队公布了利用EGFR CAR-T技术治疗胆道系统肿瘤的初步结果。
此次纳入的患者均为EGFR强阳性(>50%的癌细胞表达EGFR)的不可切除的胆道系统恶性肿瘤患者,共纳入19例患者,包括胆管癌14例,胆囊癌5例。
研究结果显示,17例患者可评估,其中1例胆管癌患者的肿瘤完全消失,截止到目前疗效已经保持了22个月,尚未发现疾病复发。10例患者疾病稳定,疗效保持2.5~15.5个月,中位无进展生存期为4个月。
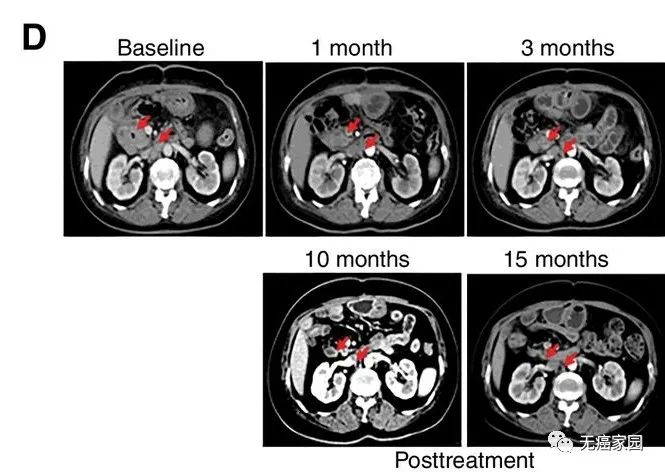
CART-RGFR细胞治疗之前和1、3、10和15个月患者1的CT扫描图像。
红色箭头表示原发肿瘤和腹膜后淋巴结转移。
在研究中有10例患者在化疗预处理中出现3~4级的副作用,经积极处理均可恢复正常。
这是中国人自主研发的针对实体瘤的CAR-T第一次报道不错的临床疗效。极度恶性的胆管癌患者,首次出现了完全缓解,可喜可贺!
CAR-T细胞治疗结直肠癌
据2018年中国癌症统计报告显示:我国结直肠癌发病率、死亡率在全部恶性肿瘤中分别位居第3及第5位,其中新发病例37.6万,死亡病例19.1万。
然而不幸的是,多数患者在确诊时已属于中晚期。手术仅作为对患者的姑息治疗方法,或是仅用于消除对患者影响较大的症状,而以辅助治疗为主,一般治疗的预后都不理想。
自从肿瘤免疫治疗成为第四种癌症治疗方法,研究者们逐渐将目光投向近几年来的热门疗法——CAR-T疗法。
小编根据众多临床研究整理出结直肠癌中CAR-T细胞疗法的潜在靶点,主要包括抗4-1BB(ANTI-4-1BB)、癌胚抗原(CEA)、GUCY2C、TAG-72、EpCAM、上皮糖蛋白40(EGP40)、NKG2D、HER-2、重组人干扰素α/β受体1(IFNAR1)、prominin-1(CD133)、上皮糖蛋白2(EGP-2)。
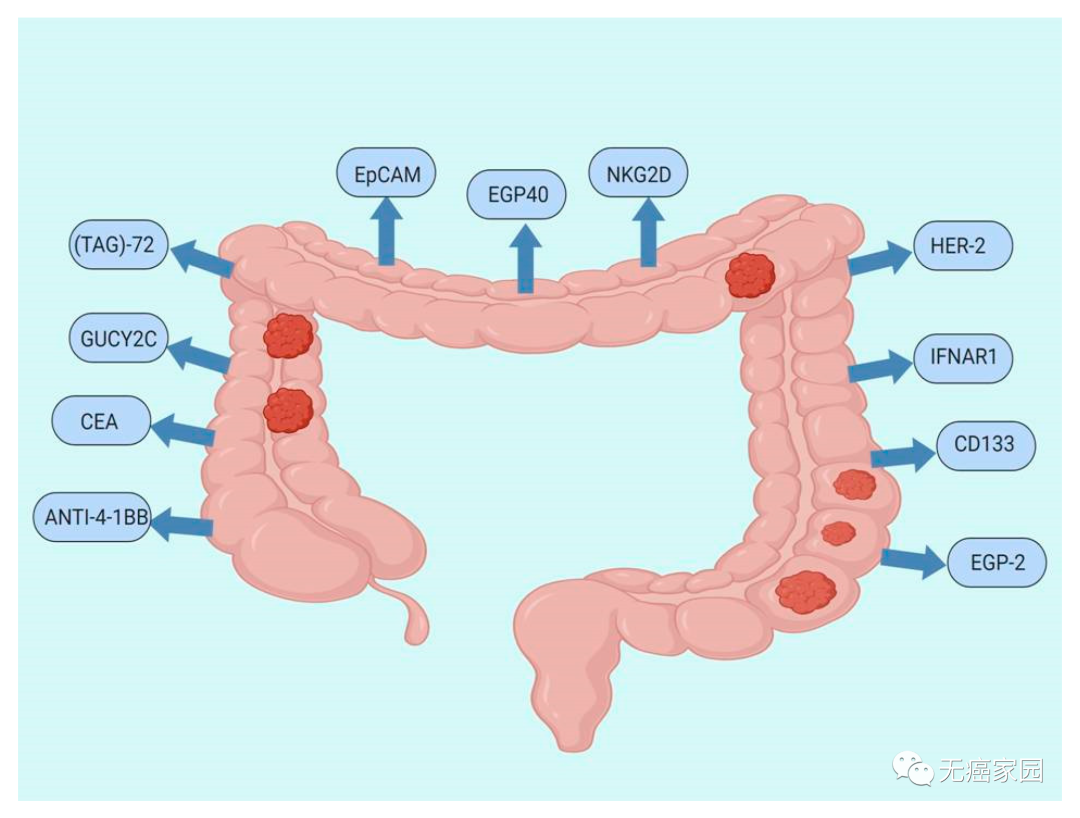
其中结直肠癌的有效靶点GUCY2C是近期研究热门,中国有一项针对7名患者的小型 CAR-T 研究,以结肠癌标志物GUCY2C为靶点。该研究发现,2~3 例患者出现部分缓解和疾病稳定。
CAR-T疗法的获批将为中国患者带来更多临床获益
阿基仑赛注射液、瑞基奥仑赛注射液的纷纷获批上市,首先对符合其适应症的患者又增加了一种新的治疗选择,也就多了一份治愈的希望。
其次,这两次的获批意味着CAR-T疗法已经被国内环境所接纳,未来更多CAR-T产品或适应症的研发及审批都将得到提速,让我们拭目以待CAR-T疗法带来的更多新惊喜!
参考文献
https://www.biospace.com/article/releases/poseida-therapeutics-to-present-interim-results-from-phase-1-trial-of-p-psma-101-at-asco-genitourinary-cancers-symposium/
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

免费治疗机会!PI3K抑制剂TL117胶
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
晚期耐药患者有救了!被纳入肺癌诊疗指南的
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
14:30 愈见大"CAR&q
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
疾病控制率超91%!我国第二款KRAS
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
重磅!全球首个无需REMS(风险评估缓解
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
2024岁末四大抗癌新药上市在即,狙击肺
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




