一文读懂肿瘤的生物治疗
肿瘤生物治疗,肿瘤生物疗法,生物治疗是什么,什么是生物疗法治疗
生物治疗是什么
生物治疗是指通过生物反应修饰剂(BRM)对肿瘤进行治疗的一种方法。它的出现在临床治疗肿瘤方面已发挥了明显的作用,成为肿瘤治疗的第四种主要手段。
BRM这一概念是由奥德汉姆在1983年首先提出的。它是指来自生物体自身的并可通过调动机体固有的防御功能去抵御肿瘤的一些分子和细胞,它们既是机体对内、外环境刺激应答的效应机制,也是机体维持内环境稳定的重要因素。
生物治疗是近十余年来分子生物学、分子免疫学、肿瘤学等学科的基础上发展起来的一种新的治疗肿瘤方法。早在17世纪,有人发现乳腺癌患者如同时发生了其他部位脓肿,可使乳腺癌消退。直到本世纪50年代才逐渐兴起了生物疗法,如卡介苗、转移因数等在临床上的应用,治疗肿瘤收到一定的效果。经过不断发展,在80年代以后,医学界才称之为「最新生物疗法」。生物疗法的主要作用是提高肿瘤患者的全身免疫功能,使肿瘤逐渐缩小消失,现已成为继外科、放疗和化疗后最有发展前途的一种重要的治疗肿瘤手段。
生物治疗共有四大类,即细胞治疗法、细胞毒素治疗法、基因治疗法和抗体治疗法。
肿瘤生物治疗
作为仅次于心血管疾病的第二大死亡原因,肿瘤已成为当今世界威胁人类健康的主要疾病之一。据世界卫生组织公布的最新数据显示,到2030年,全球因肿瘤死亡人数将增至1300万,新肿瘤病例将增至2200万。
在我国,据卫生部公布的最新统计据显示,我国肿瘤发生率正处于快速上升期,每年新增肿瘤病例260万,有180万人因肿瘤去世,肿瘤已成为中国城市和农村居民的第一死因。 对于肿瘤的治疗,几乎每个患者都在沿着手术、放疗、化疗这条路艰难前行。
传统的治疗手段虽然能暂时遏制肿瘤的发展,但却不能从根本上解决肿瘤的复发、转移和扩散等问题。同时,由于巨大的毒副作用,使得肿瘤患者自身免疫力下降,最终残存的肿瘤细胞死灰复燃,反而加速了病情的恶化。
近年来,随着肿瘤学、免疫学、分子生物学及生物工程等技术的迅速发展和交叉渗透,如何从肿瘤发病的根本原因入手,防止肿瘤的转移和复发,提高恶性肿瘤患者的生存时间,已成为世界各国科学家治疗肿瘤的方向,也是肿瘤治疗的根本出路。
肿瘤生物治疗(tumor biotherapy)是一种新兴的、具有显著疗效的肿瘤治疗模式,它是运用生物技术和生物制剂干扰肿瘤细胞的发生、生长、分化、凋亡、侵袭、转移和复发,促进机体免疫系统重建,使细胞毒性物质集中于肿瘤组织,从而激发和增强机体对肿瘤的生物应答,达到控制和消灭体内微小残留病灶,甚至使晚期肿瘤得到部分或完全缓解的治疗方法。
由于高度特异性,没有任何毒副作用,降低了肿瘤患者术后复发、转移的几率,提高了患者对放化疗的敏感性及耐受性,使得肿瘤生物治疗成为继手术、放疗和化疗之后的第四大肿瘤治疗技术。包括细肿瘤生物治疗常用的方法主要包括细胞因子治疗、过继性细胞免疫治疗、肿瘤疫苗治疗、肿瘤基因治疗、分子靶向药物治疗、抗新生血管生成治疗等。
根据肿瘤生物治疗的原理可以将其分为四大类(见表1)。其中,肿瘤的主动免疫治疗是指给机体输入具有抗原性的瘤苗,刺激机体免疫系统产生抗肿瘤免疫以治疗肿瘤的方法;而肿瘤的被动免疫治疗是指给机体输注外源的免疫效应物质,由这些外源性效应物质在机体内发挥治疗肿瘤作用。
表1 肿瘤生物治疗的分类
图表1
一、体细胞治疗与细胞因子治疗
细胞因子是由活化的免疫细胞(单核/巨噬细胞、T细胞、B细胞、NK细胞等)和一些非免疫细胞(血管内皮细胞、表皮细胞、纤维母细胞)经刺激而合成、分泌的一类作为细胞间信号传递分子的、具有广泛生物学活性的小分子蛋白,具有调节免疫应答、免疫细胞分化和发育,参与炎性反应,刺激造血功能等作用。
细胞因子具有多种活性,如重叠性、拮性、多效性、协同性等,调整机体的生理功能,刺激细胞活化、分化、增殖和凋亡,与肿瘤发生、发展的有关。临床应用较多的有干扰素(IFN-α,IFN-β,IFN-γ)、白细胞介素(IL-2,IL-4,IL-7,IL-12等)、造血刺激因子(EPO,TPO,G-CSF,GM-CSF,IL-11,IL-3等)、肿瘤坏死因子(TNF-α)、修复因子(GM1,EGF,BFGF)等。
1. 干扰素:干扰素(interferon, IFN)是有核细胞在诱生剂的刺激下产生的糖蛋白,根据细胞来源、理化性质和抗原特征可以分为IFN-α、IFN-β、IFN-γ这三种类型。干扰素的生物学效应主要包括抑制病毒在细胞内的增殖、抑制细胞分裂、增强免疫细胞的活性等,它被广泛应用于毛细胞性白血病、慢性粒细胞白血病、多发性骨髓瘤、非霍奇金淋巴瘤、肾癌及黑色素瘤等肿瘤的治疗。
2. 白细胞介素-2:白细胞介素-2(IL-2)是目前应用最广泛的白细胞介素(interleukin, IL),它是活化的T细胞产生的活性递质,能诱导淋巴细胞的增殖反应,诱导LAK细胞的生成,促进B淋巴细胞的增殖分化,参与机体多种免疫调节等。IL-2适用范围广,适用于各种实体瘤,恶性浆膜腔积液,肾癌,黑色素瘤等。
3. 促红细胞生成素:促红细胞生成素(erythropoietin, EPO)是由肾小管间质细胞产生的、促进红细胞系前体细胞增殖与分红成熟的细胞因子,临床上主要运用于肾性贫血的治疗,对肿瘤放化疗后引起的贫血也有一定疗效。
4. 集落刺激因子:集落刺激因子(colony stimulating factor, CSF)是一类促进造血祖细胞形成粒细胞和巨噬细胞等克隆的细胞因子。粒细胞集落刺激因子(G-CSF)和粒细胞巨噬细胞集落刺激因子(GM-CSF)是临床上常用的集落刺激因子。G-CSF具有促进骨髓粒细胞系祖细胞生成、分化、成熟,增强中性粒细胞的功能等作用,适用于肿瘤放化疗后引起的粒细胞减少;GM-CSF具有促进粒系统和单核巨噬细胞系统的增殖,激活成熟粒细胞和单核巨噬细胞的作用,可用于肿瘤的免疫治疗。
二、过继性细胞免疫治疗
肿瘤过继性细胞免疫治疗是指将体外扩增及激活的肿瘤特异性免疫细胞过继回输给肿瘤病人,进行肿瘤治疗的方法。过继性细胞免疫可分为特异性和非特异性两类,前者是用已知抗原致敏的淋巴细胞注入受体后使其获得对该抗原的细胞免疫能力;后者是用未经特殊抗原致敏的正常人淋巴细胞注入受体后使其获得对多种抗原的细胞免疫能力。特异性过继性细胞免疫治疗所使用的细胞主要包括TIL和特异性转基因T细胞;非特异性过继性细胞免疫治疗所使用的细胞主要包括LAK、CD3AK和CIK等。
1. LAK:淋巴因子激活的杀伤细胞(lymphokine-activated killer cell, LAK)是采用IL-2在体外刺激、活化外周血单核细胞而诱导产生的非效应性细胞毒作用的效应细胞。LAK细胞对正常细胞没有杀伤效应,对肿瘤细胞的杀伤表现为MHC非限制性、广谱性、非特异性。
由于LAK杀伤力不强,扩增能力有限,因此,在临床上应用LAK时需大量输注,且在输注的同时须大剂量应用IL-2。在大量应用IL-2时刻出现多种毒副反应,最严重的是毛细血管渗漏综合征(capillary leak syndrome),主要表现为全身性水肿和多器官功能失调,可引起胸腹腔积液、肺间质水肿和充血性心力衰竭。
2. TIL:肿瘤浸润淋巴细胞(tumor infiltrating lymphocyte, TIL)是从肿瘤组织中分离的T淋巴细胞在体外经IL-2激活后大量扩增形成,对肿瘤细胞具有很强的杀伤活性。TIL对肿瘤有一定的特异性,其杀伤效应是LAK细胞的50~100倍。将TIL回输到机体内血液或肿瘤中它可以持续起效两个月。目前,TIL在临床中已用于治疗皮肤、肝、肾、肺、头颈部、卵巢等部位的原发或继发性肿瘤,有着巨大的潜在治疗价值。
3. CD3 AK:抗CD3 单克隆抗体激活的杀伤细胞(anti-CD3 monoclonal antibody activated killer cell, CD3 AK)是采用抗CD3单克隆抗体作为主要的刺激因子与IL-2一起刺激淋巴细胞诱生的杀瘤效应细胞。其最大特点是CD3 单克隆抗体在体外可刺激淋巴细胞大量扩增,对淋巴细胞的激活一次性完成并能保持至少16天的增殖生长趋势,其扩增效应远高于单纯采用IL-2刺激活化的淋巴细胞(LAK、TIL等)。
CD3 AK主要用于肿瘤术后清除残余肿瘤细胞,对于延缓复发、延长肿瘤患者的生存期有一定的作用。自1993年CD3 AK被报道联合IL-2用于治疗肿瘤以来,CD3 AK的应用发展迅速,2008年在美国肿瘤学大会上再次报道了CD3 AK联合IL-2成功用于肾癌的治疗。最近有研究表明,CD28单抗能增强CD3 AK的抗肿瘤活性。
4. CIK细胞:细胞因子诱导的杀伤细胞(cytokine induced killer cell, CIK)是在CD3 AK基础上制备的一类新的具有肿瘤杀伤效应的细胞,它是以CD3 +和CD56 +细胞为主的抑制细胞群。CIK能溶解多种肿瘤细胞,表现为非MHC限制性杀伤,对化疗药物敏感的耐药的肿瘤细胞均有较好的杀伤作用。
CIK的杀伤活性剂治疗效果优于LAK和CD3 AK。由于CIK能长时间保持细胞的杀瘤活性,因此具有较大的临床应用价值。
目前,CIK细胞的抗肿瘤机制尚未完全阐明,其可能机制为:
(1)CIK细胞中CD3 +、CD56 +T细胞以 MHC非限制机制杀伤体内残留的肿瘤细胞,并通过 LIF-1/ICAM-1 系统与靶细胞结合,释放颗粒酶和穿孔素对靶细胞实行MHC非限制性杀伤;
(2)CIK细胞中 CD3 +CD8 +T细胞和 CD3 +CD4 +T细胞具备免疫调节作用,可间接杀伤肿瘤细胞;
(3)通过变形及趋向运动接近粘附靶细胞,释放一些穿孔素、颗粒酶等化学介质,使靶细胞发生溶解坏死和细胞凋亡,从而杀伤靶细胞。
5. γδT细胞: γδ T细胞是介于特异性免疫与非特异性免疫之间的一种特殊类型的免疫细胞,它主要分布于皮肤和黏膜组织,在人体内含量不超过T细胞总数的5%。在抗肿瘤免疫早期,γδT细胞同时具有DC疫苗及NK等细胞的功能特点,有较强的特异性和非特异性肿瘤杀伤能力。但由于含量低,γδT细胞发挥的作用非常有限。
6. 联合细胞治疗
(1)DC-CIK细胞治疗
DC以及CIK作为肿瘤免疫治疗上的两个重要的细胞,DC可识别抗原,激活获得性免疫系统;而CIK可以借助自身的细胞毒性以及分泌细胞因子实现杀伤肿瘤细胞的目的,两者的联合使用可以构造一个高效稳定的免疫体系,从而起到更好的杀瘤作用。把具有肿瘤抗原的DC细胞与CIK细胞混合培养能够增强细胞因子的释放以及细胞毒性,大幅提升CIK细胞的增殖能力以及杀伤活性,并让机体的特异性抗肿瘤免疫效应得到激发,实现对肿瘤的长期控制杀伤目标。
CIK-DC肿瘤治疗中的DC疫苗技术是现在仅有的通过国家批准进入临床、获得国家级认证的高科技肿瘤生物治疗方法。目前,CIK-DC细胞疗法已广泛应用于临床各个系统疾病,特别是在清除白血病微小残留和治疗恶性肿瘤方面,取得了较理想的治疗效果。
(2)CLS多细胞免疫治疗
CLS多细胞免疫治疗是在DC-CIK细胞治疗的基础上增加了三种抗肿瘤免疫细胞:CD3AK细胞、NK细胞和γδT细胞。NK细胞可以有效地杀伤肿瘤干细胞,同时也具有杀伤成熟肿瘤细胞的功能;γδT细胞在杀伤肿瘤细胞的同时又可以与DC细胞互为补充,对DC无法识别的肿瘤细胞进行标记杀伤;CD3AK细胞针对病毒癌细胞具有超强杀伤力。
新增加的免疫细胞一方面都具有各自的独特杀伤能力,杀伤范围扩大,疗法的特异性抗肿瘤能力增强;另一方面,γδT细胞在杀伤肿瘤细胞的同时又与DC细胞互为补充,对DC无法识别的肿瘤细胞进行标记杀伤,不仅加强了特异性抗肿瘤能力,且提高了对肿瘤细胞的识别能力,有利于彻底清除肿瘤细胞,成为细胞生物治疗的第一方案。
7. 基于嵌合抗原受体修饰T细胞的过继性免疫治疗:嵌合抗原受体修饰T细胞(chimeric antigen receptor T-cell, CAR-T细胞)是以能编码单链抗体-共刺激分子-免疫受体酪氨酸活化基序的嵌合分子的融合基因修饰T细胞而产生的一种特殊的基因修饰T细胞。
通过基因修饰的手段,使能特异性识别靶抗原的单克隆抗体的单链可变区表达在T细胞内的活化增殖信号域相耦联。CAR-T细胞将单克隆抗体对靶抗原的特异性识别与T细胞的功能相结合,产生特异性的杀伤作用,而且能够以非主要相容性复合体限制性的方式杀伤靶细胞。目前关于CAR-T的研究正如火如荼地进行。
三、肿瘤疫苗治疗
肿瘤疫苗的原理是利用诱导机体的特异性细胞免疫和体液免疫反应,增强机体的抗肿瘤效应,从而抑制肿瘤细胞的生长、转移和复发。目前研究比较多的有肿瘤细胞疫苗、肿瘤多肽疫苗、肿瘤基因工程疫苗、肿瘤核酸疫苗和抗独特型抗体疫苗等。
1. 肿瘤细胞疫苗:将完整的肿瘤细胞经物理照射、研磨、热灭活等方法处理以及基因修饰后接种于患者。然而,单独使用自体或异体的肿瘤细胞难以产生足够强度的免疫应答。具有局限性,不能达到有效控制和治疗肿瘤的目的。
2. 树突状细胞疫苗:树突细胞(dendritic cell, DC)是目前发现的功能最强的专职抗原递呈细胞(antigen presenting cell, APC),它能摄取、加工、和递呈抗肿瘤抗原,是机体免疫反应的启动者的参与者。临床上已采用DC疫苗回输进行抗肿瘤免疫治疗,并已经在多种肿瘤的治疗中取得了很好的疗效。
3. 多肽疫苗:采用肿瘤相关抗原或肿瘤特异性抗原的特异性表位诱导特异性的CTL免疫应答。由于多肽疫苗具有肿瘤抗原特异性,可诱导特异性免疫应答以及对正常细胞无害等优点使得其具有较强的特异性。但是,较弱的免疫原性阻碍了多肽疫苗的应用。
4. 肿瘤基因工程疫苗:肿瘤基因工程疫苗是将编码某种抗原的基因片段克隆到真核表达质粒并直接注入机体,利用宿主细胞的转译系统表达相应抗原,从而诱导机体产生特异性体液和细胞免疫应答。目前,国际上已有多种肿瘤疫苗已经在进行临床试验中。
5. 基因疫苗:基因疫苗又称为核酸疫苗,包括DNA疫苗和RNA疫苗。它是将携带编码肿瘤抗原基因的核酸载体疫苗注入组织细胞内,以激发免疫反应。肿瘤基因疫苗由于必须设法将基因转化到抗原呈递细胞上,至今未有突破性的进展
6. 抗独特型肿瘤疫苗:由抗独特型抗体制成的疫苗,具有模拟肿瘤抗原和免疫调节的双重作用,能打破肿瘤患者免疫耐受或免疫抑制状态,产生抗肿瘤免疫反应,延长肿瘤患者存活期,提高生活质量。抗独特型抗体疫苗包括Ab1和Ab2疫苗、微抗体疫苗、单链抗体疫苗等。
四、分子靶向药物治疗
分子靶向药物主要有两类:单克隆抗体和表皮生长因子受体-酪氨酸激酶抑制剂(EGFR-TKI)的小分子化合物。近十年来,人源化抗体作为肿瘤特异性靶向药物在临床上取得了极大的成功。
1. 单克隆抗体类:单克隆抗体类分子靶向药物常用的有:赫赛汀、美罗华(利妥昔单抗)、西妥昔单抗和阿瓦斯汀等,一些单克隆抗体具有直接的抗肿瘤作用,大多数单克隆抗体不具有直接杀死肿瘤细胞的特点,它们可以通过耦联一种细胞杀伤介质,靶向作用于肿瘤位点,起到特异性杀伤肿瘤细胞的作用,从而增强对肿瘤细胞的杀伤效应,减少对正常细胞的损害。
(1)赫赛汀(Herceptin/ Trastuzumab):是一种作用于人类表皮生长因子受体II的单克隆抗体,1998由美国FDA批准上市,与紫杉醇联用可作为HER2/neu过度表达或不适合采用蒽环类药物治疗的晚期乳腺癌的一线治疗方案。
(2)美罗华(Mabthera/Rituximab):是一种针对CD20的人/鼠嵌合单克隆抗体,也 是全球第一个被批准用于临床治疗非霍奇金淋巴瘤(NHL)的单克隆抗体。美罗华因在过去20年里治疗侵袭性非霍奇金淋巴瘤,全面提高患者总生存率,仅伴随极小的毒副作用而备受瞩目。
(3)西妥昔单抗(Erbitux/Cetuximab/IMC-C225):是一种抗表皮生长因子受体(epithelial growth factor receptor, EGFR)的人/鼠嵌合的单克隆抗体,可与表达于正常细胞和多种癌细胞表面的EGF受体特异性结合,并竞争性阻断EGF和其他配体,进而达到抑制肿瘤细胞增殖和转移的作用。西妥昔单抗对EGFR阳性的肿瘤具有较好的疗效,可以提高患者生存率,延长缓解期。
(4)阿瓦斯汀(Avastin/Bevacizumab/rhuMAb-VEGF):是重组人抗血管内皮生长因子(vascular endothelial growth factor, VEGF)配体的单克隆抗体,也是第一个被美国FDA批准的通过抑制血管生成而发挥抗癌作用的新药。阿瓦斯汀已被批准治疗肺癌、结直肠癌、乳腺癌等多种肿瘤。
2. 小分子化合物
酪氨酸激酶受体的过度表达或过度激活在许多肿瘤中均可见到,它往往导致下游信号途径的激活,最终导致细胞的转化、增殖和抵抗细胞凋亡,与肿瘤的发生发展密切相关。阻断酪氨酸激酶受体信号传导途径,将可以阻止细胞的过度增殖。常见的药物有:格列卫、吉非替尼、厄洛替尼。
(1)格列卫(Glivec/imatinib mesylate/STI-571):是一种能抑制酪氨酸激酶第571号信号转导的小分子化合物,能特异地与BCR-ABL基因的ATP位点结合并抑制该酶的活性,阻断肿瘤细胞的信号转导,选择性抑制肿瘤生长,而不影响正常细胞的功能。已被美国FDA批准用于治疗慢性粒细胞白血病(CML),胃肠道间质瘤(GIST)等。
(2)吉非替尼(Gefitinib/Iressa/ZD1839):是一种新型的小分子量肿瘤治疗药物,主要是通过抑制EGFR自身磷酸化而阻滞传导,抑制肿瘤细胞的增殖,实现靶向治疗。临床主要用于治疗既往接受过化学治疗的局部晚期或转移性非小细胞肺癌,尤其对肺腺癌疗效确切
(3)厄洛替尼(Erlotinib/ Tarceva/OSI-774):是一种创新的生物靶向抗癌药物,适用于所有非小细胞肺癌患者,是现在世界上唯一经国际大型III期随机对照临床研究证明能够显著延长非小细胞肺癌(NSCLC)患者生命的人体表皮生长因子(EGFR)酪氨酸激酶抑制剂,具有广阔的前景。
五基因治疗
基因治疗是指利用细胞工程技术将外源目的基因导人人体靶细胞或组织以取代有缺陷的基因,通过其正常表达,以达到防治肿瘤的目的。肿瘤基因治疗主要有以下几种方式:基因替代、基因修饰、基因添加、基因补充、基因封闭等。根据功能基因导入方式不同分为体内基因治疗和体外基因治疗。常用病毒作为运送基因的载体。目前已有基因转导p53、基因转导的DC、基因转导的TIL等运用于各期临床研究。
参考文献
1. http://www.who.int/en/index.html
2. 罗荣城,尤长宣.肿瘤生物治疗新进展[J].中国新药杂志,2005,14(2):143-146.
3. 马锡慧,高钰.树突状细胞联合细胞因子诱导的肿瘤杀伤细胞生物学特性及其在肿瘤治疗中的研究进展[J].医学综述,2013,19(23):4268-4270.
4. 张艳.生物治疗在肿瘤综合治疗中的作用[J].医学综述,2013,19(19):3507-3510.
5. 白东晓,姚德茂.肿瘤细胞疫苗的研究进展[J].现代肿瘤医学,2006,14(2):245-248.
6. 刘宝瑞,钱晓萍.临床肿瘤学——基本理论与诊疗路径[M].北京:科学出版社,2007.
7. Rosenberg SA. Karnofsky Memorial Lecture. The immunotherapy and gene therapy of cancer[J]. J Clin Oncol, 1992, 10(2): 180-199.
8. Wolchok JD, Hoos A, O'Day S, et al. Guidelines for the evaluation of immune therapy activity in solid tumors: immune-related response criteria[J]. Clin Cancer Res, 2009, 15(23): 7412-7420.
9. Richman LP, Vonderheide RH. Role of crosslinking for agonistic CD40 monoclonal antibodies as immune therapy of cancer[J]. Cancer Immunol Res, 2013: canimm. 0152.2013.
10. Palucka K, Banchereau J. Dendritic-cell-based therapeutic cancer vaccines[J]. Immunity, 2013, 39(1): 38-48.
11. Kroemer G, Galluzzi L, Kepp O, et al. Immunogenic cell death in cancer therapy[J]. Annu Rev Immunol, 2013, 31: 51-72.
12. Steinman RM, Cohn ZA. Identification of a novel cell type in peripheral lymphoid organs of mice[J]. J Immunol, 2007, 178(1): 5-25.
13. Koido S, Hara E, Homma S, et al. Cancer immunotherapy by fusions of dendritic cells and tumor cells[J]. Immunotherapy, 2009, 1(1): 49-62.
14. Zhang J, Wang Y, Wu Y, et al. Mannan-modified adenovirus encoding VEGFR-2 as a vaccine to induce anti-tumor immunity[J]. J Cancer Res Clin. 2014: 1-12.
15. Miest TS, Cattaneo R. New viruses for cancer therapy: meeting clinical needs[J]. Nature Rev Microbiol, 2014, 12(1), 23-34.
16. Wenqing Wei,Jing Liu,Mancang Zhao, et al.The effect of anti-CD28 on the CD3-AK proliferation and tumoricidal activity[J].中德临床肿瘤学杂志(英文版),2012,11(8):469-471.
(来源:科学网陈润哲的博客 2016-2-15 )
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
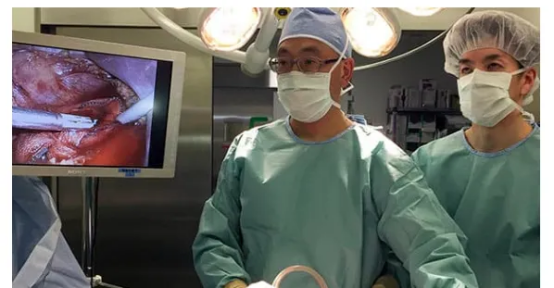
早期膀胱癌术后五年生存率高达90%,这五
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

警惕!乳腺癌复发偏爱这3大人群!术后一定
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【实体瘤溶溜病毒免费招募】溶瘤病毒Ml(
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
从多处转移到完全缓解!新型CAR-T细胞
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
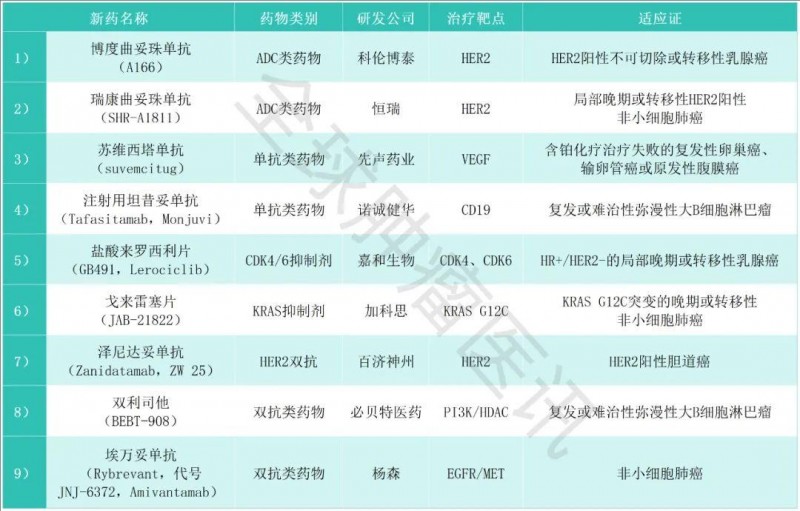
救命药加速入场!2025第二季度9款抗癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05



 Qzone
Qzone



![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




