【临床试验招募】宝船生物BC008临床试验
招募标准
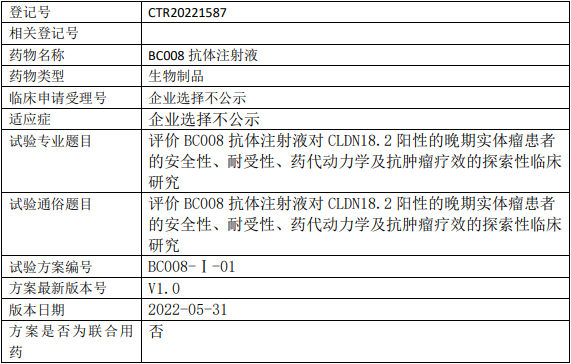
宝船生物BC008临床试验,评价BC008抗体注射液治疗CLDN18.2阳性的晚期实体瘤安全性、耐受性、药代动力学及抗肿瘤疗效的探索性I期临床试验
试验目的
主要目的
评估BC008治疗CLDN18.2阳性的晚期实体瘤受试者的剂量限制性毒性(DLT)、最大耐受剂量(MTD)。
次要目的
1)评价BC008的药代动力学(PK)特征;
2)评价BC008的安全性;
3)评价BC008的免疫原性;
4)评价BC008在CLDN18.2阳性的晚期实体瘤患者中的初步疗效。
探索性目的
回顾性分析CLDN18.2的表达和BC008疗效的相关性。
试验设计
试验分类:安全性
试验分期:I期
设计类型:单臂试验
随机化:非随机化
盲法:开放
试验范围:国内试验
受试者信息
年龄:18岁(最小年龄)至无上限(最大年龄)
性别:男+女
健康受试者:无
出入排标准
入排标准
入选标准
1、须对本研究知情同意,并自愿签署书面的知情同意书。
2、年龄≥18周岁,性别不限。
3、递增阶段:组织学或细胞学确认、经标准治疗失败、不可切除或转移性晚期实体瘤受试者;CLDN18.2蛋白阳性(中心实验室IHC检测≥1%的肿瘤细胞CLDN18.2膜染色≥1+)。
4、扩展阶段:组织学或细胞学确认、经标准治疗失败、不可切除或转移性晚期胃腺癌和食管胃交界部腺癌受试者;CLDN18.2蛋白阳性(中心实验室IHC检测≥40%的肿瘤细胞CLDN18.2膜染色≥2+)。
5、预计生存时间3个月以上。
6、至少有一个可测量的肿瘤病灶(根据RECIST1.1标准)。
7、ECOG体力评分0-1分(附录1)。
8、有足够的器官功能,首次给药前7天内的实验室检查值满足以下要求(检查前14天内未输血及血制品、未使用粒细胞集落刺激因子[G-CSF]及其他造血刺激因子、未使用保肝药或其他医学支持疗法):
a)血常规:NEUT≥1.5×109/L,PLT≥80×109/L,Hb≥80g/L;
b)肝功能:TBIL≤1.5×ULN,ALT≤2.5×ULN,AST≤2.5×ULN(肝转移患者ALT≤5×ULN,AST≤5×ULN);
c)肾功能:Cr≤1.5×ULN或肌酐清除率≥50ml/min(Cockcroft-Gault公式计算,附录2);
d)凝血功能:活化部分凝血活酶时间(APTT)≤1.5×ULN,凝血酶原时间(PT)≤1.5×ULN或国际标准化比值(INR)≤1.5×ULN。
9、有生育能力的受试者(男性和女性)必须同意在试验治疗期间和末次用药后至少9个月内使用可靠的避孕方法(激素或屏障法或禁欲)。
排除标准
排除标准
1、首次使用研究药物前4周内接受过抗肿瘤治疗(包括化疗、放疗、靶向治疗等)。
2、已知对BC008任何成分有过敏史。
3、既往接受过任何靶向CLDN18.2的治疗。
4、维生素K拮抗剂与抗凝剂同时给药,或给予治疗剂量的肝素(可以接受预防剂量)。
5、存在胃幽门梗阻或持续反复呕吐(24小时呕吐≥3次)。
6、存在未经治疗或未控制的消化性溃疡。
7、根据研究者的判断,有无法控制的或严重的消化道出血或消化道穿孔风险。
8、首次给药前4周内接受过主要脏器外科手术(穿刺活检/引流、静脉置管除外)或出现过严重外伤。
9、存在需要局部治疗或者反复引流的、研究者判断控制不良的体腔积液(胸水、腹水、心包积液等)。
10、既往抗肿瘤治疗的不良反应尚未恢复到NCICTCAE5.0等级评价≤1级(脱发除外)。
11、具有临床症状的脑转移、脊髓压迫、癌性脑膜炎,或有其他证据表明患者脑、脊髓转移灶尚未控制,经研究者判断不适合入组。
12、有需要治疗的活动性感染或首次使用研究药物前2周内使用过全身性抗感染药物。
13、患有活动性、或有病史且有可能复发的自身免疫性疾病的受试者(如:全身性红斑狼疮、类风湿性关节炎、溃疡性结肠炎、克罗恩病、自身免疫性甲状腺疾病、多发性硬化,血管炎、肾小球肾炎等,包括但不限于这些疾病或综合症);
但允许患以下疾病的受试者入组:
a)采用固定剂量的胰岛素后病情稳定的I型糖尿病患者;
b)只需接受甲状腺素替代治疗的自身免疫性甲状腺功能减退症;
c)无需进行全身治疗的皮肤疾病(如湿疹,占体表10%以下的皮疹,无眼科症状的银屑病等)。
14、首次给药前14天内接受过全身使用的皮质类固醇(强的松>10mg/天或等价剂量的同类药物)的患者;以下情况除外:使用局部、眼部、关节腔内、鼻内和吸入型皮质类固醇治疗,短期(≤3天)使用皮质类固醇进行预防治疗(如使用造影剂前的预处理)。
15、过去五年内有其他恶性肿瘤病史(既往接受根治治疗且未复发的皮肤基底细胞癌、皮肤鳞状细胞癌、浅表性膀胱癌、宫颈原位癌或其他原位癌除外)。
16、有器官移植史或异基因骨髓移植史或干细胞移植史。
17、活动性乙型肝炎或丙型肝炎,活动性乙型肝炎定义为乙肝表面抗原(HBsAg)阳性且HBVDNA>正常值上限,活动性丙型肝炎定义为丙肝抗体(HCV-Ab)阳性且HCVRNA>正常值上限;。
18、有免疫缺陷病史,包括人类免疫缺陷病毒(HIV)抗体检测阳性。
19、有严重的心脑血管疾病史,包括但不限于:需要临床干预的室性心律失常;首次使用研究药物前6个月内的急性冠脉综合征、脑卒中或短暂性脑缺血发作;满足美国纽约心脏病协会(NYHA)心功能分级≥II级的充血性心力衰竭。
20、已知有精神类药物滥用、酗酒或吸毒史。
21、妊娠(具有生育能力的女性患者根据首次给药前7天内的血清妊娠试验确定)或哺乳期女性。
22、首次给药前4周内或计划在研究治疗期间接受活疫苗或减毒疫苗。
23、研究者认为可能影响受试者参与整个研究、增加受试者风险、或混淆研究结果的任何疾病、治疗或实验室检查异常,或者研究者认为参与研究不符合受试者的最佳利益。









![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




