【临床试验招募】HWH340临床试验
招募标准
HWH340临床试验,HWH340片晚期实体瘤I期耐受性和药代动力学研究
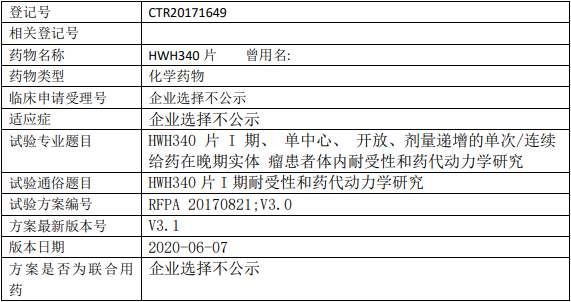
1、试验目的
1.观察单次和连续口服不同剂量 HWH340 片在患者体内的安全性和耐受性,探索最大耐受剂量( MTD)
2.考察单次和连续口服 HWH340 片在患者体内的药代动力学特征
3.初步观察口服 HWH340 片抗肿瘤的疗效。
4.初步探索口服 HWH340片体内代谢产物情况
2、试验设计
试验分类:其他其他说明:安全性/药代动力学/药效动力学试验
试验分期:I 期
设计类型:单臂试验
随机化:非随机化
盲法:开放
试验范围:国内试验
3、受试者信息
年龄:18 岁(最小年龄)至 70 岁(最大年龄)
性别:男+女
健康受试者:无
入排标准
入选标准
1.经组织学和/或细胞学确诊的晚期的实体瘤患者
2.经常规治疗无效或缺乏有效治疗的晚期实体瘤患者
3.剂量扩展阶段受试者还需满足以下条件:
小组 1:体系或胚系BRCA1 或 BRCA2 基因突变,可以提供用于体系或胚系 BRCA 基因检测的血样 4mL 和/或足够的肿瘤组织样本;
小组 2:存在除 BRCA1或 BRCA2 基因以外的其他胚系或体系 HRD 相关基因突变;可以提供用于体系或胚系HRD相关基因检测的血样4mL和/或用于生物标志物分析所需的足够的肿瘤组织样本;既往阳性报告经评估后可作为阳性筛选依据;若为乳腺癌患者,需要经组织学或细胞学证实的 HER2(-);既往曾接受 ≤3 线用于晚期或转移性疾病的化疗
4.年龄大于等于 18 岁, 小于等于 70 岁
5.预计生存期≥6 个月
6.无严重的造血功能异常,心、肺、肝、肾等器官和骨髓功能基本正常,给药前 14 天内,扩展期患者为给药前 7 天内,实验室数值在下列范围内(未使用造血细胞生长因子或输血的状态下):
血常规:中性粒细胞绝对数(ANC)≥1.5×109/L,血小板(PLT)≥100×109/L,血红蛋白(Hb)≥100 g/L;
肾功能:血清肌酐(Cr)≤1.5×ULN;
肝功能:血清总胆红素≤1.5×ULN, 天冬氨酸转氨酶(AST)及丙氨酸转氨酶(ALT)≤2.5×ULN(如果肿瘤有肝脏转移,则≤ 5×ULN);
凝血功能:国际标准化比率(INR)≤1.5,活化部分凝血活酶时间(APTT)≤1.5×ULN
7.有生育潜能的受试者必须同意在研究期间及末次给药后 6 个月内采取医学认可的两种有效的避孕措施,在给药前 7 天内的血清妊娠试验必须为阴性
8.对本研究已充分了解,自愿签署知情同意书, 能够遵循研究的操作程序及随访检查要求,并同意进行相关基因检测
9.参加连续给药/剂量扩展试验受试者肿瘤协作组评分 ECOG 评分≤2
10.参加连续给药/剂量扩展试验受试者必须至少有一个根据RECIST V1.1 版标准定义的可测量的病灶
排除标准
排除标准
1.除肿瘤外,合并其他严重的和(或)无法控制的重要脏器或不稳定的系统性疾病,包括但不限于未控制的糖尿病,不稳定型心绞痛,脑血管意外或短暂性脑缺血(筛选前 6 个月内),心肌梗死(筛选前 6 个月内),严重的充血性心力衰竭,未控制的高血压,无法控制的活动性感染,肝脏、肾脏或其他严重代谢性疾病,严重胃肠道疾病,有影响遵循研究程序能力的任何精神疾病
2. 任何之前接受 PARP 抑制剂治疗,包括相关药物临床试验(本试验药物除外);剂量扩展阶段受试者,既往接受过 PARP 抑制剂(包括药物临床试验),但使用 PARP 抑制剂未达治疗剂量,或使用≤28 天且不是最近一线治疗的患者除外
3. 2 周内接受 CYP3A4 和/或 CYP2D6 抑制剂患者
4. 在首次给药前 4 周内接受过手术、化疗、放射治疗、内分泌治疗、靶向治疗、生物治疗、免疫治疗、抗肿瘤中草药治疗或其他抗肿瘤治疗者;剂量扩展阶段受试者在入组前已开始双膦酸盐或RANK - L 抑制剂治疗骨转移,且剂量保持稳定者除外
5. 在进入研究前 3 周内参加过其他临床试验或使用过其他研究药物者
6. 有自身免疫性疾病、免疫缺陷疾病,或有器官移植史者
7. 乙肝表面抗原(HBsAg)阳性,丙型肝炎病毒(HCV)抗体阳性,人体免疫缺陷病毒(HIV)抗体阳性,或梅毒检测阳性
8. 有由前期治疗引起的持续存在的毒性反应(≥CTCAE 2 级),除外不存在安全性风险的 AE,如脱发,特定的实验室检查异常
9. 在进入研究前 4 周内进行过重大手术
10. 已知对研究药物或同类药物过敏
11. 有酗酒或药物滥用史
12. 妊娠或哺乳期女性,或准备在研究期间妊娠或哺乳的女性
13. 有症状的中枢神经系统转移
14. 无法吞服口服制剂和/或胃肠功能紊乱的患者可能会干扰研究药物的吸收
15. 研究前 4 周内接受过输血
16. 研究者认为不合适入组的情况
研究者信息
1、主要研究者信息
姓名:佟仲生
学位:医学硕士
职称:主任医师
单位名称:天津市肿瘤医院
2、各参加机构信息
| 序号 | 机构名称 | (主要)研究者 | 国家 | 省(州)-城市 |
| 1 | 天津市肿瘤医院 | 佟仲生 | 中国 | 天津市 -天津市 |
| 2 | 南昌市第一医院 | 章卫华 | 中国 | 江西省 -南昌市 |
| 3 | 中国医科大学附属第一医院 | 刘云鹏 | 中国 | 辽宁省 -沈阳市 |
| 4 | 辽宁省肿瘤医院 | 孙涛 | 中国 | 辽宁省 -沈阳市 |
| 5 | 河北医科大学第四附属医院 | 耿翠芝 | 中国 | 河北省 -石家庄市 |
| 6 | 四川大学华西医院 | 罗婷 | 中国 | 四川省 -成都市 |
| 7 | 湖南省肿瘤医院 | 欧阳取长 | 中国 | 湖南省 -长沙市 |
| 8 | 华中科技大学同济医学院附属协和医院 | 董晓荣 | 中国 | 湖北省 -武汉市 |
| 9 | 湖北省肿瘤医院 | 徐慧婷 | 中国 | 湖北省 -武汉市 |
| 10 | 宜春市人民医院 | 陈金平 | 中国 | 江西省 -宜春市 |
| 11 | 河北大学附属医院 | 臧爱民 | 中国 | 河北省 -保定市 |
| 12 | 沧州市人民医院 | 王淑梅、石金升 | 中国 | 河北省 -沧州市 |
| 13 | 粤北人民医院 | 雷睿文 | 中国 | 广东省 -韶关市 |
| 14 | 九江市第一人民医院 | 曾录芝 | 中国 | 江西省 -九江市 |
| 15 | 南昌大学第四附属医院 | 周荣伟 | 中国 | 江西省 -南昌市 |
| 16 | 北京大学第三医院 | 王墨培 | 中国 | 北京市 -北京市 |
| 17 | 南昌市第三医院 | 王红 | 中国 | 江西省 -南昌市 |
| 18 | 浙江省肿瘤医院 | 王晓稼 | 中国 | 浙江省 -杭州市 |
| 19 | 西南医科大学附属医院 | 何丽佳 | 中国 | 四川省 -泸州市 |
| 20 | 北京大学首钢医院 | 莫雪莉、向平超 | 中国 | 北京市 -北京市 |








![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




