破解胃癌治疗困境,免疫治疗强势入局,拯救患者于“水火”
胃癌免疫疗法,胃癌免疫治疗药物,胃癌免疫治疗用什么药
胃癌是我国常见的恶性肿瘤,也继肺癌之后的第二大癌种,发病率和死亡率都高居恶性肿瘤排行榜前列,而且我国胃癌发病和死亡人数分别占全球44%和50%,约80%的中国胃癌患者确诊时已是晚期,即使接受了胃癌根治术,仍有超过一半的患者局部复发或远处转移,而发生转移的胃癌患者5年生存率不足10%。
在治疗方面,胃癌一线治疗仍以手术、放化疗为主,而临床获批靶向药物仅有为数不多的几种,势单力薄,对胃癌患者总生存期的改善差强人意。
一句话概括,中国胃癌治疗形势严峻!
二十一世纪,随着免疫疗法的兴起,各种免疫疗法也纷纷将矛头指向胃癌领域,意欲破解胃癌治疗的困境,拯救胃癌患者于水火。
免疫检查点抑制剂率先入围,全面冲击胃癌三线治疗
免疫检查点抑制剂可谓是最成功的免疫疗法之一,在多个癌种的治疗上均表现出优异的成绩,对于胃癌患者也不例外。在众多免疫疗法中,免疫检查点抑制剂率先入围,在胃癌三线治疗上均有不同成绩的表现。
晚期患者无药可解,免疫疗法在三线治疗中获益明显
K药(Keytruda,pembrolizumab,帕博利珠单抗)一马当先,首个获批胃癌三线治疗
2017 年 9 月 22 日,FDA 加速批准 pembrolizumab(KEYTRUDA,默沙东)用于局部复发性晚期或转移性胃癌或食管胃交界腺癌,适用于肿瘤表达 PD-L1 的患者。
此次批准基于 KEYNOTE 059(NCT02335411)的结果,这是一项开放式、多中心、非对照、多队列试验,该试验招募了 259 名胃癌或食管胃交界腺癌患者。在 259 名患者中,55%(n = 143)的患者肿瘤表达 PD-L1,并有微卫星稳定(MSS)或未确定微卫星不稳定(MSI)或错配修复(MMR)状态。患者接受pembrolizumab 200 mg,每3周重复。研究的中位随访时间为5.8个月。
结果显示,所有患者的总体有效率为11.6%,有42.4%的患者出现不同程度的肿瘤缩小,其中完全缓解达3%。
值得注意的是,在143位PD-L1阳性患者中,有效率为15.5%,而PD-L1阴性患者中有效率仅为6.4%。PD-L1阳性和阴性患者的6个月无进展生存期(PFS)率分别为18.2%和9.9%,6个月总生存期(OS)率分别为48.4%和42.9%。
O药(Opdivo,Nivolumab,纳武利尤单抗)奋力突围,奠定三线治疗地位
2020年3月,中国国家药品监督管理局(CFDA)正式批准欧狄沃(纳武利尤单抗)用于治疗既往接受过两种或两种以上全身性治疗方案的晚期或复发性胃或胃食管交界腺癌患者,使其成为中国首个胃癌免疫治疗药物。
此次获批是基于一项Ⅲ期临床试验研究ATTRACTION-2的结果,这是全球首个胃癌免疫治疗的Ⅲ期试验。该研究是目前样本量最大的一项对比纳武利尤单抗及安慰剂用于晚期胃癌后线治疗的随机、双盲、多中心III期研究。研究入组的患者均为亚洲人群,其中80%的胃癌入组患者接受过三线及以上治疗。
研究结论,与安慰剂组相比,纳武利尤单抗治疗,患者死亡风险显著降低38%,且无论PD-L1的表达如何,患者均可得到总生存期(OS)获益。2年随访结果显示,在所有493例入组患者中,纳武利尤单抗组与安慰剂组患者的中位OS时间分别为5.26个月和4.14个月;一年总生存率分别为27.3%和11.6%,翻了一倍多!两年总生存率分别为10.6%和3.2%,翻了三倍多!
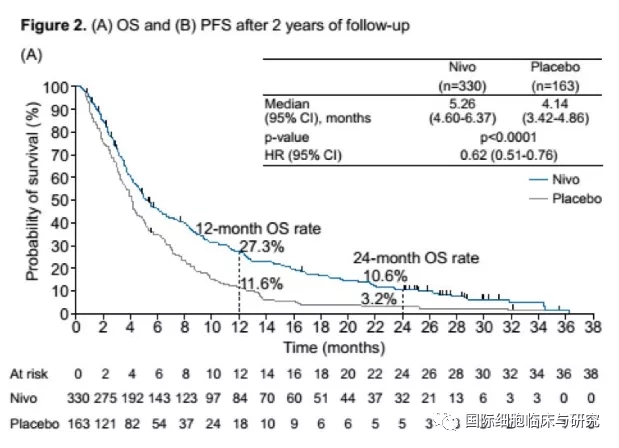
更为重要的是,亚组分析显示,患者1年总生存率为87.1%,2年总生存率61.3%。纳武利尤单抗治疗组完全缓解(CR)患者和部分缓解(PR)的患者平均总生存期随访2年尚未达到,而安慰剂组没有任何患者达到CR或PR。这对于以往生存期不足半年的晚期胃癌患者来说意义是巨大的。
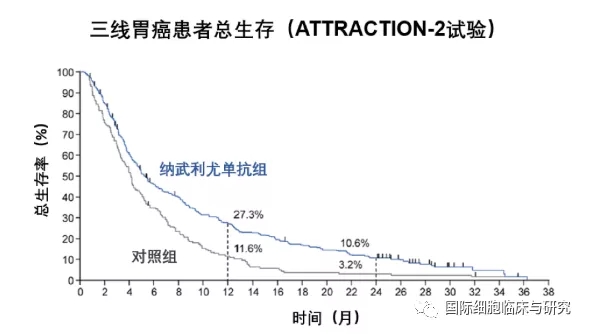
基于ATTRACTION-02的研究结果,日本、韩国、新加坡、中国台湾等地区也批准了纳武利尤单抗用于治疗化疗后进展的不可切除的晚期或者复发性胃癌。
自此,纳武利尤单抗基本奠定免疫疗法在胃癌三线治疗中的地位。
行路难,K药(帕博利珠单抗)率先试水胃癌二线治疗,收效惨淡
基于K药(Keytruda,pembrolizumab,帕博利珠单抗)获批用于胃癌的三线及以上治疗,KEYNOTE-061研究旨在探索Pembrolizumab用于晚期胃或胃食管结合部腺癌二线治疗的疗效与安全性。
该研究纳入的592位患者,其中有395位患者PD-L1表达CPS ≥1,随机分为免疫治疗组(n=196)和化疗组((n=199),中位随访时间为8个月。结果显示,免疫治疗组和化疗组的12个月总生存率为39.8%和27.1%,18个月为25.7%和14.8%。两组治疗之间的无进展生存期和客观反应率无明显差异。亚组分析中,PD-L表达CPS ≥5 和CPS≥10 的患者接受帕博利珠单抗治疗效果更好。
总体来说,帕博利珠单抗在胃-食管交界腺癌或PD-L1 CPS ≥1患者的二线治疗上较单纯紫杉醇化疗降低了18%的死亡风险,但无统计学意义;帕博利珠单抗较紫杉醇更具有临床安全性。
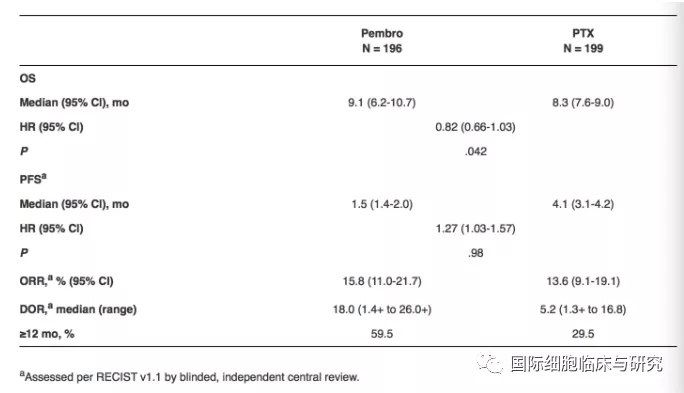
该试验的失败表明免疫疗法在胃癌的治疗上困难重重,仍需更进一步的研究。
而在早期的研究中,《NEJM) 杂志报道入组41例其他治疗失败的晚期实体瘤患者,MSI-H阳性与阴性分别接受PD-1抗体K药治疗进行对比。临床结果显示MSI-H阳性的患者,有效率是40%,20周的无疾病进展生存率是78%;而MSI-H阴性的患者,有效率是0%,20周的无疾病进展生存率是11%。
《science》 杂志报道:科学家招募86例MSI-H阳性的、来自12种癌症的患者PD-1抗体K药治疗。临床结果显示86例患者整体有效率53%,其中21%的患者完全缓解,77%的患者疾病控制。
正是基于以上临床数据,K药获得美国FDA加速批准用于MSI-H阳性的实体瘤,其中包括胃癌。
在最新版的美国NCCN指南中,针对晚期不可切除的胃癌患者,派姆单抗(K药)作为被美国FDA批准用于胃癌患者的药物,可用作MSI-H(微卫星高度不稳定性)或dMMR(错配修复缺陷)胃癌的二线治疗,以及PD-L1阳性联合分数(CPS)≥1的胃腺癌的三线治疗。
希望尤在,免疫疗法联合化疗或成未来一线治疗趋势
对于胃癌一线治疗,免疫疗法尚无突破。基于K药(Keytruda,pembrolizumab,帕博利珠单抗)获批的KEYNOTE-059研究分析,队列2和队列3纳入的是初治的复发或转移性胃和胃食管交界处腺癌患者,分别接受Pembrolizumab联合传统化疗(顺铂联合氟尿嘧啶类药物)和Pembrolizumab单药治疗。
队列2的患者不限制肿瘤中PD-L1的表达,而队列3仅纳入PD-L1阳性的患者。最终队列2招募了25例患者,总体客观缓解率(ORR)为60%,其中PD-L1阳性者为69%,而PD-L1阴性者也达到38%。中位无进展生存期(PFS)为6.6个月,中位总生存期(OS)为13.8个月。
队列3最终招募了31例患者,PD-L1阳性患者客观缓解率达26%,疾病控制率达36%,77%的患者肿瘤靶病灶有缩小,中位PFS为3.3个月,中位OS为20.7个月。
队列2中高达60%的有效率提示着Pembrolizumab在晚期胃癌中的应用还可以更加提前。基于KEYNOTE-059良好的试验数据,有研究者设计了帕博利珠单抗作为单药和联合化疗一线治疗PD-L1阳性胃或胃食管结合部癌的KEYNOTE-062研究。
结果显示,在PD-L1阳性联合分数(CPS)≥1的意向性治疗(ITT) 人群中,帕博利珠单抗单药治疗的总生存期(OS) 不劣于化疗,达到主要终点。然而,帕博利珠单抗联合化疗组的OS (CPS>1或CPS>10)和无进展生存期(PFS)(CPS>1)不优于化疗组。
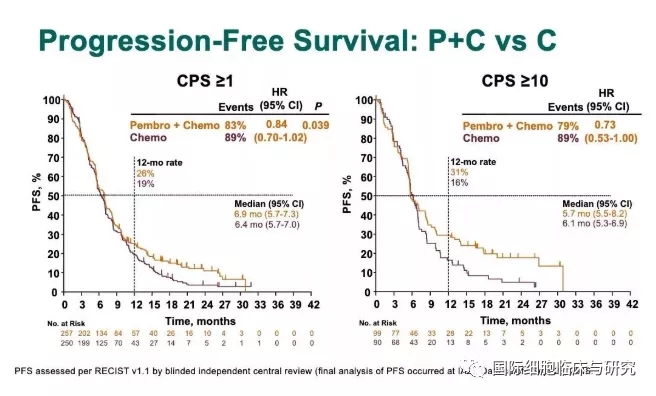
虽然,帕博利珠单抗在冲击胃癌一线治疗过程惨遭折戟,但试验也表明免疫治疗联合化疗也是未来一线和二线治疗的趋势所在。此外,对于PD-L1阴性或未检测的患者也可考虑采用免疫联合化疗来增加有效率。
过继性细胞疗法乘风破浪,表现不俗
过继性细胞疗法是肿瘤免疫治疗一个重要的分支,在推进免疫疗法的发展中做出了不可磨灭的贡献,尤其是嵌合抗原受体T细胞(CAR-T)疗法在血液肿瘤治疗中表现惊艳,成为唯一被FDA批准上市的细胞产品。随后,越来越多的过继性细胞疗法向实体瘤发起冲击,希望在实体瘤的治疗上一战成名。
随着免疫疗法在癌症治疗上不断传出利好消息,过继性细胞疗法乘借免疫治疗的东风,顺势而起。
入局胃癌,CAR-T疗法不负众望
在破解实体瘤的道路上,胃癌也成为CAR-T疗法的目标之一。
2020年5月27日,中国国家药品监督管理局(NMPA)官网显示,科济生物自主研发的靶向Claudin 18.2(CLDN18.2)的自体CAR-T疗法(CT041)的临床试验申请获得NMPA受理。Claudin 18.2(CLDN18.2)在胃腺癌、食管胃结合部癌、胰腺癌等多种肿瘤高表达,被认为是这些恶性肿瘤的治疗靶标。这款CAR-T疗法的新药临床试验(IND)申请也获得了美国FDA批准,用于治疗用于治疗晚期胃癌和胰腺癌。
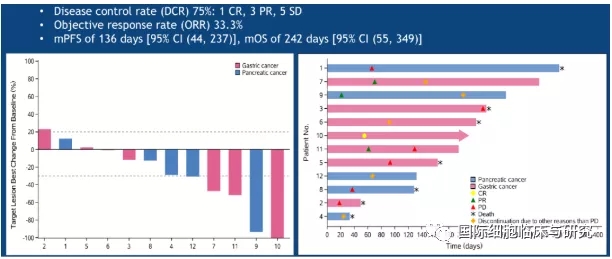
2019 ASCO年会上,靶向claudin18.2 CAR-T细胞疗法进行了数据更新,12例转移性腺癌(胃癌7例,胰腺癌5例),未发生严重不良事件、治疗相关死亡或严重神经毒性。11例评估对象中:1例(胃腺癌)完全缓解;3例(胃腺癌2例,胰腺癌1例)部分缓解;5例病情稳定;2例病情进展;总客观缓解率为33.3%。
并且,CAR-Claudin18.2 T 细胞治疗胃癌的临床前研究成果显示,靶向Claudin18.2的CAR-T细胞在小鼠模型中可以完全清除胃肿瘤,且没有发生脱靶毒性。
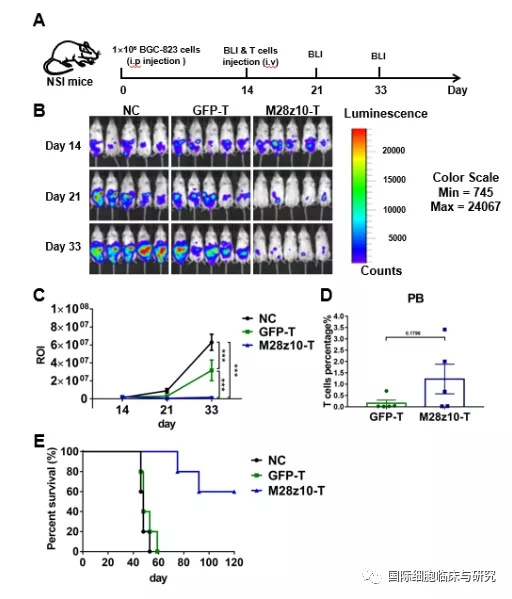
2019年2月18日,中国科学院广州生物医药与健康研究院研究人员在国际学术期刊《Journal of Hematology & Oncology》上发表了题为Mesothelin is a target of chimeric antigen receptor T cells for treating gastric cancer 的研究论文。该论文揭示了间皮素(MSLN, Mesothelin)可作为CAR-T治疗胃癌的有效新靶点。
靶向MSLN的第三代CAR-T——M28z10 T在与靶细胞共培养时展示出强大的靶向杀伤能力和细胞因子分泌能力。体内尾静脉模型和腹腔模型等多个模型表明,M28z10 T细胞能够明显抑制肿瘤的生长,甚至在部分小鼠体内达到完全清除肿瘤的效果,从而延长小鼠生存期。
该研究获得国家自然科学基金、中科院战略先导项目、广东省重大研究专项、广东省重大应用专项等的支持。
此外,在胃癌中刚刚开展多项临床研究,治疗靶点包括上皮细胞粘附分子(Epithelial cell adhesion molecule, EpCAM)、MUC1、HER-2、癌胚抗原(carcino-embryonicantigen,CEA)这几类肿瘤相关抗原,目前均处于临床研究招募阶段,效果需要进一步的数据证实。
TILs疗法用于晚期胃癌初见成效,但广泛应用受限
肿瘤浸润的淋巴细胞(TILs)是从患者肿瘤中分离出淋巴细胞,回输到患者体内。目前关于胃癌TILs治疗的研究不多。一项研究使用肿瘤浸润的淋巴细胞(TILs)联合或不联合化疗治疗44例晚期胃癌患者,结果显示与单纯化疗相比,TILs联合化疗治疗晚期胃癌患者可以使中位生存期从8.3个月延长至11.5个月。

但TILs获取困难,扩增耗时长,个体化难以大量生产等原因在临床上暂时未获得广泛应用。
CIK疗法助力胃癌常规治疗,疗效有待深挖
CIK是多种细胞因子共同诱导培养的细胞,包括CD3+ CD8+ CD56−的细胞到高度分化的CD56阳性的自然杀伤细胞(NK)、T细胞。这些细胞无论是有无抗体或组织相容性复合体(MHC),都能够识别肿瘤细胞,因此,他们可以识别缺失MHC的肿瘤细胞。
一项回顾性研究显示,对于进行胃癌根治术后的患者,辅助化疗联合CIK与单纯化疗相比,可使生存率、无进展生存期得到提高。

但这类细胞缺乏抗原特异性,不能特异杀伤肿瘤细胞。
肿瘤疫苗破局胃癌免疫疗法前景广阔、任重道远
肿瘤疫苗是将肿瘤抗原以多种形式导入患者体内,以克服肿瘤引起的免疫抑制,激活免疫反应,主要是激活针对肿瘤抗原的细胞毒性T淋巴细胞(CTL)杀伤肿瘤,从而起到抗肿瘤的效果。
肿瘤疫苗目前在胃癌中仅处于临床研究的阶段,研究所采用的抗原有多种形式,包括:黑色素瘤相关抗原MAGE-A3、HER2、VEGFR、白喉类毒素(G17DT)等。
有一项关于MAGE-A3/DC治疗晚期胃癌的临床研究,3例患者出现了一定程度的肿瘤缩小。

也有研究发现经过HER2/DC疫苗治疗后,HER2阳性的不可切除局部进展期和复发转移胃癌患者可获得一定的疾病控制。

还有研究表明,VEGFR多肽疫苗联合化疗治疗晚期胃癌患者,55%患者达部分缓解,联合治疗的耐受性较好。
一项多中心Ⅱ期临床研究应用G17DT 疫苗联合化疗治疗初治的晚期胃癌患者,结果显示,与未发生免疫应答的患者比较,成功接种并发生免疫应答的患者的疾病进展时间和中位生存时间均有所延长。

以上研究表明,肿瘤疫苗联合标准化疗治疗晚期胃癌的也许是一种较有前途的策略。但目前由于胃癌疫苗治疗的客观反应率较低,还需要进一步的研究明确如何筛选抗原,如何筛选人群,还有较长的路要走。
作为中国的第二大癌种,胃癌发病率高,死亡率高,临床治疗手段有限。目前化疗药遭遇瓶颈,靶向药治疗现状并不乐观,亟需新的疗法破解胃癌患者治疗困境。
免疫疗法的出现给胃癌患者带来新的生存希望,多种免疫疗法并行,有望改写胃癌治疗格局。我们期待免疫疗法再创佳绩,让胃癌的临床治疗翻开新的历史篇章。
参考资料:
1.https://mp.weixin.qq.com/s/StEJrO4lgA5BRZcnUSp5UA
2.https://mp.weixin.qq.com/s/0uKMgmOykvMmloqXn2XCeA
3.https://mp.weixin.qq.com/s/0vQTmLOK0wB3bsMr-IAQDw
4.https://mp.weixin.qq.com/s/0an0Qm6ZwlJFIZJzfnY6NQ
5.http://yao.dxy.cn/article/531580
6.http://www.360doc.com/content/19/0606/08/52645714_840711744.shtml
7.http://www.360doc.com/content/18/0202/00/46553095_727068615.shtml
8.https://mp.weixin.qq.com/s/-FrjejCMfv7z2ApZJIupvA
9.https://mp.weixin.qq.com/s/_oj4mH4033mBJKWgtr4ZXQ
10.https://mp.weixin.qq.com/s/OeZRiWHTmhGcT5YCqzm_7Q
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
里程碑!mRNA-4157联合派姆单抗让
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

刚刚!"双免王炸"纳
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2025肺癌生存新希望:六大"
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
早期甲状腺癌术后五年生存率超99%,但要
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
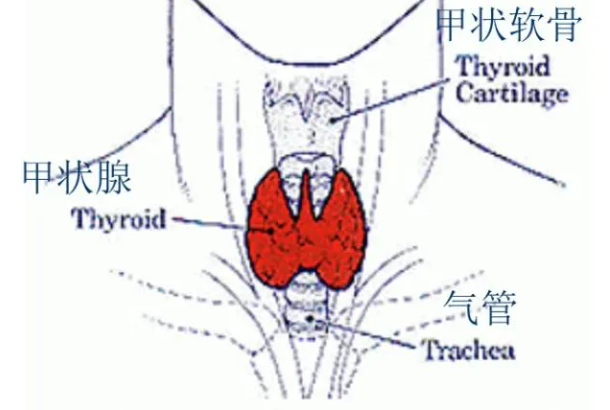
早期甲状腺癌术后五年生存率超99%!但忽
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




