救命药加速入场!2025第二季度9款抗癌新药即将入华,主攻肺癌、乳腺癌、卵巢癌等六大癌种
2025年第二季度9种抗癌新药有望在中国获批上市,主攻肺癌、乳腺癌、卵巢癌等六大癌种
近期,抗癌战场捷报频传,多款极具潜力的抗癌新药接连提交了上市申请。这也意味着,2025年第二季度,或将有一大批突破性的抗癌新药在国内成功获批,涵盖单抗、双抗、ADC类药物等多种类型!届时,这些新药将为无数在黑暗中苦苦等待的肿瘤患者带来曙光,改写抗癌的艰难战局!
小编争分夺秒,精心汇总了一份“2025年第二季度有望获批上市的抗癌新药榜单”,旨在帮助广大癌友坚定战胜癌症的信心!
抢鲜看!2025第二季度有望获批的抗癌新药大盘点
2025抗癌新药速览
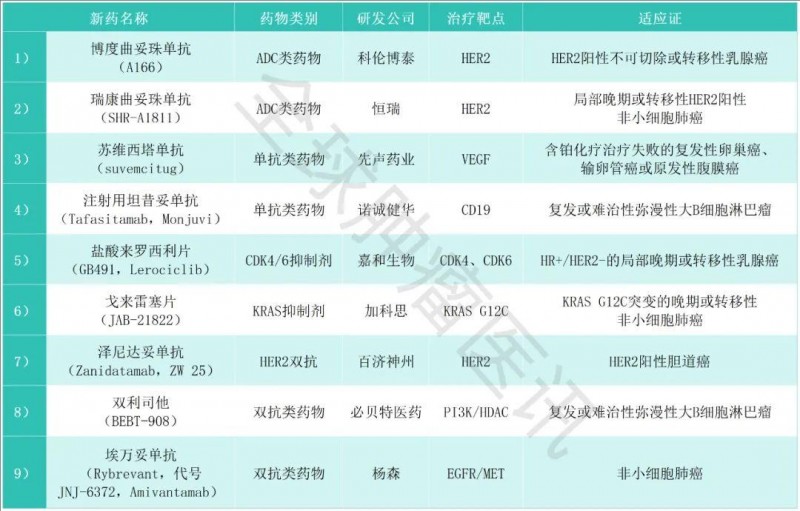
▲数据源自“NMPA”,医学部整理汇总
01、博度曲妥珠单抗
药品简介
①药物名称:博度曲妥珠单抗(A166)。
②研发公司:科伦博泰。
③治疗靶点:HER2。
④适应证:HER2阳性不可切除或转移性乳腺癌。
药物详情
2025年1月7日,博度曲妥珠单抗第二个适应证的新药上市申请(NDA),获得中国国家药品监督管理局药品评审中心受理,针对成人既往至少接受过一种抗HER2治疗的HER2阳性不可切除或转移性乳腺癌。
此前(2023年5月11日),该药的1类新药上市申请就已获得CDE的受理,拟用于既往经过二线及以上抗HER2治疗失败的HER2阳性不可切除的局部晚期、复发或转移性乳腺癌的治疗。
临床研究数据
本次获批申请基于多中心、随机、开放、对照的III期KL166-III-06临床研究,旨在评估博度曲妥珠单抗单药与恩美曲妥珠单抗(T-DM1),在既往接受过曲妥珠单抗和紫杉类治疗的HER2阳性不可切除或转移性乳腺癌患者中的疗效和安全性。预设的期中分析表明,相较于T-DM1,博度曲妥珠单抗单药在BICR(盲态独立中心评估)的无进展生存期(PFS)上,实现了具有显著统计学和临床意义的改善。
此外,在“博度曲妥珠单抗(A166)治疗经过二线及以上抗HER2治疗的HER2阳性乳腺癌”的Ⅰ期拓展研究中,也取得了优异成果:4.8mg/kg剂量组的客观缓解率(ORR)为73.9%(17/23),6.0mg/kg剂量组的ORR达68.6%(24/35)。
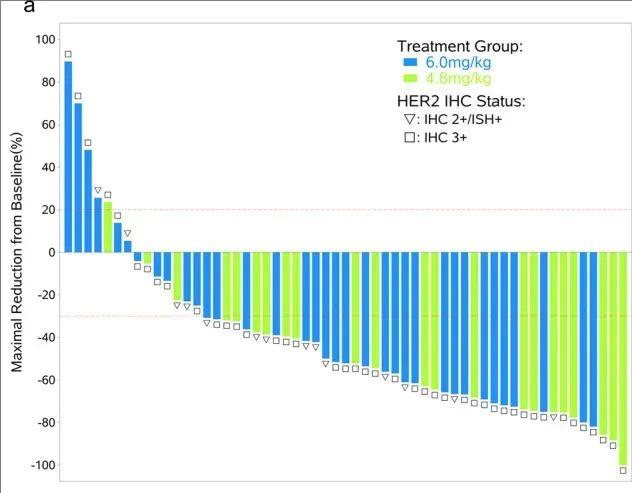
▲图源“NPJ Breast Cancer”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
02、瑞康曲妥珠单抗
药品简介
①药物名称:瑞康曲妥珠单抗(SHR-A1811)。
②研发公司:恒瑞。
③治疗靶点:HER2。
④适应证:局部晚期或转移性HER2阳性非小细胞肺癌(NSCLC)。
药物详情
瑞康曲妥珠单抗(SHR-A1811)作为一款靶向HER2的抗体偶联药物(ADC),在肿瘤治疗领域取得了重大突破。2024年9月13日,中国国家药品监督管理局药品审评中心(CDE)正式受理其上市许可申请,并将其纳入优先审评程序,适用于既往接受过至少一种系统治疗的局部晚期或转移性HER2阳性非小细胞肺癌(NSCLC)成年患者的治疗!它也成为了首个在国内申报治疗非小细胞肺癌的HER2ADC类药物,有望为肺癌治疗带来新的解决方案,填补临床空白。
临床研究数据
瑞康曲妥珠单抗的1/2期临床研究(NCT04818333),共入组63例既往接受过治疗的HER2突变的晚期非小细胞肺癌(NSCLC)患者,结果显示:全部入组患者中,24例患者达到部分缓解(PR),33例达到病情稳定(SD),客观缓解率(ORR)为38.1%(95% CI 26.1–51.2),疾病控制率(DCR)高达90.5%(95% CI 80.4–96.4)。
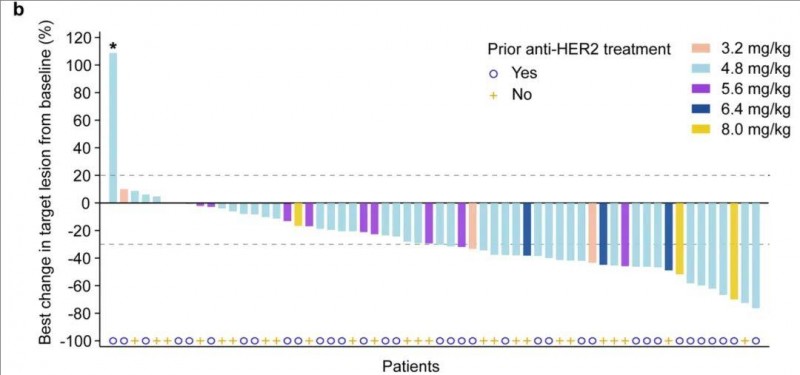
▲图源“nature”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
03、苏维西塔单抗
药品简介
①药物名称:苏维西塔单抗(suvemcitug)。
②研发公司:先声药业。
③治疗靶点:VEGF。
④适应证:含铂化疗治疗失败的复发性卵巢癌、输卵管癌或原发性腹膜癌。
药物详情
苏维西塔单抗(suvemcitug)属于新一代重组人源化抗VEGF兔源单克隆抗体。其作用机制在于,能高度选择性地与人体VEGF相结合,阻断VEGF的生物活性,从根源上减少肿瘤血管生成,进而抑制肿瘤的生长。2024年3月15日,中国国家药品监督管理局(NMPA)受理了注射用苏维西塔单抗的生物新药上市申请。若成功上市,它将用于联合化疗,为含铂化疗治疗失败的复发性卵巢癌、输卵管癌或原发性腹膜癌患者提供治疗方案。
临床研究数据
2024年美国临床肿瘤学会(ASCO)年会上,公布了苏维西塔单抗对照Ⅲ期SCORES临床试验(NCT04908787)的数据。该试验共纳入421例含铂化疗方案治疗失败的复发性上皮卵巢癌、输卵管癌和原发性腹膜癌患者。对苏维西塔单抗组和安慰剂组进行观察,两组的中位随访期分别为14.36个月和14.26个月。
结果显示:经盲态独立审查委员会(BIRC)评估,苏维西塔单抗组中位无进展生存期(PFS)达到5.49个月,而安慰剂组仅为2.73个月[风险比(HR)0.46,P<0.0001]。在客观缓解率(ORR)方面,BIRC评估结果显示,苏维西塔单抗组为26.0%,安慰剂组为12.1%;研究者评估的结果为,苏维西塔单抗组ORR为23.1%,而安慰剂组仅为8.6%。这表明,苏维西塔单抗在治疗含铂化疗治疗失败的复发性卵巢癌等癌症上具有显著效果。
04、坦昔妥单抗
药品简介
①药物名称:注射用坦昔妥单抗(Tafasitamab,Monjuvi)。
②研发公司:诺诚健华。
③治疗靶点:CD19。
④适应证:复发或难治性弥漫性大B细胞淋巴瘤。
药物详情
注射用坦昔妥单抗(Tafasitamab)是一款CD19单抗,可通过免疫效应机制、细胞凋亡,介导B细胞肿瘤的裂解。2024年6月3日,该药被中国NMPA纳入拟优先审评,与来那度胺联合,用于成人复发或难治性且不适合自体干细胞移植(ASCT)的弥漫性大B细胞淋巴瘤(DLBCL)的治疗。
值得一提的是,Tafasitamab联合来那度胺,早在2022年12月28日就已获得香港卫生署批准,用于不适合自体干细胞移植的复发/难治性弥漫性大B细胞淋巴瘤(DLBCL)成人患者的治疗。此前(2020年8月)该药还曾获得美国FDA加速获批上市,用于复发或难治性(R/R)弥漫性大B细胞淋巴瘤(DLBCL)的治疗,它也是美国首个获批的针对DLBCL的二线及二线以上疗法!
临床研究数据
坦昔妥单抗与来那度胺联合,治疗复发/难治性DLBCL的5年随访数据显示,总缓解率(ORR)达到57.5%,完全缓解率(CR)高达41.2%。中位总生存期(OS)为33.5个月,中位无进展生存期为(PFS)为11.6个月。
05、盐酸来罗西利片
药品简介
①药物名称:盐酸来罗西利片(GB491,Lerociclib)。
②研发公司:嘉和生物。
③治疗靶点:CDK4、CDK6。
④适应证:HR+/HER2-的局部晚期或转移性乳腺癌。
药物详情
盐酸来罗西利片(GB491,Lerociclib)是一款高选择性口服型CDK4/6抑制剂,对CDK4和CDK6具有高度选择性和强效性,但对CDK9仅具有中度抑制作用。2024年3月13日,中国国家药品监督管理局(NMPA)已正式受理盐酸来罗西利片的新药上市许可申请,与来曲唑联合,用于既往未经过系统性抗肿瘤治疗的激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性(HR+/HER2-)晚期乳腺癌的治疗。
临床研究数据
盐酸来罗西利片(GB491,Lerociclib)的LEONARDA-1 III期临床研究,共入组275例既往接受内分泌治疗后疾病进展的HR+/HER2-复发或转移性乳腺癌患者,结果显示:研究者评估的无进展生存期(PFS)显著改善,盐酸来罗西利片(Lerociclib)组的中位无进展生存期(PFS)为11个月,而安慰剂组仅为5.5个月。
06、戈来雷塞片
药品简介
①药物名称:戈来雷塞片(JAB-21822)。
②研发公司:加科思。
③治疗靶点:KRAS G12C。
④适应证:KRAS G12C突变的晚期或转移性非小细胞肺癌。
药物详情
JAB-21822是加科思自主研发的KRAS G12C抑制剂,2024年5月22日,中国CDE受理了该药的上市申请,并将其纳入优先审评程序,用于≥二线KRAS G12C突变的晚期或转移性非小细胞肺癌(NSCLC)的治疗。
临床研究数据
2022年ASCO大会上同步了该药的1期临床数据,本次共入组72例晚期实体瘤患者,在32例可评估疗效的KRAS G12C突变非小细胞肺癌患者中,客观缓解率(ORR)为56.3%(18/32),疾病控制率(DCR)为90.6%(29/32)。
07、泽尼达妥单抗
药品简介
①药物名称:泽尼达妥单抗(Zanidatamab,ZW 25)。
②研发公司:百济神州。
③治疗靶点:HER2。
④适应证:HER2阳性胆道癌。
药物详情
泽尼达妥单抗(Zanidatamab)是一款针对HER2的双特异性抗体,2024年6月7日,该药的上市申请获中国国家药品监督管理局(CDE)受理并纳入优先审评,用于HER2阳性胆道癌患者的二线治疗。此前(2024年11月)该药还曾获得美国FDA加速批准,用于经治、不可切除、局部晚期或转移性HER2阳性胆道癌的治疗,它是首个获FDA批准用于治疗HER2阳性局部晚期或转移性胆道癌的HER2靶向药!
临床研究数据
泽尼达妥单抗本次生物制品许可申请(BLA),得到了2b期HERIZON-BTC-01(NCT04466891)临床研究数据的支持。结果显示:在队列1(n=80)中,独立中央审查(ICR)评估的客观缓解率(ORR)为41.3,中位缓解持续时间(DOR)长达12.9个月。
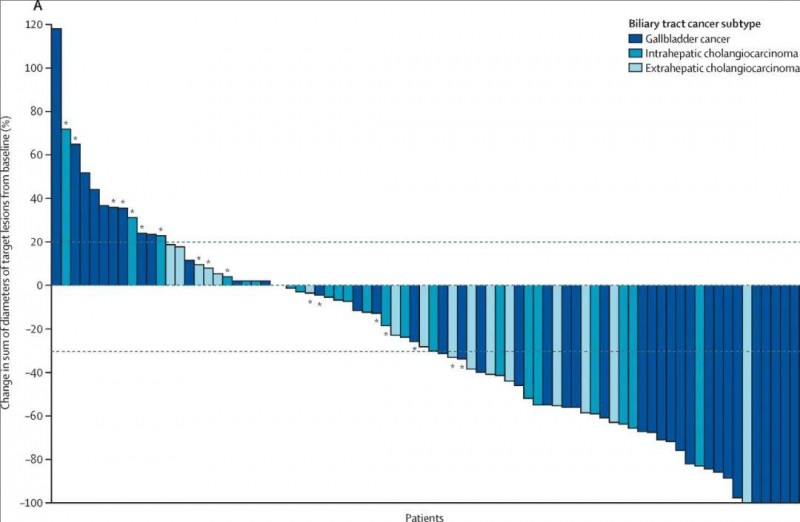
▲图源“THE LANCET”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
08、双利司他
药品简介
①药物名称:双利司他(BEBT-908)。
②研发公司:必贝特医药。
③治疗靶点:PI3K/HDAC。
④适应证:复发或难治性弥漫性大B细胞淋巴瘤。
药物详情
双利司他是一款同时靶向PI3K和HDAC的双靶点抗肿瘤新药。2023年10月9日,中国CDE受理了该药的上市申请,用于成人既往接受过≥2种系统治疗的复发或难治性弥漫性大B细胞淋巴瘤(DLBCL)的治疗。它也成为了全球首个申报新药上市申请(NDA)的PI3K/HDAC双靶点抑制剂。
临床研究数据
双利司他的IIb期关键临床试验(CTR20200035),共纳入93例复发或难治弥漫性大B细胞淋巴瘤(r/rDLBCL)患者,结果显示可显著延长患者的总生存期。
09、埃万妥单抗
药品简介
①药物名称:埃万妥单抗(Amivantamab,Rybrevant,代号JNJ-6372)。
②研发公司:杨森。
③治疗靶点:EGFR/MET。
④适应证:非小细胞肺癌。
药物详情
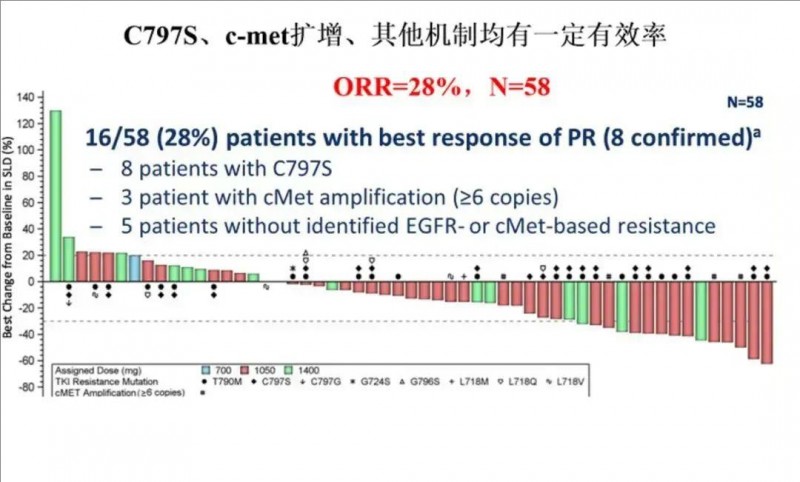
埃万妥单抗是一款c-Met/EGFR(EGFR间充质-上皮转化因子)双特异性抗体,2025年将有至少3个适应症在国内获批:①单药治疗非小细胞肺癌;②联合化疗治疗非小细胞肺癌;③联合兰泽替尼作为EGFR敏感突变的局部晚期或转移的非小细胞肺癌的一线治疗等。此前该药的静脉注射剂型已在欧美、日本等国获批上市,它也成为了全球首个获批的c-Met/EGFR双抗类药物。
临床研究数据
在一项开放标签,多中心1期临床研究中,埃万妥单抗(JNJ-6372)对复发性EGFR突变和EGFR外显子20插入的患者产生了初步反应。结果显示:在88位可评估反应的患者中,有28%达到了部分缓解(PR)。
小编寄语
上文所提及的新药/新技术,不过是众多研发热潮中的冰山一角,实际上还有众多在研的抗癌新药/新技术正在如火如荼地进行中,为广大癌症患者带来了新的希望和更有效的治疗选择。我们也期待这些新药能够顺利通过评审,尽快应用于临床实践,让更多的癌症患者有药可医!
好消息是,当前有多款在研药物已经陆续开启临床试验阶段,这也意味着中国患者将有获得最新抗癌药物免费治疗的机会。与此同时,“方舟援助计划”也可为患者提供已上市/未上市抗癌新药免费治疗的机会。对现有治疗方案不满意或耐药的患者,可将近期病理及影像学检查报告、治疗经历等资料,汇总并提交至全球肿瘤医生网医学部,进行初步评估或了解详细的入排标准。
参考资料
[1]Li Z,et al.SHR-A1811 (antibody-drug conjugate) in advanced HER2-mutant non-small cell lung cancer: a multicenter, open-label, phase 1/2 study[J]. Signal Transduction and Targeted Therapy, 2024, 9(1): 182.
https://www.nature.com/articles/s41392-024-01897-y
[2]Zhang J,et al.Phase I study of A166, an antibody‒drug conjugate in advanced HER2-expressing solid tumours. NPJ Breast Cancer. 2023 Apr 18;9(1):28.
https://pmc.ncbi.nlm.nih.gov/articles/PMC10113253/
[3]Harding J J,et al.Zanidatamab for HER2-amplified, unresectable, locally advanced or linkstatic biliary tract cancer (HERIZON-BTC-01): a multicentre, single-arm, phase 2b study[J]. The Lancet Oncology, 2023, 24(7): 772-782.
https://www.thelancet.com/journals/lanonc/article/PIIS1470-2045(23)00242-5/abstract
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
早期膀胱癌术后五年生存率高达90%,这五
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

警惕!乳腺癌复发偏爱这3大人群!术后一定
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【实体瘤溶溜病毒免费招募】溶瘤病毒Ml(
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
从多处转移到完全缓解!新型CAR-T细胞
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

救命药加速入场!2025第二季度9款抗癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




