国内首款!第三代高选择性PI3Kα抑制剂-伊那利塞片在华获批,填补晚期乳腺癌无药可用困境!
2025年3月11日国家药监局批准PI3Kα抑制剂伊那利塞片(Inavolisib、Itovebi、GDC-0077)用于乳腺癌
2025年3月11日,抗癌圈再次传来一个好消息,中国国家药品监督管理局(NMPA)批准了伊那利塞片的上市申请,该药与哌柏西利+氟维司群联合,用于内分泌治疗耐药(包括在辅助内分泌治疗期间或之后出现复发)、PIK3CA突变、HR(激素受体)阳性、HER2(人表皮生长因子受体2)阴性的局部晚期或转移性乳腺癌成人患者的治疗。
值得一提的是,伊那利塞片是中国首个获批的第三代高选择性PI3Kα抑制剂,填补了HR+/HER2-晚期乳腺癌精准治疗的空白。同时,也是首个获得中美双重突破性疗法认证的HR+乳腺癌治疗产品,具有里程碑氏的重要意义!

▲截图源自“NMPA”
首个第三代高选择性PI3Kα抑制剂—伊那利塞片,在中国成功获批!填补乳腺癌治疗空白
伊那利塞片(Inavolisib,Itovebi,GDC-0077)是由罗氏公司研发的一款高选择性PI3Kα抑制剂,它能够抑制磷脂酰肌醇3-激酶复合物(由PIK3CA编码)的p110催化亚基的α异构体,同时促进突变p110α的降解。
2024年4月,被中国国家药品监督管理局(CDE)纳入优先审评,拟用于标准内分泌治疗失败后的PIK3CA基因突变内分泌型乳腺癌。此前(2024年10月10日)伊那利塞片已获美国FDA批准,与哌柏西利+氟维司群联合,用于成人在完成辅助内分泌治疗期间或之后出现复发的PIK3CA突变、激素受体(HR)阳性、人类表皮生长因子受体2(HER2)阴性、局部晚期或转移性乳腺癌的治疗,该药也成为了在HR+乳腺癌治疗领域,首个获得中美双重突破性疗法认证的药品!
值得欣慰的是,历经38年的研发突破,如今(2025年3月11日)终于迎来了伊那利塞片在中国获批上市的好消息!它也成为了首个获批的第三代高选择性PI3Kα抑制剂,填补了HR+/HER2-晚期乳腺癌精准治疗空白,为这类患者带来了新的曙光!
伊那利塞片填补PIK3CA突变晚期乳腺癌的治疗空白,1年总生存率高达85.9%
伊那利塞片本次获批,主要是基于一项3期INAVO120临床研究(NCT04191499)的惊艳数据。本次研究共入组325例PIK3CA突变的晚期乳腺癌患者,将其分为两组,即Inavolisib组(即伊那利塞片组,161例)、安慰剂组(164例)。中位随访时间分别为21.3个月、21.5个月。
结果显示:Inavolisib(伊那利塞片)组的客观缓解率(ORR)高达58.4%,而安慰剂组仅为25.0%。换言之,与安慰剂组相比,接受伊那利塞片治疗组的患者,其客观缓解率足足提高了33.4个百分点(详见下图)。
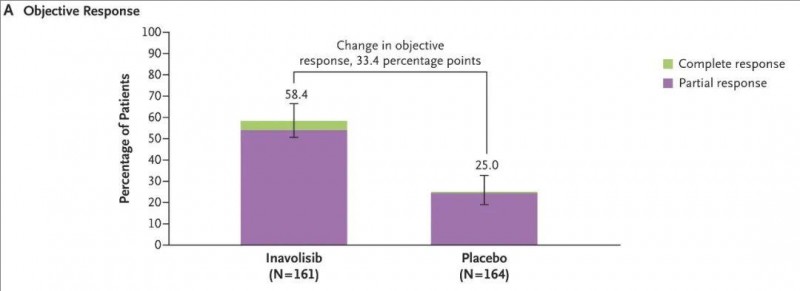
▲图源“N Engl J Med”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
此外,Inavolisib将患者的中位无进展生存期(PFS)提高近一倍,分别为15.0个月(Inavolisib组) vs 7.3个月(安慰剂组)(详见下图)。
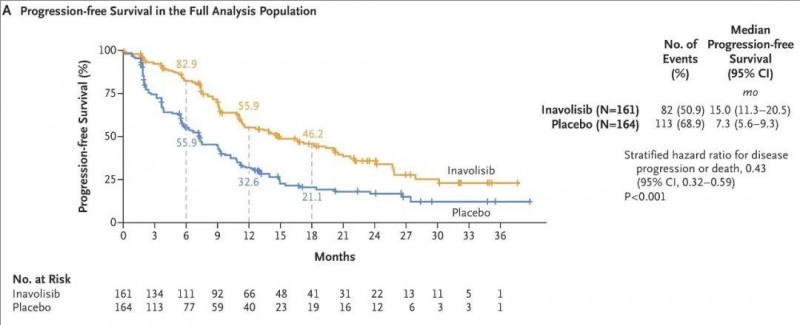
▲图源“N Engl J Med”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
在总生存期中期分析显示:6个月的总生存(OS)率分别为97.3%(Inavolisib组) vs 89.9%(安慰剂组);12个月的OS率分别为85.9%(Inavolisib组) vs 74.9%(安慰剂组);18个月的OS率分别为73.7%(Inavolisib组) vs 67.5%(安慰剂组)(详见下图)。
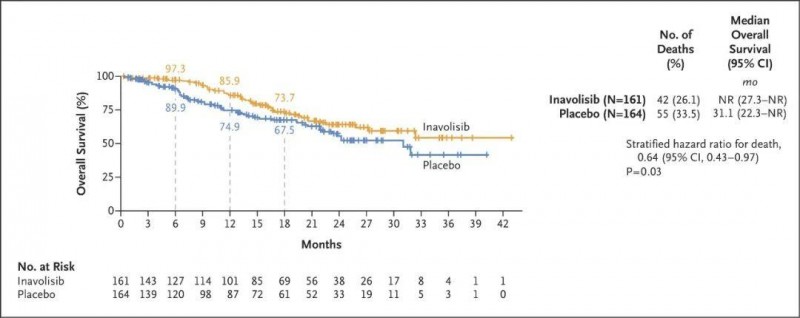
▲图源“N Engl J Med”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
小编寄语
除了上文所提及的伊那利塞片外,我国还有众多针对乳腺癌的抗癌新药/新技术正在如火如荼地研究中,为广大癌症患者带来了新的希望和更有效的治疗选择。我们也期待这些新药能够顺利通过评审,尽快应用于临床实践,让更多的癌症患者有药可医!
好消息是,当前有多款在研药物已经陆续开启临床试验阶段,这也意味着中国患者将有获得最新抗癌药物免费治疗的机会。与此同时,“方舟援助计划”也可为患者提供已上市/未上市抗癌新药免费治疗的机会。对现有治疗方案不满意或耐药的患者,可将近期病理及影像学检查报告、治疗经历等资料,汇总并提交至全球肿瘤医生网医学部,进行初步评估或了解详细的入排标准。
参考资料
[1]Turner N C,et al.Inavolisib-based therapy in PIK3CA-mutated advanced breast cancer[J]. New England Journal of Medicine, 2024, 391(17): 1584-1596.
https://www.nejm.org/doi/full/10.1056/NEJMoa2404625
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
里程碑!mRNA-4157联合派姆单抗让
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

刚刚!"双免王炸"纳
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2025肺癌生存新希望:六大"
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
早期甲状腺癌术后五年生存率超99%,但要
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
早期甲状腺癌术后五年生存率超99%!但忽
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
2025年四款肺癌疫苗震撼登场!打一针治
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05








![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




