2023年FDA批准37款抗癌新药,覆盖肺癌乳腺癌等十大癌症!
2023年美国抗癌新药,38款抗肿瘤新药覆盖肺癌、乳腺癌等十大癌症
近40款肿瘤新药新疗法获批,为2023年画上圆满的句号。
2023年,国内和国际上的抗癌新药井喷上市,FDA批准了共37款抗癌新疗法,包括靶向,免疫检查点抑制剂,过继性细胞免疫疗法等等,覆盖了常见的实体瘤及血液肿瘤类型。
全球肿瘤医生网医学部每年年中和年终都会参照美国FDA官网及美国国家癌症研究院的药品获批信息,为大家整理更新所有癌症获批的靶向药物,给大家带来战胜癌症的信心。(以下获批信息按时间排序,仅供参考,具体的用药方案需遵医嘱,也可致电全球肿瘤医生网医学部)。
2023年美国上市的抗癌新药
01、结直肠癌--图卡替尼
全球首款靶向HER2结直肠癌的重磅新药获批
药品信息
药物名称:tucatinib(图卡替尼)
研发公司:Seagen
上市时间:2023年1月19日
药物介绍:图卡替尼是一种口服小分子HER2抑制剂,在表达HER2的肿瘤细胞中显示出抗肿瘤活性,2020年4月已获批用于HER2阳性乳腺癌。2023年1月19日,FDA批准全新组合疗法tucatinib(图卡替尼,Tukysa)联合曲妥珠单抗上市,治疗HER2阳性结直肠癌(CRC)成人患者!值得一提的是,这是HER+结直肠癌获批的首款靶向治疗方案,具有里程碑式的意义!、
临床数据显示:在84名接受图卡替尼联合曲妥珠单抗治疗组,确认的客观缓解率(ORR)为38.1%,这意味着,这些多种治疗方案失败的患者接受了全新的组合方案治疗后,竟然有近40%的患者肿瘤显著缩小30%以上甚至消失!
02、白血病/淋巴瘤--zanubrutinib
药品信息
药品名称:zanubrutinib(Brukinsa)
研发公司:BeiGeneUSA
上市时间:2023年1月19日
药物介绍:2023年1月19日,美国食品药品监督管理局(FDA)批准zanubrutinib(Brukinsa,BeiGeneUSA,Inc.)用于慢性淋巴细胞白血病(CLL)或小淋巴细胞淋巴瘤(SLL)。
03、非小细胞肺癌--派姆单抗
药品信息
药名名称:派姆单抗(Pembrolizumab,Keytruda)
研发公司:默沙东
上市时间:2023年1月26日
药品介绍:2023年1月26日,FDA批准PD-1抑制剂派姆单抗(Pembrolizumab,Keytruda)的新适应症,用于手术切除及铂类化疗后的Ⅰb、Ⅱ或Ⅲa期非小细胞肺癌的辅助治疗。获批的临床数据显示:与安慰剂对照组相比,派姆单抗辅助治疗可以显著延长手术完全切除的非小细胞肺癌患者的无病生存期。中位无病生存期达到了58.7个月,接近5年!安慰剂组仅有34.9个月。
04、乳腺癌--Elacestrant
首款可用于2线和3线ER+/HER2-乳腺癌的雌激素受体降解剂
药品信息
药物名称:Elacestrant
研发公司:Stemline
上市时间:2023年1月27日
药物介绍:elacestrant是一种选择性雌激素受体降解剂(SERD),用于ER+/HER2-晚期或转移性乳腺癌患者。关键3期EMERALD研究结果显示,对于总体研究人群和肿瘤携带ESR1突变的患者,其疗效优于当前的标准护理(SOC)药物。这是首款可用于2线和3线ER+/HER2-晚期或转移性乳腺癌患者的口服选择性雌激素受体降解剂(SERD)。
05、淋巴瘤--LOXO-305
药品信息
药名名称:Pirtobrutinib(LOXO-305)
研发公司:礼来
上市时间:2023年1月27日
药品介绍:2023年1月27日,FDA发布公告,批准礼来的Pirtobrutinib(LOXO-305)用于治疗接受至少2线全身治疗(包括BTK抑制剂)后复发的或难治性的套细胞淋巴瘤。
获批数据显示:在既往接受过共价BTK抑制剂治疗的复发/难治性套细胞淋巴瘤患者当中,Pirtobrutinib取得了50%的整体缓解率,其中还有13%的患者在评估时达到了临床完全缓解。值得一提的是,Pirtobrutinib是首款能够用于先前接受过共价BTK抑制剂治疗的套细胞淋巴瘤患者的BTK抑制剂。
06、乳腺癌--Trodelvy
药品信息
药名名称:sacituzumabgovitecan-hziy(Trodelvy)
研发公司:吉利得
上市时间:2023年2月3日
药品介绍:2023年2月3日,FDA批准sacituzumabgovitecan-hziy(Trodelvy,吉利德科学公司)用于无法切除的局部晚期或转移性激素受体(HR)阳性、人表皮生长因子受体2患者(HER2)阴性(IHC0、IHC1+或IHC2+/ISH-)乳腺癌,在转移情况下接受过内分泌治疗和至少两种额外的全身治疗。
07、子宫内膜癌--Jemperli
上市时间:2023年2月3日药品信息
药名名称:dostarlimab-gxly(Jemperli,多斯塔利单抗)
研发公司:葛兰素史克
上市时间:2023年2月9日
药品介绍:2023年2月9日,FDA批准dostarlimab-gxly(Jemperli,多斯塔利单抗)用于错配修复缺陷(dMMR)复发性或晚期子宫内膜癌的成年患者。获批数据显示:总体反应率(ORR)为45.4%,其中完全缓解率(CR)为15.6%;85.9%的患者持续时间≥12个月,54.7%的患者持续时间≥24个月。
08、乳腺癌--Verzenio
上市时间:2023年2月9日药品信息
药名名称:abemaciclib(阿贝西利,Verzenio)
研发公司:礼来
上市时间:2023年3月3日
药品介绍:2023年3月3日,美国食品药品监督管理局(FDA)批准abemaciclib(Verzenio,阿西贝利)与内分泌治疗(他莫昔芬或一种芳香酶抑制剂)一起用于辅助治疗激素受体(HR)阳性的成年患者,HER2阴性、淋巴结阳性、复发风险高的早期乳腺癌。
09、儿童胶质瘤--达拉菲尼&曲美替尼
药品信息
药名名称:达拉非尼(Tafinlar)和曲美替尼(Mekinist)
研发公司:诺华
上市时间:2023年3月16日
药品介绍:2023年3月16日,美国食品和药物管理局批准达拉非尼(Tafinlar,诺华)和曲美替尼(Mekinist,诺华)用于1岁及以上患有低级别神经胶质瘤(LGG)且需要全身系统治疗的BRAFV600E突变儿科患者治疗。FDA还批准了这两种药物的新口服制剂,适用于无法吞咽药片的患者。
10、皮肤癌--Zynyz
药品信息
药名名称:retifanlimab-dlwr(Zynyz)
研发公司:Incyte
上市时间:2023年1月27日
药品介绍:2023年3月22日,FDA加速批准retifanlimab-dlwr(Zynyz)用于患有转移性或复发性局部晚期默克尔细胞癌(MCC)的成年患者。
获批数据显示:总客观缓解率(ORR)高达52%,其中18%的人获得了完全反应(CR),这意味着影像学显示靶病灶全部消失!
11、尿路上皮癌--Padcev
药品信息
药名名称:enfortumabvedotin-ejfv(恩诺单抗)
研发公司:AstellasPharma
上市时间:2023年4月3日
药品介绍:2023年4月3日,FDA加速批准enfortumabvedotin-ejfv(Padcev,AstellasPharma)与pembrolizumab(Keytruda,默克)联合用于治疗不适合接受含顺铂化疗的局部晚期或转移性尿路上皮癌患者。
获批数据显示:121名患者的确认总客观缓解率(ORR)为68%(95%CI:59,76),其中12%完全缓解,这意味着影像学显示靶病灶全部消失!
12、淋巴瘤--Polivy
药品信息
药名名称:polatuzumabvedotin-piiq(Polivy)
研发公司:Genentech,Inc.
上市时间:2023年4月19日
药品介绍:2023年4月19日,FDA批准了polatuzumabvedotin-piiq(Polivy,Genentech,Inc.)与利妥昔单抗产品、环磷酰胺、多柔比星和泼尼松(R-CHP)联合用于治疗既往未经治疗的弥漫性大B细胞瘤成人患者细胞淋巴瘤(DLBCL),未另有说明(NOS)或高级别B细胞淋巴瘤(HGBL),且国际预后指数(IPI)评分为2或更高。
13、淋巴瘤--Epkinly
药品信息
药名名称:Epcoritamab-bysp(Epkinly)
研发公司:GenmabUS,Inc.
上市时间:2023年5月19日
药品介绍:2023年5月19日,FDA加速批准epcoritamab-bysp(Epkinly,GenmabUS,Inc.)用于治疗未另有说明的复发或难治性弥漫性大B细胞淋巴瘤(DLBCL),包括惰性淋巴瘤引起的DLBCL和经过两次或多次全身治疗后的高级别B细胞淋巴瘤。
获批数据显示:总客观缓解率(ORR)高达61%,其中38%的人获得了完全反应(CR)!
14、前列腺癌--奥拉帕尼
药品信息
药名名称:奥拉帕尼(Lynparza)
研发公司:阿斯利康
上市时间:2023年5月31日
药品介绍:2023年5月31日,FDA批准奥拉帕尼(Lynparza,阿斯利康)联合阿比特龙和泼尼松(或泼尼松龙)用于治疗胚系BRCA突变(BRCAm)转移性去势抵抗性前列腺癌(mCRPC)成年患者。
15、淋巴瘤--Columvi
药品信息
药名名称:glofitamab-gxbm(Columvi)
研发公司:Genentech,Inc.
上市时间:2023年6月15日
药品介绍:2023年6月15日,FDA加速批准glofitamab-gxbm(Columvi)用于治疗复发或难治性弥漫性大B细胞淋巴瘤,未另有说明(DLBCL,NOS)或大B细胞淋巴瘤(LBCL)由滤泡性淋巴瘤经过两次或多次全身治疗后引起。
获批数据显示:总客观缓解率(ORR)高达56%,其中43%的人获得了完全反应(CR),这意味着近一半患者影像学显示靶病灶全部消失!
16、前列腺癌--Talzenna
药品信息
药名名称:talazoparib(Talzenna)
研发公司:辉瑞公司
上市时间:2023年6月20日
药品介绍:2023年6月20日,FDA批准talazoparib(Talzenna)与恩杂鲁胺联合用于同源重组修复(HRR)基因突变的转移性去势抵抗性前列腺癌(mCRPC)。
17、白血病-Vanflyta
药品信息
药名名称:quizartinib(Vanflyta)
研发公司:第一三共株式会社
上市时间:2023年7月20日
药品介绍:2023年7月20日,FDA批准quizartinib用于治疗FLT3-ITD突变新诊断急性髓细胞白血病(AML)成人患者。quizartinib成为首个也是当前唯一一个获FDA批准用于治疗FLT3-ITD阳性AML的FLT3抑制剂,且涵盖新诊断AML未移植患者的诱导、巩固以及维持治疗三个阶段。
18、子宫内膜癌-dostarlimab-gxly
药品信息
药名名称:dostarlimab-gxly(多斯塔利单抗,Jemperli)
研发公司:葛兰素史克
上市时间:2023年7月31日
药品介绍:2023年7月31日,FDA批准了dostarlimab-gxly(Jemperli)联合卡铂和紫杉醇,随后批准单药dostarlimab-gxly,用于治疗dMMR或MSI-H的原发性晚期或复发性子宫内膜癌。
19、结直肠癌-LONSURF
药品信息
药名名称:曲氟尿苷和替匹拉西(LONSURF)
研发公司:TaihoOncology
上市时间:2023年8月2日
药品介绍:2023年8月2日,FDA批准曲氟尿苷和替匹拉西(LONSURF,TAS-102)与贝伐珠单抗联合用于治疗先前接受过基于氟嘧啶、奥沙利铂和伊立替康的化疗的转移性结直肠癌(mCRC)。
20、骨髓瘤-Talvey
药品信息
药名名称:talquetamab-tgvs(Talvey)
研发公司:JanssenBiotech
上市时间:2023年8月9日
药品介绍:2023年8月9日,FDA加速批准talquetamab-tgvs(Talvey)用于治疗患有复发性或难治性多发性骨髓瘤且已接受过至少四种既往治疗(包括蛋白酶体抑制剂,免疫调节剂和抗CD38单克隆抗体)的成人患者。
21、前列腺癌--Akeega
药品信息
药名名称:尼拉帕尼联合醋酸阿比特龙与泼尼松
研发公司:杨森生物
上市时间:2023年8月11日
药品介绍:2023年8月11日,FDA批准尼拉帕尼和醋酸阿比特龙与泼尼松的固定剂量组合,用于治疗有害或疑似有害BRCA突变去势抵抗性前列腺癌的成年患者(mCRPC),
22、骨髓瘤-Elrexfio
药品信息
药名名称:elranatamab-bcmm(Elrexfio)
研发公司:辉瑞公司
上市时间:2023年8月14日
药品介绍:2023年8月14日,FDA加速批准了elranatamab-bcmm(Elrexfio),这是一种双特异性B细胞成熟抗原(BCMA)导向的CD3T细胞接合剂,用于患有复发或先前接受过至少四种治疗的难治性多发性骨髓瘤,包括蛋白酶体抑制剂、免疫调节剂和抗CD38单克隆抗体。
23、黑色素瘤-马法兰
药品信息
药名名称:马法兰(HEPZATO)
研发公司:DelcathSystems
上市时间:2023年8月14日
药品介绍:2023年8月14日,FDA批准含有马法兰(HEPZATO,DelcathSystems,Inc.)的HEPZATOKIT(注射用马法兰/肝输送系统)作为肝脏定向治疗,用于治疗患有不可切除肝转移的葡萄膜黑色素瘤成年患者影响小于50%的肝脏且无肝外疾病(或肝外疾病仅限于适合切除或放射的骨、淋巴结、皮下组织或肺)。
24、白血病-博舒替尼
药品信息
药名名称:博舒替尼(Bosulif)
研发公司:辉瑞公司
上市时间:2023年9月26日
药品介绍:2023年9月26日,FDA批准博舒替尼(Bosulif,辉瑞)用于1岁及以上新诊断(ND)或耐药或耐药的慢性期(CP)Ph+慢性粒细胞白血病(CML)儿科患者。
25、非小细胞肺癌-Braftovi+Mektovi
药品信息
药名名称:encorafenib+binimetinib
研发公司:ArrayBioPharmaInc
上市时间:2023年10月11日
药品介绍:2023年10月11日,FDA批准encorafenib与binimetinib治疗转移性BRAFV600E突变非小细胞肺癌成年患者。
26、黑色素瘤-Opdivo
药品信息
药名名称:nivolumab(Opdivo)
研发公司:百时美施贵宝公司
上市时间:2023年10月13日
药品介绍:2023年10月13日,美国食品和药物管理局批准nivolumab(Opdivo,百时美施贵宝公司)用于12岁及以上完全切除的IIB/C期黑色素瘤患者的辅助治疗。
27、非小细胞肺癌-Keytruda
药品信息
药名名称:派姆单抗(Keytruda)
研发公司:默克
上市时间:2023年10月16日
药品介绍:2023年10月16日,美国食品和药物管理局批准派姆单抗(Keytruda,默克)联合含铂化疗作为新辅助治疗,并继续单药派姆单抗作为可切除(肿瘤≥4厘米或淋巴结)的术后辅助治疗阳性)非小细胞肺癌(NSCLC)。
28、鼻咽癌-特瑞普利单抗
药品信息
药名名称:特瑞普利单抗-tpzi(LOQTORZ)
研发公司:Coherus
上市时间:2023年10月27日
药品介绍:2023年10月27日,FDA批准特瑞普利单抗与顺铂和吉西他滨联合用于一线治疗成人转移性或复发性局部晚期鼻咽癌(NPC)。
29、胆管癌-派姆单抗
药品信息
药名名称:派姆单抗
研发公司:默克公司
上市时间:2023年10月31日
药品介绍:2023年10月31日,FDA批准派姆单抗与吉西他滨和顺铂联合用于治疗局部晚期不可切除或转移性胆道癌(BTC)。
30、结直肠癌-呋喹替尼
药品信息
药名名称:呋喹替尼(Fruzaqla)
研发公司:武田
上市时间:2023年11月8日
药品介绍:2023年11月8日,FDA批准呋喹替尼用于治疗既往接受过基于氟嘧啶、奥沙利铂和伊立替康化疗的转移性结直肠癌(mCRC)成年患者。
31、非小细胞肺癌-Augtyro
药品信息
药名名称:repotrectinib(Augtyro,瑞普替尼)
研发公司:百时美施贵宝
上市时间:2023年11月15日
药品介绍:2023年11月15日,FDA批准repotrectinib用于治疗局部晚期或转移性ROS1阳性非小细胞肺癌(NSCLC)。
32、胃癌-派姆单抗
药品信息
药名名称:派姆单抗(Keytruda)
研发公司:默克公司
上市时间:2023年11月16日
药品介绍:2023年11月16日,美国食品和药物管理局批准派姆单抗(Keytruda,默克公司)与含氟嘧啶和铂类化疗药物联合用于一线治疗患有局部晚期不可切除或转移性HER2阴性胃或胃食管交界处(GEJ)的成人患者腺癌。
33、乳腺癌-Truqap
药品信息
药名名称:capivasertib(Truqap)
研发公司:阿斯利康
上市时间:2023年11月16日
药品介绍:2023年11月16日,FDA批准capivasertib(Truqap,阿斯利康制药)与氟维司群联合治疗激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的局部晚期或转移性乳腺癌成年患者
34、前列腺癌-恩杂鲁胺
药品信息
药名名称:恩杂鲁胺(Xtandi)
研发公司:安斯泰来
上市时间:2023年11月16日
药品介绍:2023年11月16日,FDA批准恩杂鲁胺用于治疗具有高转移风险(高风险BCR)生化复发的非转移性去势敏感型前列腺癌(nmCSPC)。
35、白血病-Jaypirca
药品信息
药名名称:pirtobrutinib(Jaypirca)
研发公司:礼来
上市时间:2023年12月1日
药品介绍:2023年12月1日,FDA加速批准pirtobrutinib用于治疗已接受过至少两种既往治疗的慢性淋巴细胞白血病或小淋巴细胞淋巴瘤(CLL/SLL)成人患者,包括BTK抑制剂和BCL-2抑制剂。
36、神经母细胞瘤-IWILFIN
药品信息
药名名称:依氟鸟氨酸(IWILFIN)
研发公司:辉瑞公司
上市时间:2023年12月13日
药品介绍:2023年12月13日,FDA批准依氟鸟氨酸用于降低对既往多药治疗至少有部分缓解的高危神经母细胞瘤(HRNB)成人和儿童患者复发的风险。
37、肾细胞癌-belzutifan
药品信息
药名名称:belzutifan(Welireg)
研发公司:默克
上市时间:2023年12月14日
药品介绍:2023年12月14日,FDA批准belzutifan用于治疗PD-1或PD-L1和VEGF-TKI治疗后病情进展的晚期肾细胞癌(RCC)。
38、尿路上皮癌-Padcev
药品信息
药名名称:enfortumabvedotin-ejfv(Padcev)
研发公司:安斯泰来
上市时间:2023年12月15日
药品介绍:2023年12月15日,FDA批准enfortumabvedotin-ejfv与派姆单抗联合用于治疗局部晚期或转移性尿路上皮癌(la/mUC)患者。
以上新药仅为众多研发热点中的一小部分,还有众多的新药研发,创新技术纷纷在路上,相信2024年将有更多的药物获批上市!除此之外,还有多款正在研发的抗癌新药也显示出广谱抗癌的实力。“方舟援助计划”可以为患者提供上市新药和未上市新药免费治疗的机会。
相信随着医学研究的不断深入,越来越多的新药即将研发上市,将有更多的病友跨过一个又一个5年!
参考资料:美国FDA官网、中国NMPA官网
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
早期膀胱癌术后五年生存率高达90%,这五
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

警惕!乳腺癌复发偏爱这3大人群!术后一定
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【实体瘤溶溜病毒免费招募】溶瘤病毒Ml(
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
从多处转移到完全缓解!新型CAR-T细胞
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
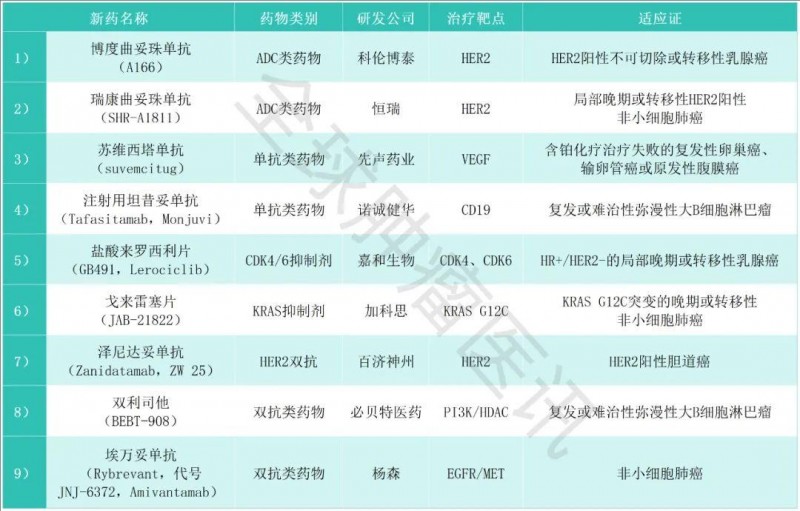
救命药加速入场!2025第二季度9款抗癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




