胶质母细胞瘤电场疗法治疗在临床指南中的进展及应用
胶质母细胞瘤电场疗法治疗在临床指南中的进展及应用
胶质母细胞瘤(GBM)是一种破坏性的脑肿瘤,尽管近年来在手术,放疗和化疗方面取得了进展,但预后差。胶质母细胞瘤患者的生存率仍然很差,4名患者中仅有1例存活2年,5年生存率约为5%。几乎都会出现复发,复发后预后差,无进展生存期和总生存期(OS)很短。各种挽救性化疗策略已经应用,但效果非常有限。电场疗法(TTFields)是一种新的治疗方式,被批准用于治疗新诊断或复发性胶质母细胞瘤!
十年磨一剑,电场疗法带来新希望
这是十多年来第一次,出现了一种非有效地疗法,能够显著的提高脑质母细胞瘤患者的生存期!
电场疗法涉及医疗设备和换能器阵列,以提供低强度,中频,交替电场,产生有选择性的、针对快速分裂肿瘤细胞抗有丝分裂毒性作用。

在新诊断的GBM中显示出前所未有的五年生存率结果。数据显示,接受Optune联合替莫唑胺治疗比单独接受替莫唑胺治疗的患者的中位生存期延长近5个月。连续五年跟踪,Optune联合替莫唑胺治疗的患者的5年生存率为13%,而单独使用替莫唑胺治疗的患者为5%!这是近十年来胶质瘤取得的最大成绩!TTFields治疗已经证实了GBM治疗的有效性,包括新诊断GBM患者的OS改善,目前正在对其他脑和颅外肿瘤进行试验。
令肿瘤患者感到兴奋的是,这种疗法可以使肿瘤患者重新正常生活和工作!

52岁的恩特雷森(Endresen)在芝加哥郊区的一家直邮公司工作,他每两个月扫描一次,检查是否有癌症复发。“我们已经庆祝了两年还没有肿瘤复发,十二月,我还去了南非。医生说很多患者因为麻烦而不能尝试这个手段,这是一个不可思议的机器,我没有头发很好。”

患者的生存治疗在电场疗法的帮助下,得到了很大的提高
什么是电场疗法
电场疗法利用低强度,中频,交替电场,其整体效应干扰细胞分裂并延长细胞分裂,并破坏快速分裂细胞中的胞质分裂,导致细胞凋亡。
电场疗法利用癌细胞的电极性,几何形状和快速分裂性,特别是针对这些细胞内的大分子产生选择性抗癌效应(图1)。最有效的细胞杀伤的最佳电频率因肿瘤类型而异。电场疗法几乎对正常细胞没有伤害。
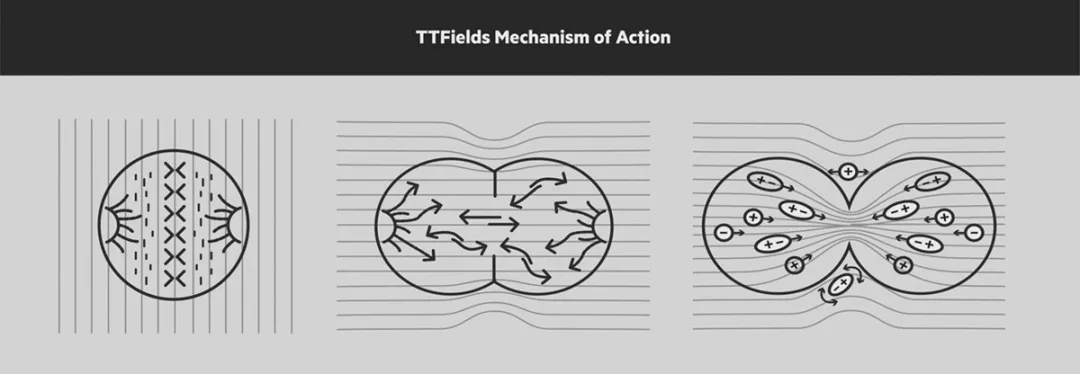
体外和体内动物模型的初步研究
电场疗法作为恶性肿瘤治疗选择的概念在21世纪初的临床前研究中进行了评估。最初显示电场疗法有效抑制体外各种快速分裂的癌细胞生长。
电场的最佳功效
电场的功效取决于施加电场的强度,频率和方向。经过多次尝试,他们发现当电场频率在150-200千赫兹范围内,强度为每厘米1.1伏特时,有趣的事情发生了:在电场的持续作用下,肺癌细胞的生长与扩散速率显著下降,这意味着这些恶性肿瘤细胞得到了控制。相反,在同样环境下的正常内皮细胞没有受到任何影响。而在没有电场的情况下,肿瘤细胞在两天内就会出现增殖和扩散。这些结果说明了电场在控制肿瘤生长方面的有效性。
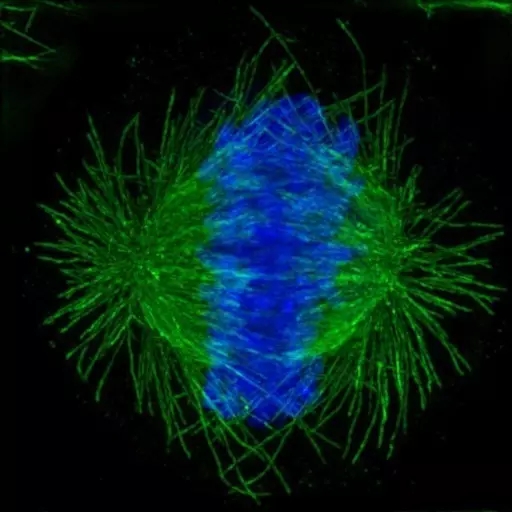
大鼠胶质瘤电场试验,肿瘤明显缩小
电场疗法的抗肿瘤作用在体内颅内大鼠胶质瘤模型中得到证实,与未治疗的肿瘤相比,观察到肿瘤体积缩小42.6%(双向电场)和53.4%(三维电场)。
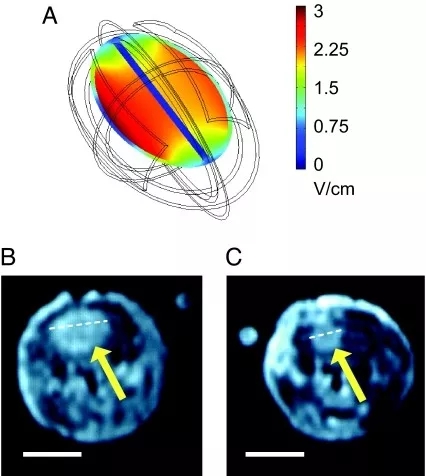
TTFields抑制颅内神经胶质瘤的生长。A:大鼠脑模型中电场强度分布模拟(使用三维网格)。B和C:冠状MRI
电场疗法重点试验数据
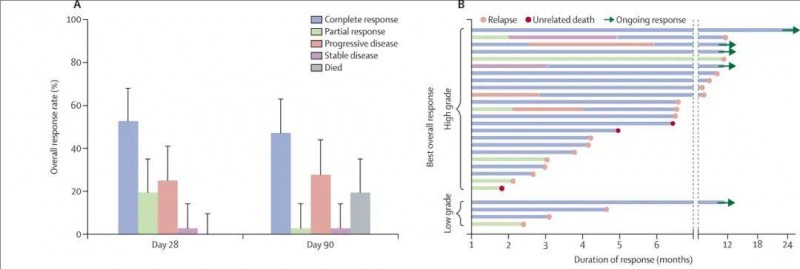
令人鼓舞的试验结果使得电场疗法迅速在胶质母细胞瘤患者开始进行初步评估。最初的试验研究了电场疗法作为10例复发性、难治性GBM患者的单纯治疗,值得注意的是,接受电场治疗的复发性高级别胶质瘤患者中有67.5%在开始治疗后1年仍然存活!
第二项试验性试验在20名初次接受标准放疗和替莫唑胺初次治疗的新确诊的GBM患者中,测试了电场疗法联合替莫唑胺对比替莫唑胺单药治疗。中位疾病进展时间分别为155周与31周。联合治疗组患者中位生存期> 39个月,而单药组大约14.7个月,存在巨大的差距,并且对于肿瘤患者意义重大!!所有接受电场治疗的患者仅出现治疗部位皮疹。没有3级或更高的毒性。
复发性GBM管理中的前瞻性随机试验
这项前瞻性,随机,国际的3期EF-11试验比较了电场治疗与全身治疗复发性GBM患者的疗效。117例患者被随机分配到电场治疗,120患者选择全身治疗。主要研究终点为总生存期(OS)。接受TTFields治疗的患者被指示每天佩戴该设备≥18小时。
2011年,美国食品和药物管理局(FDA)基于EF-11试验的结果批准了电场疗法治疗复发性GBM,与全身治疗相比,电场治疗的生存率相当,并且显著改善患者生活质量。
第三阶段关键EF-14试验
一项前瞻性随机3期临床试验(EF-14)评估了TTFields在新诊断GBM初始治疗中的应用,研究结果使FDA2015年10月批准电场疗法联合替莫唑胺用于治疗新诊断的GBM。
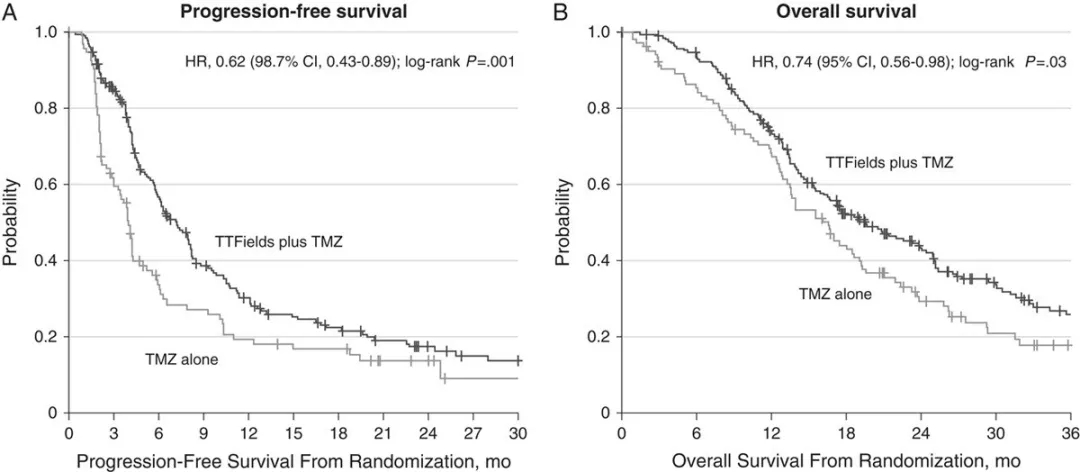
在国际EF-14试验中,695名完成放化疗的患者以2:1的比例随机接受电场疗法+替莫唑胺联合治疗或单独替莫唑胺(标准辅助治疗)的维持治疗。实验结果显示:TTFields组与对照组的中位PFS显着更长(7.1个月VS4.0个月)。联合组中位OS为20.5个月,而对照组为15.6个月。
初级毒性管理
电场疗法的主要毒性是皮肤刺激。预防策略包括适当的剃须,清洁头皮和频繁的更换电极贴片的位置。当出现皮肤问题时,通常可以更换贴片位置或口服抗生素,使用皮质类固醇。
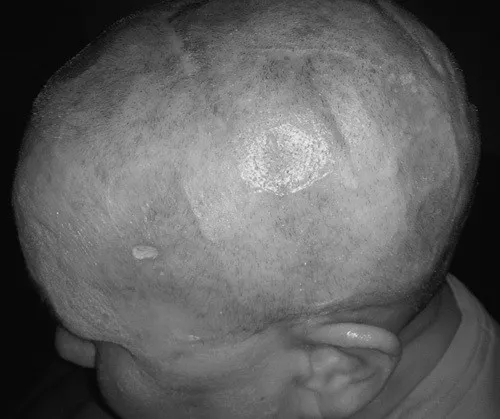
治疗的持续时间
电场治疗的抗肿瘤效果只有在使用时才会发生。与化疗不同,在初次给药后没有与治疗有关的“半衰期”。因此,依从性对电场治疗的有效性尤为重要。
大量表明,坚持电场治疗是很重要的。电场疗法不应仅在影像学发现进展时停止,因为这有可能是使用替莫唑胺所遇到的伪进展。
正在进行的临床研究
TTFields是GBM的一种新型癌症治疗方式。
目前正在测试治疗更多的癌症类型,包括:间皮瘤、非小细胞肺癌、非小细胞肺癌脑转移、乳腺癌、宫颈癌、结直肠癌、肝癌、胃癌、肾癌、小细胞肺癌等。
如何申请电场治疗
目前,电场疗法在全球范围内属于前瞻性研究,尚未正式进入中国。中国国产化的电场治疗设备正在加紧研发,并获得了301医院、华山医院等多家医院及神外专家的支持。我们期待它能在更多的癌症中验证疗效,为患者们带来更多治疗方案。
关于这项新技术,深入了解的专家并不多,美国亨利福特医院、梅奥诊所的专家可接受癌症患者电场疗法会诊申请,但是美国的治疗费用较高,每天700美金,需每天去医院治疗。
此外,日本也引进TTF电场技术,并已成功研发类似TTF的电场治疗设备,称为ECCT,一套设备9万人民币左右,可购买回国内长期使用。详情可咨询全球肿瘤医生网医学部(400-666-7998).我们希望,这种新型癌症疗法能够早日在国内上市,造福更多的肿瘤患者。
参考资料:
1. Stupp R, Hegi ME, Mason WP, et al. Effects of radiotherapy with concomitant and adjuvant temozolomide versus radiotherapy alone on survival in glioblastoma in a randomised phase III study: 5-year analysis of the EORTC-NCIC trial. Lancet Oncol. 2009;10:459–466.
2. Stupp R, Mason WP, van den Bent MJ, et al. Radiotherapy plus concomitant and adjuvant temozolomide for glioblastoma. N Engl J Med. 2005;352:987–996.
3. Siegel R, Ma J, Zou Z, et al. Cancer statistics, 2014. CA Cancer J Clin. 2014;64:9–29.
4. Gilbert MR, Wang M, Aldape KD, et al. Dose-dense temozolomide for newly diagnosed glioblastoma: a randomized phase III clinical trial. J Clin Oncol. 2013;31:4085–4091.
5. Chinot OL, Wick W, Mason W, et al. Bevacizumab plus radiotherapy-temozolomide for newly diagnosed glioblastoma. N Engl J Med. 2014;370:709–722.
6. Gilbert MR, Dignam JJ, Armstrong TS, et al. A randomized trial of bevacizumab for newly diagnosed glioblastoma. N Engl J Med. 2014;370:699–708.
7. Anton K, Baehring JM, Mayer T. Glioblastoma multiforme: overview of current treatment and future perspectives. Hematol Oncol Clin North Am. 2012;26:825–853.
8. Gallego O. Nonsurgical treatment of recurrent glioblastoma. Curr Oncol. 2015;22:e273–e281.
9. Weller M, Cloughesy T, Perry JR, et al. Standards of care for treatment of recurrent glioblastoma—are we there yet? Neuro Oncol. 2013;15:4–27.
10. Mehta M, Brem S. Recent updates in the treatment of glioblastoma: introduction. Semin Oncol. 2014;41(suppl 6):S1–S3.
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
里程碑!mRNA-4157联合派姆单抗让
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

刚刚!"双免王炸"纳
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2025肺癌生存新希望:六大"
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
早期甲状腺癌术后五年生存率超99%,但要
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
早期甲状腺癌术后五年生存率超99%!但忽
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




