【实体瘤招募】CAR-T细胞治疗晚期实体瘤的安全性和有效性临床研究
改写历史,中国CAR-T登上世界舞台!
首个靶向claudin18.2的CAR-T疗法临床招募!
年龄18至75岁,男性或女性; 患有病理证实的实体瘤(即晚期胃癌,食管胃交界癌和胰腺癌)并且经标准治疗失败的受试者; Claudin 18.2 IHC染色阳性; 预计寿命> 12周;
CAR-T细胞治疗晚期实体瘤的安全性和有效性临床研究
CAR-T细胞治疗实体瘤的Ⅰ期临床研究
关于CAR-T疗法,你需要了解的
FDA已批准两款CAR-T疗法
什么是CAR-T疗法
骄傲!华人团队研发带来变革的新型CAR-T疗法!
CAR-T技术在实体瘤中的瓶颈
突破瓶颈!CAR-T疗法迎战实体肿瘤!
其中具有代表性的抗原靶点包括:
目前,国内也进行了大量的间皮素CAR-T临床研究,取得了初步成果,在小鼠实验中,接受新型间皮素CAR-T疗法的晚期卵巢癌小鼠的肿瘤出现快速消退。目前这项技术正在国内招募各类晚期实体肿瘤患者,想参加的可以向全球肿瘤医生网医学部申请(400-666-7998)。
春暖花开!CAR-T疗法将为国内患者带来新希望!
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
里程碑!mRNA-4157联合派姆单抗让
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

刚刚!"双免王炸"纳
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2025肺癌生存新希望:六大"
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
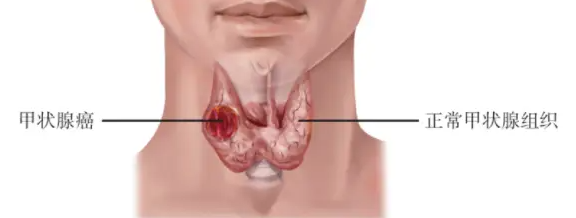
早期甲状腺癌术后五年生存率超99%,但要
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
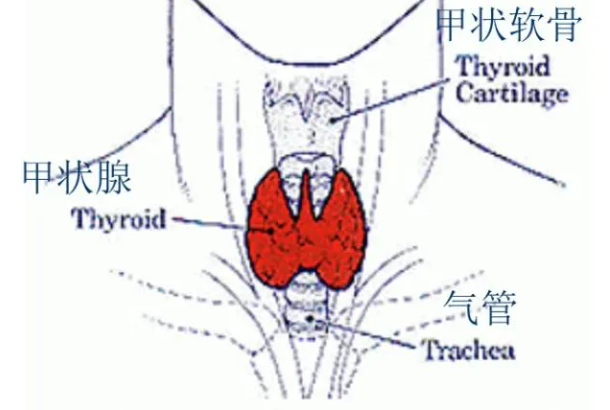
早期甲状腺癌术后五年生存率超99%!但忽
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




