30%的非小细胞肺癌患者都在用这类药,患者的中位生存期已经接近5年!
30%的非小细胞肺癌患者都在用EGFR基因突变靶向药物,那么EGFR靶向药有哪些呢
EGFR是非小细胞肺癌最常见的驱动基因,在所有非小细胞肺癌中阳性率达到17%,在国内患者中接近30%~40%,在肺腺癌中更是高达约60%。再加上EGFR抑制剂的高响应率以及出色疗效,尤其是其在亚种患者临床试验当中取得的格外优秀的结果,这类药物又被称作“上帝送给东方人的礼物”。
目前,EGFR突变已经成为了非小细胞肺癌的驱动基因突变当中,获批药物最多的一个。能够用于这类突变患者的、国内外上市靶向药物数量已经超过两位数,如此众多的选择,自然也让患者们多了几分迷惑。
这么多的EGFR抑制剂之间都有什么差别、各自有哪些特点,应当如何使用、使用顺序又是否重要呢?今天,基因药物汇带大家简单了解一下,为中国非小细胞肺癌患者创造了“奇迹”的EGFR抑制剂。
PART 1、已经上市的EGFR抑制剂
目前,已经上市的EGFR抑制剂,根据其特点,共分为三代。我们就从这三代药物的特点,带大家系统了解一下这类靶向药物。
第一代:EGFR靶点的"开拓者"与"奠基人"
关键词:可逆性结合,耐药风险高,普及率高
获批药物:厄洛替尼,吉非替尼,埃克替尼
最初,科学家发现部分非小细胞肺癌的癌细胞中EGFR蛋白表达水平远高于正常细胞,并以此为突破口研发了第一代EGFR抑制剂。从首款EGFR抑制剂吉非替尼于2003年获得FDA批准上市至今,已获得FDA批准上市的一代EGFR抑制剂包括厄洛替尼、吉非替尼和埃克替尼。
这类药物的共同点在于,化学结构上有相同的喹唑啉母环,主要通过与ATP竞争性结合的方式,抑制发生了细胞的EGFR蛋白功能,主要针对19号外显子缺失和21号外显子点突变。
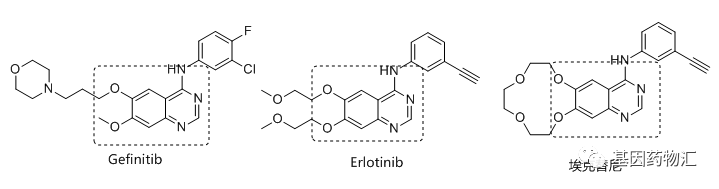
除了发生突变的细胞,一代EGFR抑制剂也同样会抑制正常细胞的EGFR蛋白功能,从而导致皮疹、腹泻等不良反应。由于药物与靶点的结合方式为可逆性结合,一代EGFR抑制剂发生耐药的风险较大,通常发生在在连续用药1年左右,最常见的耐药突变为T790M突变型。
第二代:结构更优化,缓解期延长
关键词:不可逆结合,更好的疗效,更低的耐药风险
获批药物:阿法替尼,达克替尼
与一代药物不同,二代EGFR抑制剂对于药物化学结构做出了改进,除竞争性地与EGFR上ATP结合位点可逆地结合外,还能与EGFR特有的氨基酸残基发生烷基化作用或共价键结合,即不可逆的结合。目前,获得FDA批准上市的二代EGFR抑制剂包括阿法替尼和达克替尼两款。
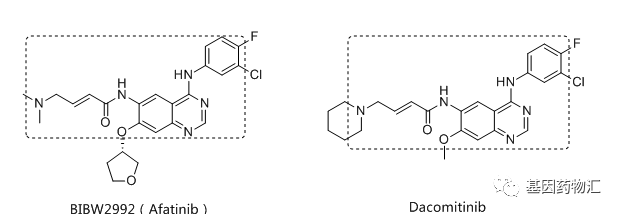
2016年ESMO大会上,全球首次一代与二代EGFR抑制剂吉非替尼和阿法替尼的头对头对比试验LUX-Lung 7试验公布了初步研究的数据。这是一二代EGFR抑制剂的首次正面“交锋”,显然,二代药物阿法替尼先下一局。
LUX-Lung 7试验的初步结果显示,接受二代EGFR抑制剂阿法替尼治疗的患者中位总生存期为27.9个月,接受一代EGFR抑制剂吉非替尼治疗的患者中位总生存期为24.5个月;阿法替尼治疗患者中位治疗失败时间为13.7个月,而吉非替尼治疗患者的中位治疗失败时间为11.5个月,显然接受阿法替尼治疗的患者治疗有效、疾病控制良好的时间整体更久。
与一代药物相比,二代EGFR抑制剂在避免耐药方面做出了卓有成效的努力。二代EGFR抑制剂的开发逻辑是,如果药物的疗效更好,或许耐药性会出现得更晚、甚至不会发生耐药。因此,二代EGFR抑制剂采取的是不可逆的共价结合方式,临床中展现出了更强的抑制作用,但仍然不能用于治疗一代EGFR抑制剂后发生耐药突变的患者,如T790M突变型患者等。
耐药之后该如何治疗?——在这样的迫切需求之下,第三代EGFR抑制剂诞生了。
第三代:耐药以及初治,都有显著疗效
关键词:克服前代耐药,一线治疗疗效更好,入脑活性更强
获批药物:奥希替尼,阿美替尼,伏美替尼
2015年,FDA批准了首款三代EGFR抑制剂奥希替尼,填补了长期以来一二代EGFR抑制剂耐药后的治疗困境。除了靶向最常见的耐药突变T790M,奥希替尼对于常见的EGFR突变类型,如外显子18、19、21的突变型,均有很好的治疗效果。此外,奥希替尼具有良好的选择性,对于未发生突变的野生型EGFR蛋白作用效果弱,脱靶毒性更小,造成的不良反应更轻微。当然,比起一代EGFR抑制剂,奥希替尼还有非常重要的一点优势,即奥希替尼的入脑性更强,对于发生了脑转移的患者同样具有较好的疗效。
而在国内,也有两款第三代EGFR抑制剂已经获批上市,从疗效上来看,与奥希替尼难分伯仲。
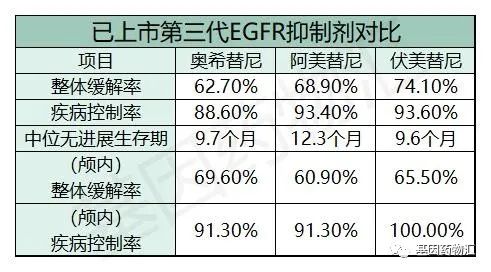
这一代药物的特点,代表了EGFR抑制剂发展的主流方向:更小的脱靶毒性带来更少的不良反应,更强的靶向性带来更好的疗效,更少发生耐药、同时也具备针对耐药突变的能力,以及更强的入脑性带来的治疗脑转移病灶的能力。能够将诸多优势集中于一身的药物,必定能够成为下一代的“明星药”。
PART 2、正在研究的新药
从适应症上来说,目前的三代药物,已经覆盖了EGFR突变当中的大部分常见亚型,但仍有部分患者不能完全匹配这些药物的适应症。目前在研的EGFR抑制剂当中,许多新药都将这部分尚未被满足的适应症作为研究重点。
第四代EGFR抑制剂
尽管能够破解一二代EGFR抑制剂最常见的突变T790M,同时也在避免耐药方面做出了卓有成效的努力,但第三代EGFR抑制剂同样存在发生进一步耐药的可能。Del19/T790M/C797S及L858R/T790M/C797S三突变是第三代EGFR抑制剂耐药后最常见的突变类型,约占20%~40%左右。目前已有的药物对于此类患者治疗效果欠佳,市场需求再次出现空白。
针对这一突变型的第四代EGFR已经投入了临床试验当中,国内外都有布局,相信会在不久的未来交出一份令人满意的“答卷”。
EGFR/c-MET"双抗"
在EGFR抑制剂耐药的患者当中,MET异常的患者占比比较高。超过20%的EGFR突变型非小细胞肺癌患者因继发的MET异常而产生了耐药,因此,能够同时抑制EGFR与c-MET的“双抗”,也成为了非常重要的研发方向。而临床研究的数据也证明,这类药物不仅能够用于耐药患者的治疗,也能够用于一部分对EGFR抑制剂不敏感的亚型的患者的治疗,例如ex20ins。
以目前已经获批的EGFR/c-MET“双抗”JNJ-6372为例。在CHRYSAILS试验中,这款药物治疗EGFR 外显子20插入突变(ex20ins)患者的整体缓解率有40%,患者的中位无进展生存期达到了8.3个月,中位总生存期22.8个月;联合第三代EGFR抑制剂拉泽替尼治疗奥希替尼耐药的患者,整体缓解率36%。
目前这类药物的临床试验进展比较快,希望尝试这类药物的患者,可以咨询基因药物汇(400-686-1602)了解详情。
结构优化的新药
还有一部分EGFR抑制剂,采用了与目前已经上市的药物完全不同的新结构。这样的结构特点,反映在适应症上就是,这部分新药的临床试验,允许已经接受过吉非替尼、厄洛替尼、奥希替尼等EGFR抑制剂治疗的患者入组。
目前这类药物的在研适应症多集中于一些相对罕见的EGFR突变亚型,具体情况大家可以咨询基因药物汇医学部了解。
PART 3、关于EGFR抑制剂的使用
了解过了EGFR抑制剂的现状,下面让我们简单了解一下EGFR抑制剂的应用与疗效。
盲试,曾经为中国患者创造"奇迹"
由于EGFR突变在亚洲人当中的阳性率比较高,且EGFR抑制剂的疗效比较好、价格又相对比较容易接受,因此这种盲试EGFR抑制剂的做法在患者当中是存在的。
EGFR抑制剂能够在中国得到推广、并通过临床试验验证了其对于中国患者的出色疗效,其实也有赖于我国专家最初的勇敢尝试。
当然,如今各种基因检测技术的发展很快,水平完全超越了十年前,所以如果有机会的话,大家最好还是完善基因检测,根据检测结果精准指导用药。
"1/2+3",还是"3+X"
目前,除了第一代EGFR抑制剂以外,以奥希替尼为代表的第三代EGFR抑制剂已经获批了一线治疗适应症,也就是说,EGFR敏感突变的患者,一线治疗已经有两类选择了。
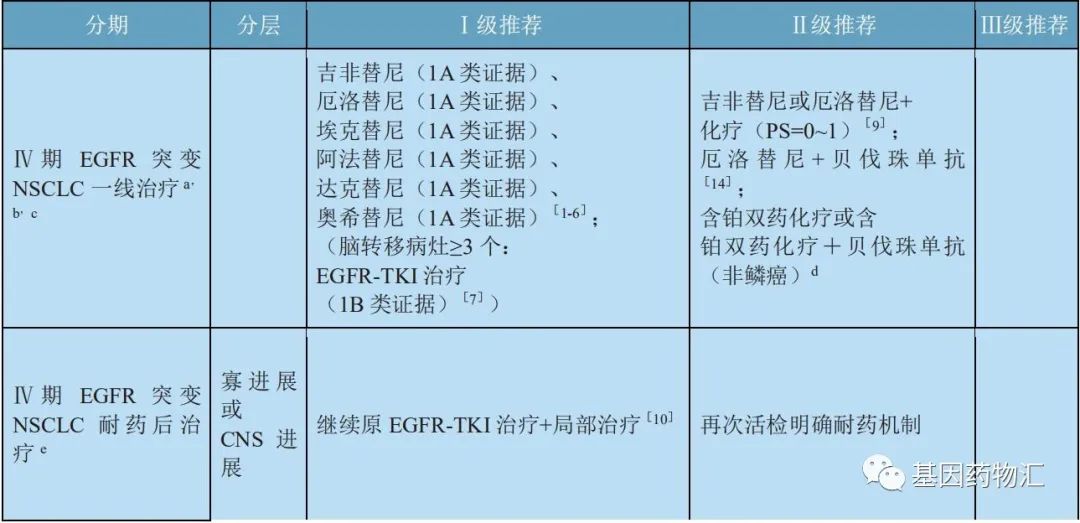
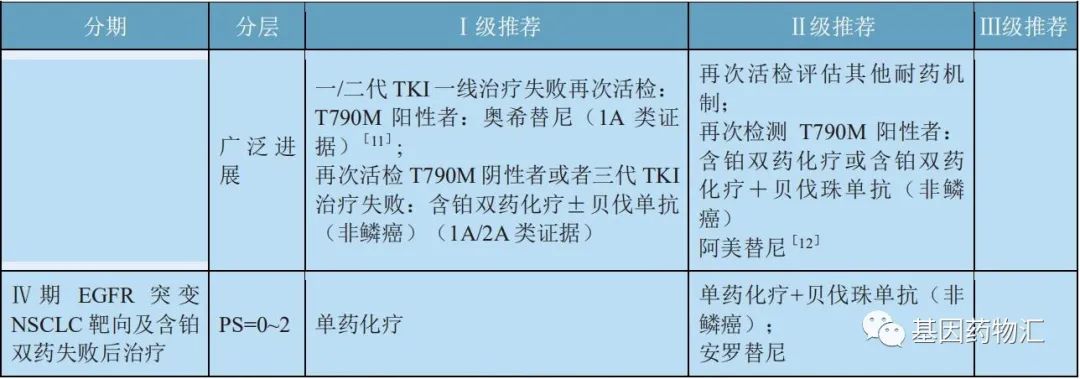
至于“先用哪一代药物”,指南当中已经针对这个问题给出了答案。除了指南推荐,许多临床研究也在尝试着解答这个重要的问题。根据三代EGFR抑制剂的特点,临床上衍生出了“1+3”、“2+3”、“3+X”等多种治疗方案。
1)"1+3",中位总生存期58.0个月
2019年WCLC大会上的报告指出,采用“1+3”模式治疗,即在接受一代EGFR抑制剂耐药后继续使用三代药物治疗的患者中,发生T790M突变的患者中位总生存期能够达到58.0个月!
2)"2+3",中位总生存期47.6个月
同一报告中同样指出,在采用“2+3”模式治疗的患者中,发生T790M耐药突变的患者中位总生存期可以达到41.3个月。
而在2020年公开的现实世界研究,第三阶段的GioTag研究中则指出,使用阿法替尼(Afatinib,Gilotrif)+奥希替尼的“2+3”序贯治疗方案,患者的中位总生存期为47.6个月,预估2年总生存率为85%;目前的数据成熟度仅有35%,还有很大的提升空间!
3)"3+X",获益患者更多
上述两种方案的生存期数据都非常可观,只要能够对药物响应、且坚持完成了全部治疗,那么就有将近一半的概率能够跨过5年生存这个坎。但现实世界的统计数据显示,“1+3”方案的获益人群比例大约25%,“2+3”方案更低,只有大约10%。效果虽好,但如果绝大部分患者都耐受不下来、完成不了治疗,那这样好的疗效也只是曲高和寡,鲜有人和。
而奥希替尼一线治疗方案的落地,则是让患者们看到了全新的希望。
根据Ⅲ期FLAURA试验的结果,奥希替尼一线治疗EGFR突变的非小细胞肺癌,中位无进展生存期为18.9个月,中位总生存期为38.6个月。研究者认为,使用“3+X”的序贯方案,患者的预估中位总生存期可以超过40个月。
基于国内患者的三项第三代EGFR抑制剂一线治疗临床试验也都给出了相似的出色结果:
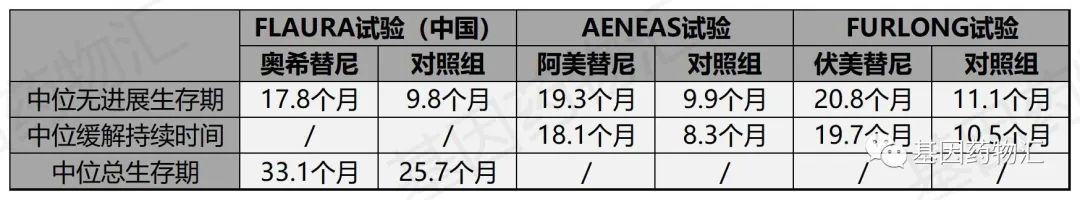
研究者指出,“3+X”方案的缓解率将远远超过“1+3”与“2+3”。以奥希替尼为一线治疗方案,优势将最大限度地体现于获益患者数量上。
EGFR抑制剂 vs 脑转移,疗效如何
相信很多关注了基因药物汇的读者,都看过我们之前的一篇文章,《20个脑转移病灶5周全部消失!肺癌脑转移=死亡通知书?选对方案,连放疗都不用!》
文中所提到的一个经典案例,就是由第三代EGFR抑制剂奥希替尼所创造的。患者治疗前,颅脑MRI检查提示,她头颅中大大小小的转移病灶数量超过20个。但在接受了仅仅5周的奥希替尼治疗之后,患者颅内的病灶,完全消失!
除了奥希替尼,其它EGFR抑制剂治疗脑转移病灶的疗效也非常出色。第一、二代EGFR抑制剂(吉非替尼、厄洛替尼、阿法替尼等),治疗颅内病灶的缓解率在60%~70%;第三代EGFR抑制剂(奥希替尼、阿美替尼、伏美替尼等),治疗第一二代药物耐药的患者,颅内病灶缓解率仍然高达60%~70%,控制率更是接近100%。
三款已经获批上市的第三代EGFR抑制剂,在脑转移患者的治疗中,颅内病灶缓解率都非常出色:
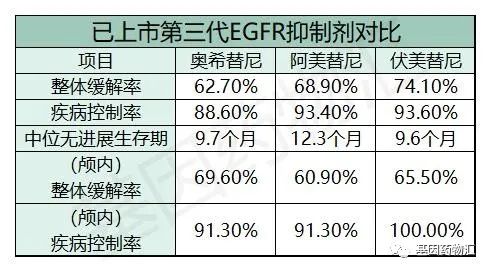
这说明,在某些特殊的情况下(比如患者可能很难耐受放疗,或颅内转移病灶数量过多等),可以考虑先使用药物治疗。如果患者对于药物的响应良好,很可能靶向药物的治疗能够为脑部放疗提供条件,甚至,部分患者有希望直接凭借药物治疗完全消除病灶。
新药的发展,让"难治"突变有了新希望
2022年的ESMO EGFR突变非小细胞肺癌治疗专家共识当中提到了这样一句话,早期报告低估了EGFR外显子20插入突变(ex20ins)的患病率。
主要限于当时检测的水平,我们一直认为ex20ins是一种比较罕见的EGFR突变亚型,占所有EGFR的2%~6%。但最近随着二代测序(NGS)的发展与普及,我们逐渐意识到,ex20ins的占比远比我们想象中更高,大约占所有已鉴定EGFR突变的12%。
与EGFR经典突变型相比,ex20ins的晚期患者的预后是更差的,对于EGFR抑制剂的治疗原发性耐药,预后与接受化疗的野生型(EGFR阴性)病例基本相似。
2021年世界肺癌大会(WCLC)上曾经公开了一项回顾性分析结果,对比了常见的EGFR突变(cEGFR)患者与EGFR ex20ins患者在现实世界条件下接受包括EGFR抑制剂在内的各项标准治疗的疗效。
研究共筛选了62464例晚期非小细胞肺癌患者,其中,接受EGFR抑制剂治疗的ex20ins患者(共76例),发生疾病进展或死亡的风险足足比cEGFR患者(共2749例)高出了170%!
在现实世界治疗条件下,这部分ex20ins患者的中位无进展生存期为2.86个月,中位总生存期为7.46个月;而cEGFR患者的中位无进展生存期为10.45个月,中位总生存期为25.49个月。
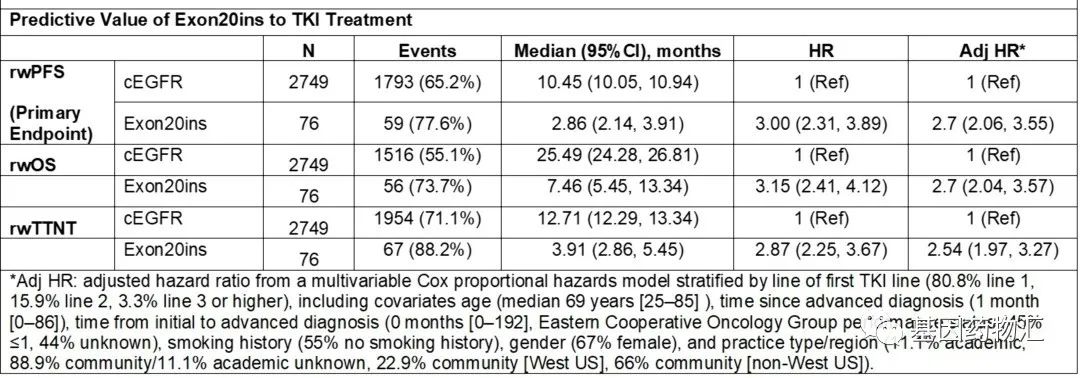
即使是在EGFR非小细胞肺癌的治疗中屡建奇功的第三代EGFR抑制剂奥希替尼,也没能突破ex20ins的“阻碍”。
一项来自荷兰的试验,使用大剂量的奥希替尼(160 mg)治疗EGFR ex20ins阳性、T790M阴性的晚期非小细胞肺癌患者,受试患者共24例。结果整体缓解率为27%,包含了1例临床完全缓解的患者;中位无进展生存期为5.5个月,中位缓解持续时间为8.2个月,中位总生存期15.8个月。治疗中21%的患者需要减少治疗剂量。
虽然加大了剂量,但是27%的缓解率还是和其它报告差不多,不良事件的发生率也差不多,患者的耐受性更算不上理想。
但新药的发展,让这些“难治突变”的患者,看到了新的希望。
同年的ESMO大会上,伏美替尼公布的一项针对ex20ins的疗效数据,则是让人眼前一亮。队列1的10例患者,都已经接受了至少1次评估,截至2021年4月30日,中位治疗时间目前是3.5个月,其中7例患者已经达到了临床部分缓解,也就是说当前的临床缓解率是70%!其中5例患者的缓解已经得到了确认,2例患者正在等待进一步的确认。
所有10例患者都观察到了靶病灶的缩小,比例从3%到72.3%不等,当前的疾病控制率高达100%!
作为初步研究结果,这个70%和100%可以说是相当的令人鼓舞,有在这个适应症上超越奥希替尼的强大潜力。当然,由于目前公开的仅为小样本的试验结果,因此我们更多地是在期待这款药物的潜力,并期待进一步的试验数据公开。
目前伏美替尼治疗ex20ins患者的临床试验还在招募阶段,如果大家想进一步了解这款药物的临床试验项目,可以联系基因药物汇。
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
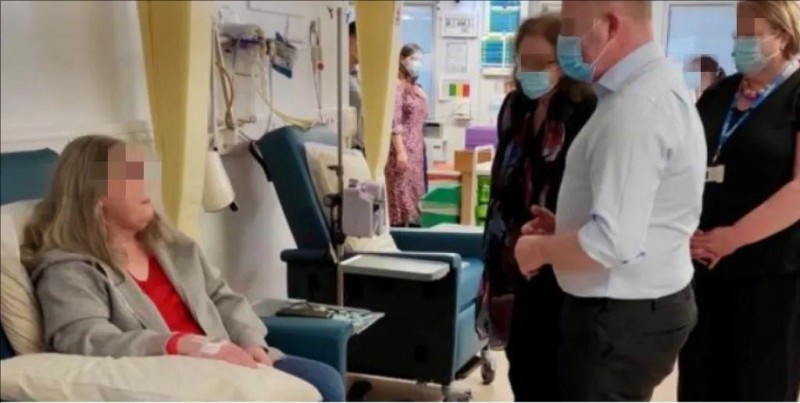
肠癌患者找到"重生密码&quo
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

绝境逆袭!NY-ESO-1 TCR-T疗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
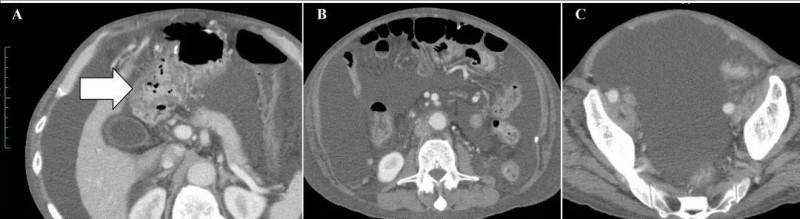
结直肠癌六大治疗性疫苗重磅集结!最长控瘤
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
253例真实世界研究证实:益生菌联合IC
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
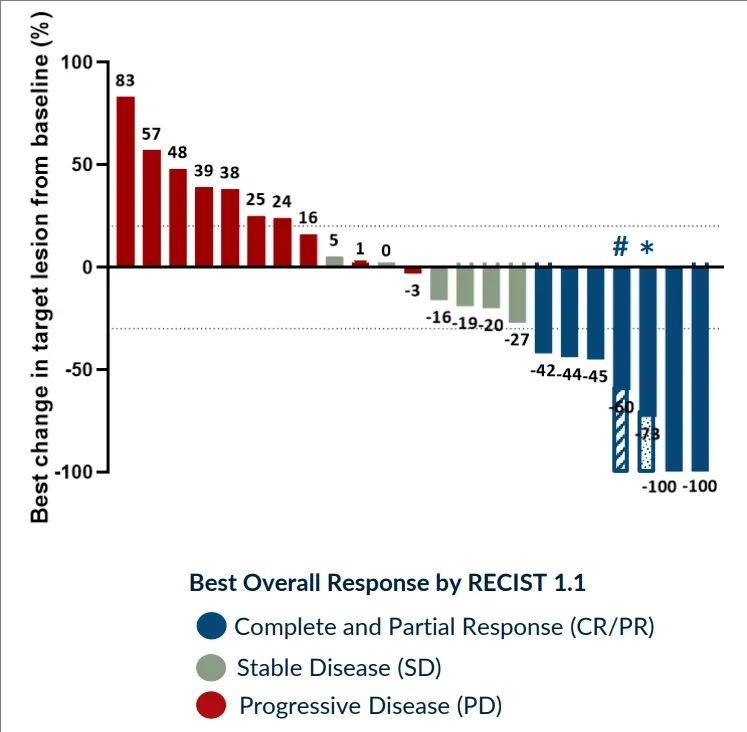
打一针激活抗癌免疫!肝癌治疗性疫苗大盘点
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
疾病控制率高达100%!2025奥希耐药
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05








![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




