突破瓶颈!攻克实体瘤的T细胞疗法最新进展盘点!(国际)
近两年,肿瘤治疗已经发生了革命性的变化,免疫治疗无疑成为了最前沿的治疗方案。除了免疫检查点抑制剂的明星代表药物PD-1,过继性细胞免疫治疗也不断涌现出“治愈性”疗法,谱写了全新的抗癌神话。但是,过继性细胞免疫疗法目前最大的瓶颈就是缺乏特异性的靶标,找到专门针对实体肿瘤的特异性靶抗原是所有免疫疗法最重要的研究方向。
近期,基于T细胞的疗法取得了前所未有的突破,不仅在实体瘤中初现曙光,还突破了免疫风暴的瓶颈,给患者带来了振奋人心的新希望。

科学家们一直在寻找只在癌细胞中表达,而在正常细胞中不表达的特异性抗原作为理想的靶标,这在成功的癌症免疫疗法中起着至关重要的作用。不幸的是,很少有癌症特异性抗原可用作实体瘤免疫治疗的有用靶标。
近期,研究发现,纽约食管鳞状细胞1(NY-ESO-1),一种癌症-睾丸抗原(CTA),常见于多种侵袭性肿瘤中的癌症相关蛋白,它在包括乳腺癌、膀胱癌、前列腺癌、黑色素瘤、NSCLC、肝细胞癌以及卵巢癌在内的多种癌症中广泛表达,表达范围为20-80%,是全身最具免疫原性的抗原之一,因此,被认为是肿瘤免疫治疗的理想靶抗原。具体为:
粘液样/圆形细胞脂肪肉瘤(89%-100%)
神经母细胞瘤(82%)
滑膜肉瘤(80%)
黑色素瘤(46%)
卵巢癌(43%)
以及其他几种肿瘤(20%-40%)。
靶向肿瘤特异性NY-ESO-1可以通过以下三种途径激活肿瘤免疫反应:
a)NY-ESO-1癌症疫苗:DC细胞摄取由NY-ESO-1衍生肽组成的癌症特异性抗原,随后呈递至肿瘤微环境。携带NY-ESO-1肽的DC疫苗直接刺激T细胞。
b) NY-ESO-1过继性T细胞疗法(TCR-T):具有NY-ESO-1 T细胞受体的CD8+或CD4+ T细胞转导的过继性T细胞治疗攻击携带NY-ESO-1的肿瘤细胞。
c)联合检查点抑制剂治疗:以上两种免疫治疗方式可以联合免疫检查点抑制剂(派姆单抗,纳武单抗,阿特珠单抗等)解除DC与T细胞以及T细胞与肿瘤细胞之间抑制信号。

六七年前,发现这种在实体瘤中特异性表达的抗原之后,免疫治疗界的泰斗,美国癌症研究所的Steven Rosenberg教授率先基于靶点NY-ESO-1,通过TCR-T技术针对晚期滑膜肉瘤和恶性黑色素瘤的临床研究。
研究表明用NY-ESO-1肽刺激的自体NY-ESO-1特异性CD4 + T细胞治疗的难治性黑色素瘤患者实现了长期完全缓解。


治疗前右肺门的原发肿瘤转移至纵隔,右胸膜,右肝叶和肝囊。在2016年1月(第43天),在第一次T细胞输注后2个月CT扫描显示原发性肺肿瘤和肝转移的客观消退,以及胸腔积液吸收和肺再扩张。四个月后病情再次进展。
NY-ESO-1靶向治疗已经取得了长足的进展。目前的研究成果推动了许多实体瘤的新临床试验,绝大多数临床试验集中于晚期实体瘤。其中美国排名第一的癌症中心MD安德森癌症中心,以及著名的加州大学洛杉矶分校综合癌症中心也正在进行肉瘤以及晚期恶性肿瘤的临床试验,想了解详情的可以直接咨询全球肿瘤医生网医学部(400-666-7998)


CAR-T是近两年涌现出的基于T细胞的“治愈性”抗癌疗法。几乎无人不知。但是,CAR T细胞疗法无法被忽视的局限性也一直困扰着科学家们,比如仅针对血液肿瘤有效,并且容易引发免疫风暴等。
重磅!针对多种儿童实体肿瘤的CAR T细胞疗法横空出世!(髓母细胞瘤/肾母细胞瘤/尤文肉瘤/横纹肌肉瘤)
新型间皮素特异性CAR-T疗法有望治疗胰腺癌!
骄傲!华人团队研发带来变革的新型CAR-T疗法!
近期,研究人员发现,自然杀伤T细胞NKT(natural killer T)细胞是一群细胞表面既有T细胞受体TCR,又有NK细胞受体的特殊T细胞亚群。是一种淋巴细胞,通过释放细胞毒性颗粒破坏癌细胞。

随后,研究人员开发了同种异体“即用型(通用型)”嵌合抗原受体 - 自然杀伤T细胞(CAR-NKT)疗法,可以克服目前自体CAR-T疗法的重大挑战,临床前数据表明,与常规CAR-T细胞不同,工程化CAR-NKT细胞不介导移植物抗宿主反应(GvHD)。并且能够:
1.分泌IL-15(白细胞介素15)以改善其活性,持久性和抗肿瘤活性

图像显示给予荷瘤小鼠的荧光素酶标记的NKT细胞
亮红色成像显示较高数量的NKT细胞,其表现出更强的扩增和持久性
经工程改造以表达IL-15的CAR-NKT细胞显示出最高的扩增和持久性
2.减少其同种异体反应并改善同种异体受者的耐受性,不会引起抗宿主反应。

来自用相同CAR转染的相同人供体的T细胞或NKT细胞
4-5周后进行分析荷瘤小鼠,CAR-NKT没有引起任何抗宿主反应
休斯顿的贝勒医学院和德克萨斯儿童医院已经基于这种工程化CAR-NKT细胞共同开展了一期临床试验,评估复发性神经母细胞瘤患儿的全新治疗方--CAR-NKT细胞治疗(代号CMD-501,由英国的细胞公司Cell Medica开发),这是有史以来第一个在多种实体肿瘤中进行试验的细胞疗法。
目前,两名患有神经母细胞瘤的儿童是第一批接受由他们自己的NKT细胞制成的转基因治疗的患者。
实验结果:第一名患者在随访4周时病情稳定,第二名患者有两个骨肿瘤,其中一个完全消失,另一个病灶正在缩小。
FDA最近批准了对患者的第二次输注,因为第一次注射的结果非常有希望。
只有两名患者不可能得出很多结论,但目前两个孩子对治疗的响应很好,并且没有明显的副作用。我们期待进一步更大规模的临床试验验证其安全及有效性。

在癌症的早期阶段,免疫系统试图通过动员淋巴细胞的特殊免疫细胞来攻击肿瘤。淋巴细胞具有识别和攻击肿瘤流量的能力,并深入肿瘤。这些细胞被称为肿瘤浸润淋巴细胞(TIL),是由免疫界泰斗Rosenberg及其团队发现的。
LN-145就是由Iovance公司研发的基于自体肿瘤浸润淋巴细胞(TIL)的疗法,这是一种基于T细胞的过继性细胞疗法(ACT)。此外过继性细胞疗法还有大家知道的用T细胞受体(TCR)或基因工程改造表达嵌合抗原受体(CAR)的自体T细胞,回输到患者体内以诱导自身免疫的抗肿瘤作用。
Iovance的创新细胞疗法是基于患者自身的TIL。这些TIL在癌症发生时会迁移到肿瘤处并且对肿瘤发起攻击。然而,通常患者体内的TIL数目不足以消灭肿瘤,而且肿瘤微环境会抑制TIL的功能。Iovance的T细胞癌症免疫疗法从患者体内获取肿瘤组织并且提取TIL,然后在体外使用IL-2细胞因子刺激TIL的扩增。这一体外刺激手段不但增加了TIL的数量,而且激活TIL的抗肿瘤能力。然后这些TIL被注回患者体内,更有效地杀伤肿瘤细胞。

▲LN-145 TIL疗法机理(图片来源:Iovance Biotherapeutics公司官网)
近期在ASCO公布的初步试验结果表明,在2019年2月4日的数据截止时,在27名复发、转移性或持久性宫颈癌患者中,LN-145疗法达到44%的客观缓解率和11%的完全缓解率。这些患者平均接受过2.4种前期疗法。值得指出的是,在中位随访期为7.4个月时,10名患者的症状得到持续缓解,中位响应持续时间还未达到。
44%(12名)的患者有效果,包括1名完全应答,9名部分应答和2个未确认的部分应答;
疾病控制率为89%;
中位随访时间为3.5个月,12例患者中有11例持续应答;
没有任何严重的副作用发生。
值得振奋的是,基于此临床试验的惊艳数据,FDA批准LN-145用于晚期宫颈癌突破性治疗,并加速其上市审批。因为,在化疗期间或之后进展的宫颈癌患者的治疗选择有限,之前报道的晚期宫颈癌化疗或免疫治疗二线治疗的应答率仅在4%-14%之间。而这款新型的非常安全的细胞免疫疗法为晚期宫颈癌患者带来了44%的应答率,并且在一些患者中表现出持久的应答效果,研究人员表示这种治疗方式可以实现长期疾病控制的希望。希望这款疗法能尽快获批上市。
癌症的难治性 | 终极解决方案--TIL技术 |
肿瘤异质性 癌症由许多不同的细胞类型组成,可以突变数百次,使它们能够逃避免疫检测 | 专门针对癌症患者的特异性抗原 针对患者特异性抗原。与许多靶向预先选择的肿瘤抗原的癌症疫苗不同,我们的技术基于患者自身的TIL,其自然靶向针对该患者肿瘤特异的抗原。 |
T细胞反应不足 肿瘤微环境使T细胞失活并抑制其生长,因此它们的数量和效力不足以产生足够的免疫反应。 | 增强T细胞数量和效力 从切除肿瘤中分离的TIL在体外扩增至数十亿个细胞,远离抑制性影响,从而能够施用有效的,高度活化的细胞。 |
免疫抑制 肿瘤细胞表面的蛋白质,如PD-1和CTLA4,抑制T细胞反应 | 控制肿瘤微环境以减少免疫抑制 在输注培养的TIL之前,患者被预处理以去除所有抑制性影响以增强治疗结果。 |

新鲜肿瘤组织通过手术从患者体内分离。
肿瘤样本被运送到GMP设施,在那里TIL被分离并繁殖,在三周内产生数十亿TIL。
患者开始一周的预处理治疗以准备接受TIL.TIL产品作为一次性疗法施用,
患者在TIL输注后立即接受多达6剂白细胞介素2(IL-2),来支持患者体内TIL的生长和激活。
首先会确定患者病例中特定的突变,之后利用突变信息找到能够最有效瞄准这些突变的T细胞,最后提取出专门患者肿瘤中细胞突变的T细胞。
这些免疫细胞经过体外培养后,重新注入到患者体内。同时,研究发现联合使用了免疫增强药物白细胞介素2和另一种“明星抗癌药”PD-1抑制剂Keytruda,Keytruda即属于另一种免疫疗法免疫检查点阻断,在某些癌症中有显著的效果。基于上述操作过程,该新疗法被认为是为患者“量身定制”。

该研究的治疗流程(图片来源:《Nature Medicine》)
目前,这款新型的免疫疗法暂未上市,但在全球范围内开展了多项针对各类实体肿瘤(非小细胞肺癌,结直肠癌,卵巢癌,黑色素瘤...)的临床试验,想参加的患者可以致电全球肿瘤医生网医学部咨询入组信息(400-666-7998)。

最后,要告诉大家的好消息是,这款疗法最快将于明年下半年上市,一旦FDA批准,这将是首款用于实体瘤的细胞免疫疗法,将给癌症患者带来巨大的生存获益,让我们拭目以待。疾病控制率89%!首个迎战实体瘤的细胞免疫疗法获FDA突破性疗法称号!

免疫肿瘤学的潜力刚刚开始实现。揭开更多的冰山将会更加详细地了解如何控制免疫反应,以及将将这些治疗手段用于临床获得益处。每天我们能看到更多的进展,我们相信这种治疗方法将在未来几年攻克更多的瓶颈,取得重大突破,让我们共同期待。

医患交流群
我们一起”愈“见未来!

肺癌 | 胃癌 | 结直肠癌 | 肝癌 |
胰腺癌 | 乳腺癌 | 食管癌 | 肉瘤 |
儿童肿瘤 | 泌尿系统肿瘤 | 妇科肿瘤 | 其他肿瘤 |
PD-1 | 基因检测 | 靶向治疗 | 质子治疗 |
免疫治疗 | 电场治疗 | 专家会诊 | 出国就医 |

扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
里程碑!mRNA-4157联合派姆单抗让
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

刚刚!"双免王炸"纳
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2025肺癌生存新希望:六大"
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
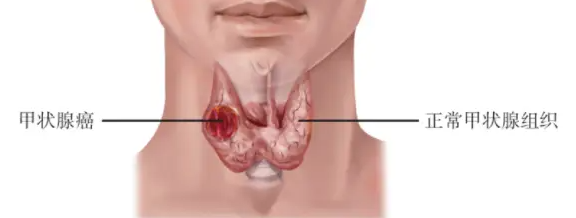
早期甲状腺癌术后五年生存率超99%,但要
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
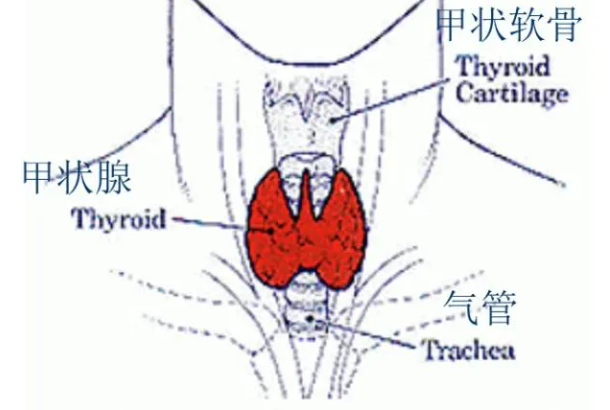
早期甲状腺癌术后五年生存率超99%!但忽
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05








![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




