2021上半年FDA批准的抗癌新药:十大癌症迎来22款新疗法
2021年上半年美国FDA批准的抗癌新药新疗法、肿瘤新药、抗肿瘤新疗法共22款覆盖十大癌症
2021年转眼过半,这半年,国内和国际上的抗癌新药井喷上市,FDA批准了共22款抗癌新疗法,包括靶向,免疫检查点抑制剂,过继性细胞免疫疗法等等,覆盖了几乎全部的癌症种类,值得一提的是KRAS和EGFR20ins两大难治性靶点打破了治疗僵局,迎来了首款靶向药物,又有很多幸运的病友们等来了新的希望和治疗选择。
全球肿瘤医生网医学部每年年中和年终都会参照美国FDA官网及美国国家癌症研究院的药品获批信息,为大家整理更新所有癌症获批的靶向药物,给大家带来战胜癌症的信心。(以下信息仅供参考,具体的用药方案需遵医嘱,也可致电全球肿瘤医生网医学部)。

非小细胞肺癌新药新疗法
01、2021年5月29日,全球首款KRAS靶向药AMG510震撼上市
2021年5月29日,针对KRAS突变有效,让我们期待了两年的“革命性抗癌药Sotorasib(AMG-510)终于获得FDA批准,提前上市!用于治疗患有KRAS G12c突变的非小细胞肺癌患者,这些患者至少接受过一种前期全身性治疗。同时,这款药物也有了自己的大名--Lumakras。
这是全球首款针对KRAS的靶向药,具有里程碑式的意义!将有无数携带KRAS突变的癌症患者迎来生存新希望!
药物名称:Sotorasib(索拖拉西布 Lumakras AMG510)
生产厂家:安进
FDA批准时间:2021年5月29日
适应症:患有KRAS G12c突变的非小细胞肺癌患者
原文链接:里程碑!全球首款KRAS靶向药AMG-510(Sotorasib)震撼上市!
02、2021年5月21日,非小细胞肺癌EGFR 20ins首款靶向药Rybrevant获批上市
2021年5月21日,FDA正式批准Rybrevant(amivantamab-vmjw,代号为JNJ6372)用于EGFR外显子20插入突变的非小细胞肺癌成年患者。这是EGFR外显子20插入突变肺癌患者的首款靶向疗法,是医学届对于这部分患者的一项重大进步,具有里程碑式的意义!
药物名称:Rybrevant(amivantamab-vmjw,代号为JNJ6372)
生产厂家:杨森(Janssen)
FDA批准时间:2021年5月21日
适应症:EGFR外显子20插入突变的非小细胞肺癌成年患者
原文链接:里程碑!FDA重磅宣布:非小细胞肺癌EGFR 20ins首款靶向药Rybrevant获批上市
03、2021年3月3日,FDA批准第三代ALK抑制剂用于一线治疗
2021年3月3日,FDA最新批准了l第三代ALK抑制剂lorlatinib用于ALK阳性非小细胞肺癌一线治疗!
劳拉替尼(Lorlatinib,LORBRENA)自问世以来就备受青睐,这款三代靶向药物的强大之处在于可以克服所有已知的ALK抗性突变并可通过血脑屏障;可抑制克唑替尼耐药的9种突变,对二代TKI药物耐药后仍有较高的有效性;同时劳拉替尼也具有较强的血脑屏障透过能力,入脑效果较强,特别适合对其他ALK耐药的晚期NSCLC患者。此次获批让劳拉替尼这个曾经的保底药物一跃成为ALK阳性患者一线首选治疗,相信将给患者带来更好的治疗效果和更大的生存获益。
药物名称:Lorlatinib(LORBRENA)
生产厂家:辉瑞
FDA批准时间:2021年3月3日
适应症:ALK阳性非小细胞肺癌一线治疗
原文链接:"钻石靶点"再添猛将!第三代ALK抑制剂劳拉替尼进军一线治疗
04、2021年2月22日,非小细胞肺癌第五款免疫疗法Libtayo获批一线治疗
2021年2月22日,FDA批准PD-1疗法cemiplimab单药一线治疗PD-L1表达>50%的晚期非小细胞肺癌患者。这意味着,非小细胞肺癌迎来了第五款免疫检查点抑制剂,cemiplimab成功冲进免疫单药一线治疗肺癌,晚期患者迎来了“去化疗”新时代!
药物名称:LIBTAYO(cemiplimab)
生产厂家:赛诺菲&再生元
FDA批准时间:2021年2月22日
适应症:PD-L1≥50%非小细胞肺癌一线治疗
原文链接:刚刚!非小细胞肺癌第五款免疫疗法Libtayo获批一线治疗
05、2021年2月3日,FDA加速批准了特普替尼上市
2021年2月3日,FDA加速批准了特普替尼(Tepotinib,Tepmetko)上市,用于治疗MET外显子14(MET ex14)跳跃突变的转移性非小细胞肺癌成年患者。
药物名称:特普替尼(Tepotinib,Tepmetko)
生产厂家:默克
FDA批准时间:2021年2月3日
适应症:MET外显子14(MET ex14)跳跃突变的转移性非小细胞肺癌成年患者
原文链接:速递|缓解率43%!肺癌迎新药,FDA加速批准特普替尼上市
胃癌和食管癌新药新疗法
06、2021年5月6日,FDA批准派姆单抗一线治疗胃癌
2021年5月6日,FDA批准了派姆单抗的新联合用药方案,用于一线治疗无法切除的局部晚期或转移性HER2阳性胃及胃食管交界处腺癌患者。
药物名称:派姆单抗
生产厂家:默克
FDA批准时间:2021年5月6日
适应症:一线治疗无法切除的局部晚期或转移性HER2阳性胃及胃食管交界处腺癌患者
原文链接:超越曲妥珠单抗!派姆单抗联合方案获FDA批准,一线治疗胃癌缓解率74%
07、2021年5月20日,FDA 批准纳武单抗用于食管癌及胃食管交界癌患者的新辅助治疗
2021年5月20日,美国食品药品监督管理局(FDA)批准nivolumab(Opdivo,百时美施贵宝公司)用于接受新辅助放化疗的完全切除食管或胃食管交界处(GEJ)癌残留患者。
药物名称:纳武单抗
生产厂家:百时美
FDA批准时间:2021年5月20日
适应症:新辅助放化疗的完全切除食管或胃食管交界处(GEJ)癌残留患者
08、2021年4月16日,FDA 批准纳武单抗联合化疗治疗转移性胃癌和食管腺癌
2021年4月16日,美国FDA批准纳武单抗(Opdivo,百时美施贵宝公司)联合含氟嘧啶和含铂化疗药物治疗晚期或转移性胃癌、胃食管交界处癌和食管腺癌。
药物名称:纳武单抗
生产厂家:百时美
FDA批准时间:2021年4月16日
适应症:联合含氟嘧啶和含铂化疗药物治疗晚期或转移性胃癌、胃食管交界处癌和食管腺癌
09、2021年3月22日,FDA 批准派姆单抗治疗食管癌或 GEJ 癌
美国食品和药物管理局批准派姆单抗(Keytruda)联合铂类和氟嘧啶类化学疗法治疗转移性或局部晚期食管或胃食管 (GEJ)(肿瘤中心位于胃食管交界处上方 1 至 5 厘米的患者) ) 不适合手术切除或根治性放化疗的癌症。
药物名称:派姆单抗(Keytruda)
生产厂家:默克
FDA批准时间:2021年3月22日
适应症:联合铂类和氟嘧啶类化学疗法治疗转移性或局部晚期食管或胃食管癌
10、2021年1月15日,Enhertu获批HER2阳性胃或胃食管癌
2021 年 1 月 15 日,美国食品和药物管理局批准 fam-trastuzumab deruxtecan-nxki(Enhertu,Daiichi Sankyo)用于既往接受过基于曲妥珠单抗治疗的局部晚期或转移性 HER2 阳性胃或胃食管(GEJ)腺癌成人患者。
药物名称:Enhertu
生产厂家:阿斯利康
FDA批准时间:2021年1月15日
适应症:既往接受过基于曲妥珠单抗治疗的局部晚期或转移性 HER2 阳性胃或胃食管(GEJ)腺癌成人患者。
胆管癌新药新疗法
11、2021年5月28日,FDA加速批准infigratinib治疗转移性胆管癌
2021年5月28日,美国食品和药物管理局加速批准 infigratinib(Truseltiq,QED Therapeutics, Inc.),这是一种激酶抑制剂,用于既往接受过治疗的、不可切除的局部晚期或转移性FGFR2融合胆管癌成人患者。
药物名称:infigratinib
生产厂家:QED Therapeutics, Inc
FDA批准时间:2021年5月28日
适应症:接受过治疗的、不可切除的局部晚期或转移性FGFR2融合胆管癌成人患者。
肾癌新药新疗法
12、2021年3月10日,FDA批准Tivozanib用于治疗复发性或难治性晚期肾细胞癌
美国食品和药物管理局批准 tivozanib(Fotivda,AVEO Pharmaceuticals, Inc.),一种激酶抑制剂,用于既往接受过两次或多次全身治疗的复发性或难治性晚期肾细胞癌 (RCC) 成人患者。
药物名称:tivozanib
生产厂家:AVEO Pharmaceuticals, Inc
FDA批准时间:2021年3月10日
适应症:既往接受过两次或多次全身治疗的复发性或难治性晚期肾细胞癌 (RCC) 成人患者。
13、2021年1月22日,FDA批准纳武单抗联合卡博替尼治疗晚期肾细胞癌
美国食品和药物管理局批准纳武单抗(Opdivo,百时美施贵宝公司)和卡博替尼(Cabometyx,Exelixis)联合作为晚期肾细胞癌(RCC)患者的一线治疗。
药物名称:纳武单抗+卡博替尼
生产厂家:百时美
FDA批准时间:2021年1月22日
适应症:晚期肾细胞癌(RCC)患者的一线治疗
子宫内膜癌新药新疗法
14、2021年4月22日,FDA 加速批准Dostarlimab-gxly用于dMMR子宫内膜癌
美国食品和药物管理局批准加速批准 dostarlimab-gxly (Jemperli, GlaxoSmithKline LLC) 用于患有错配修复缺陷 (dMMR) 复发或晚期子宫内膜癌的成年患者,含铂方案治疗后进展。
药物名称:Jemperli
生产厂家:GlaxoSmithKline LLC
FDA批准时间:2021年4月22日
适应症:患有错配修复缺陷 (dMMR) 复发或晚期子宫内膜癌的成年者,含铂方案治疗后进展
三阴乳腺癌新药新疗法
15、2021年4月7日,FDA 定期批准Sacituzumab Govitecan用于治疗三阴性乳腺癌
美国食品和药物管理局定期批准 sacituzumab govitecan(Trodelvy,Immunomedics Inc.)用于接受过两种或多种既往全身治疗的不可切除局部晚期或转移性三阴性乳腺癌 (mTNBC) 患者,其中至少一种用于转移性治疗疾病。
药物名称:Trodelvy
生产厂家:Immunomedics Inc
FDA批准时间:2021年4月7日
适应症:接受过两种或多种既往全身治疗的不可切除局部晚期或转移性三阴性乳腺癌 (mTNBC) 患者,其中至少一种用于转移性治疗疾病
晚期尿路上皮癌新药新疗法
16、2021年4月13日,FDA 加速批准Sacituzumab Govitecan用于晚期尿路上皮癌
2021 年 4 月 13 日,FDA 加速批准 sacituzumab govitecan 用于晚期尿路上皮癌。
药物名称:Trodelvy
生产厂家:Immunomedics Inc
FDA批准时间:2021年4月13日
适应症:晚期尿路上皮癌
基底细胞癌新药新疗法
17、2021年2月9日,FDA批准Cemiplimab-rwlc用于局部晚期和转移性基底细胞癌
2021年2月9日,FDA 批准cemiplimab-rwlc 用于局部晚期和转移性基底细胞癌。
药物名称:cemiplimab-rwlc
生产厂家:赛生元
FDA批准时间:2021年2月9日
适应症:晚期尿路上皮癌
多发性骨髓瘤新药新疗法
18、2021年3月31日,FDA 批准Isatuximab-irfc 用于多发性骨髓瘤
美国食品和药物管理局批准 isatuximab-irfc(Sarclisa,赛诺菲-安万特美国有限责任公司)与卡非佐米和地塞米松联合用于治疗已接受过一到三种先前治疗的复发性或难治性多发性骨髓瘤成年患者。
19、2021年3 月26 日,FDA批准Idecabtagene Viceucel治疗多发性骨髓瘤
2021年3月26日,美国FDA批准idecabtagene vicleucel(Abecma,Bristol Myers Squibb)用于治疗复发或难治性多发性骨髓瘤的成年患者,这些患者在接受过四线或更多线治疗后,包括免疫调节剂、蛋白酶体抑制剂和抗 CD38 单克隆抗体。这是 FDA 批准的第一个用于多发性骨髓瘤的基于细胞的基因疗法。
药物名称:idecabtagene
生产厂家:Bristol Myers Squibb
FDA批准时间:2021年3月26日
适应症:多发性骨髓瘤
淋巴瘤新药新疗法
20、2021年4月23日,美国食品和药物管理局加速批准Loncastuximab Tesirine-lpyl用于大B细胞淋巴瘤
2021 年 4 月 23 日,美国食品和药物管理局加速批准 loncastuximab tesirine-lpyl(Zynlonta,ADC Therapeutics SA),一种 CD19 定向抗体和烷化剂偶联物,用于治疗后复发或难治性大 B 细胞淋巴瘤的成年患者。两种或多种全身治疗,包括未另作说明的弥漫性大 B 细胞淋巴瘤 (DLBCL)、低级别淋巴瘤引起的 DLBCL 和高级别 B 细胞淋巴瘤。
药物名称:Zynlonta
生产厂家:ADC Therapeutics SA
FDA批准时间:2021 年 4 月 23 日
适应症:多发性骨髓瘤
21、2021年3月25日,Yescarta获批用于滤泡性淋巴瘤
美国食品和药物管理局加速批准 axicabtagene ciloleucel (Yescarta, Kite Pharma, Inc.) 用于接受两线或多线全身治疗后复发或难治性滤泡性淋巴瘤 (FL) 的成年患者。
药物名称:axicabtagene ciloleucel
生产厂家:Kite Pharma
FDA批准时间:2021 年3 月 25日
适应症:难治性滤泡性淋巴瘤
22、2021年2月5日,FDA批准Breyanzi用于大B细胞淋巴瘤
美国食品和药物管理局批准 lisocabtagene maraleucel(Breyanzi,Juno Therapeutics,Inc.)用于治疗接受两线或多线全身治疗后复发或难治性 (R/R) 大 B 细胞淋巴瘤的成年患者,包括弥漫性大 B-未特别指明的细胞淋巴瘤 (DLBCL)(包括源自惰性淋巴瘤的 DLBCL)、高级别 B 细胞淋巴瘤、原发性纵隔大 B 细胞淋巴瘤和 3B 级滤泡性淋巴瘤。
药物名称:Breyanzi
生产厂家:Juno Therapeutics
FDA批准时间:2021 年2 月 5日
适应症:大 B 细胞淋巴瘤
写给病友的话
除了上述写到的FDA批准的抗癌新药外,全球肿瘤医生网医学部还将持续关注国内外的抗癌前沿信息,后续还会更新最近获批的新药,请各位癌友们持续关注,想了解最新药物进展的患者可申请美国及日本专家会诊。除此之外,还有多款正在研发的抗癌新药也显示出广谱抗癌的实力。
“方舟援助计划”“可以为患者提供上市新药和未上市新药免费治疗的机会。想参加的病友可以将基因检测报告,诊断报告电子版或拍照发送至doctor.huang@globecancer.com,邮件中留下联系方式,医学部收到报告分析完毕后一个工作日内电话联系或直接致电全球肿瘤医生网医学部400-666-7998评估。
相信随着医学研究的不断深入,越来越多的新药即将研发上市,将有更多的病友跨过一个又一个5年!
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
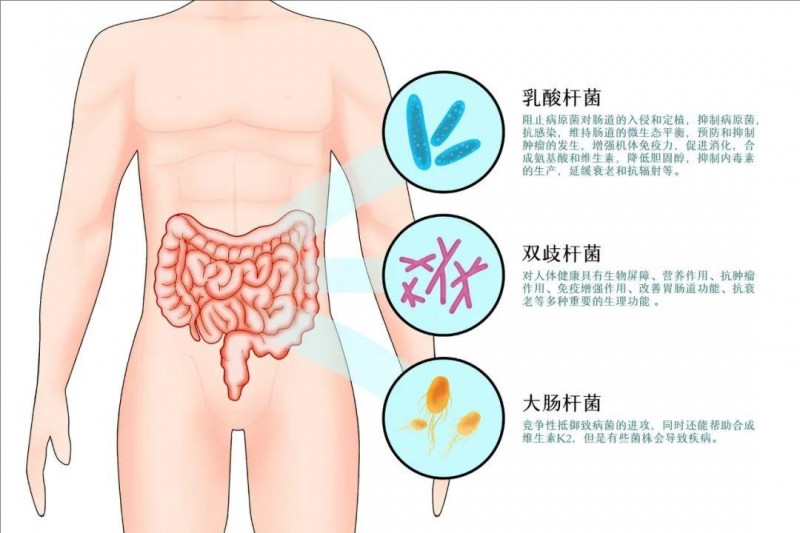
253例真实世界研究证实:益生菌联合IC
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
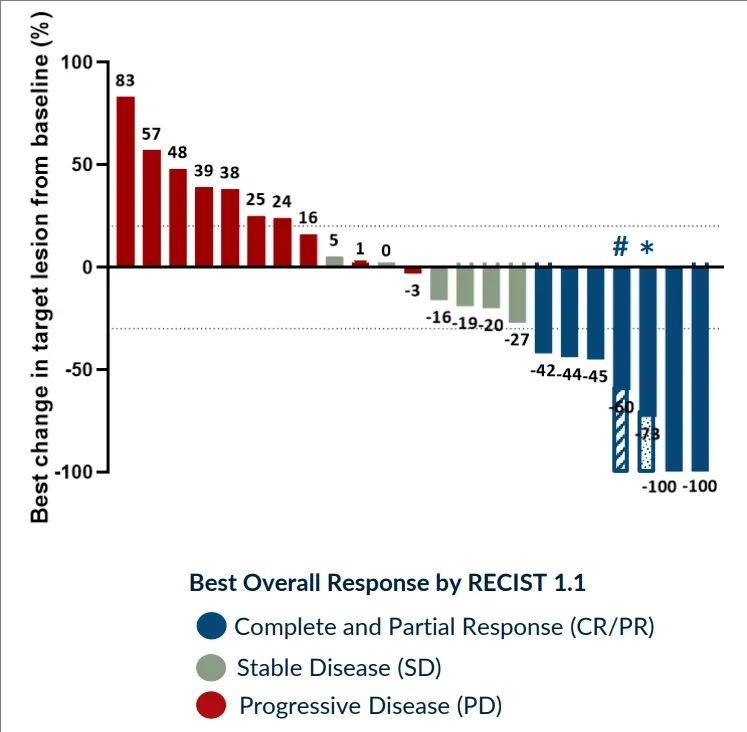
打一针激活抗癌免疫!肝癌治疗性疫苗大盘点
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
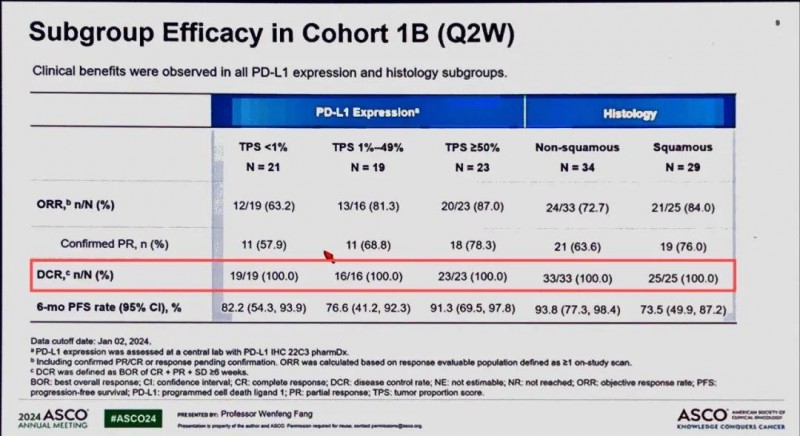
疾病控制率高达100%!2025奥希耐药
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【mRNA癌症疫苗免费招募】Vx-001
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

肝癌"黄金拍档"再发
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
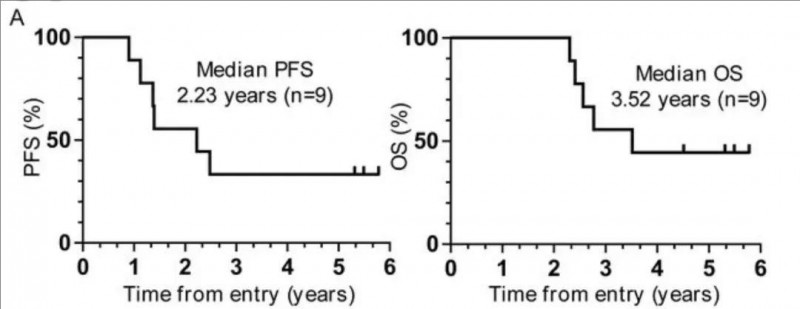
胰腺癌治疗性疫苗大盘点!最长OS超3年,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




