食道癌质子治疗的优势
食道癌质子治疗的优势
我国是食道癌(Esophageal carcinoma)全球最高发的国家之一,全球 53.3% 的食道癌发生在中国。每年我国食道癌死亡病例超过 30 万例,5 年生存率仅为 20%。NCCN 及 CSCO 指南均将放射治疗列为食道癌一线治疗的可选方案。
目前,光子治疗是食道癌患者放射治疗的主要治疗方式。光子束在杀伤肿瘤的同时,对周围正常组织如肺、心脏等造成一定程度的损害,可引起放射性肺炎等并发症。为了减轻放射治疗对正常组织的损害,医生在使用光子束时往往只能通过限制治疗的剂量来保护肿瘤周围的正常组织,但这可能影响到肿瘤放射治疗的疗效。
质子治疗是一种更为先进的放射治疗技术。质子治疗是利用质子束所特有的“布拉格峰”这一物理特性,将大部分能量在靶病灶里集中释放,可使肿瘤前方正常组织仅受小剂量照射,而肿瘤后方及侧方正常组织几乎不受照射(图 1)。从理论上来看,质子治疗较传统的光子放射治疗更高效,在达到治疗目的的同时能更好地保护周围正常组织(图 2)。质子治疗的“布拉格峰”特性为进一步提高肿瘤照射剂量提供了可能。那么,临床实践与理论推导是否一致呢?
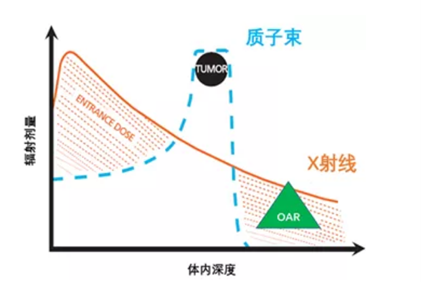
▲ 图 1 质子和光子(X 射线)的辐射剂量与人体体内深度的关系
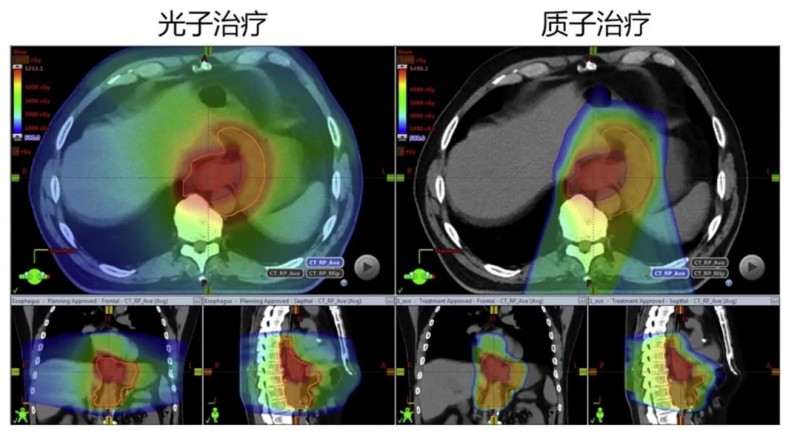
▲ 图 2
图 2 一例食道癌患者的光子治疗对比
质子治疗计划的等剂量曲线图。
红色为高剂量区(也是肿瘤所在的区域),
绿色为中等剂量区,蓝色为低剂量区。
可见质子治疗计划对周围正常组织的保护作用更为显著
美国德克萨斯大学 MD 安德森癌症中心的 Steven H. Lin 博士领衔开展了一项临床 ⅡB 期随机对照研究。该研究旨在比较光子治疗和质子治疗在治疗食道癌的疗效。研究成果发表于 2020 年美国《临床肿瘤学杂志》(J Clin Oncol)上。结果表明两种疗法的无进展生存时间(PFS, Progression-free survival)和总生存时间(OS, Overall survival)均无差异(图 3)。治疗毒性方面,后期光子治疗组的平均总毒性负荷(39.9;95%CI:26.2~54.9)为质子治疗组(17.4;95%CI:10.5~25)的 2 倍以上。在接受手术治疗的患者中,光子治疗组术后并发症评分是(19.1;95%CI:7.3~32.3)质子治疗组(2.5;95%CI:0.3~5.2)的 7 倍以上。研究者表示,与光子治疗相比,质子治疗进一步减少了正常组织的受照剂量。对于食道癌患者而言,减少心脏、肺的照射剂量就意味着可降低辐射引起的毒副反应。随着医学的进步,肿瘤患者的生存时间日益延长,因此质子治疗给患者带来的远期获益将越来越引起人们的重视。
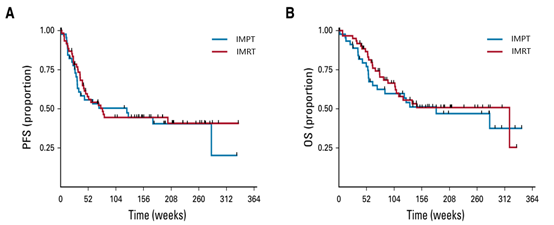
▲ 图 3. 质子治疗组与光子治疗组患者的
无进展生存时间(PFS) 和总生存时间 (OS) 的比较,
两者无差异
总之,质子治疗在不降低食道癌患者治疗效果的同时,能够减少不良事件发生率,且对患者的长期影响更小,有希望成为优于 IMRT 的首选放射治疗方案。
撰稿人:
卢卉,广州泰和肿瘤医院放疗科住院医师
袁太泽,广州泰和肿瘤医院放疗科副主任,主任医师
中国抗癌协会肿瘤微环境专业委员会组稿
作者 | GCCC
来源 | 广州泰和
参考文献
1.https://www.iarc.fr/faq/latest-global-cancer-data-2020-qa/
2. Siegel R, MillerK, Goding Sauer A, Fedewa S, Butterly L, Anderson J, et al. Colorectal cancerstatistics, 2020. CA: a cancer journal for clinicians. 2020;70(3):145-64.
3.Ono T, Wada H,Ishikawa H, Tamamura H, Tokumaru S. Clinical Results of Proton Beam Therapy forEsophageal Cancer: Multicenter Retrospective Study in Japan. Cancers.2019;11(7).
4.Garant A,Whitaker TJ, Spears GM, Routman DM, Harmsen WS, Wilhite TJ, et al. A Comparisonof Patient-Reported Health-Related Quality of Life During Proton Versus PhotonChemoradiation Therapy for Esophageal Cancer. Practical radiation oncology.2019;9(6):410-7.
5.Lin SH, HobbsBP, Verma V, Tidwell RS, Smith GL, Lei X, et al. Randomized Phase IIB Trial ofProton Beam Therapy Versus Intensity-Modulated Radiation Therapy for LocallyAdvanced Esophageal Cancer. Journal of clinical oncology : official journal ofthe American Society of Clinical Oncology. 2020;38(14):1569-79.
6.Davuluri R,Jiang W, Fang P, Xu C, Komaki R, Gomez DR, et al. Lymphocyte Nadir andEsophageal Cancer Survival Outcomes After Chemoradiation Therapy. Internationaljournal of radiation oncology, biology, physics. 2017;99(1):128-35.
7.Diehl A,Yarchoan M, Hopkins A, Jaffee E, Grossman SA. Relationships between lymphocytecounts and treatment-related toxicities and clinical responses in patients withsolid tumors treated with PD-1 checkpoint inhibitors. Oncotarget.2017;8(69):114268-80.
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
里程碑!mRNA-4157联合派姆单抗让
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

刚刚!"双免王炸"纳
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

2025肺癌生存新希望:六大"
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
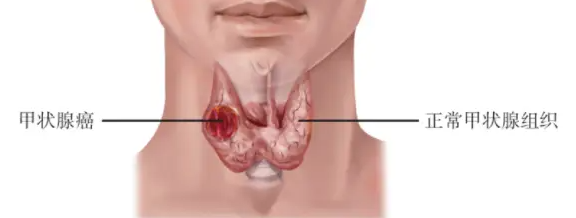
早期甲状腺癌术后五年生存率超99%,但要
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
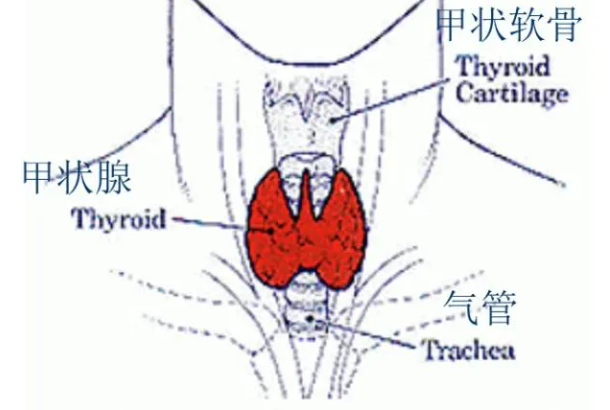
早期甲状腺癌术后五年生存率超99%!但忽
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




