新型免疫检查点TIGIT抑制剂与PD-L1单抗联用,在肺癌患者中展现强劲疗效
什么是TIGIT靶点,TIGIT抑制剂Tiragolumab联合PD-L1抑制剂阿托珠单抗治疗肺癌效果强烈
关键词:免疫检查点;TIGIT抑制剂;PD-L1单抗
免疫检查点抑制剂作为最成功的免疫疗法之一,改变了很多癌症患者的命运,尤其是多种PD-1/PD-L1单抗的成功获批,鼓舞着更多研究者在这一领域的深入研究。
近期,一个新的免疫检查点TIGIT引起了研究界的强烈兴趣。
什么是TIGIT靶点
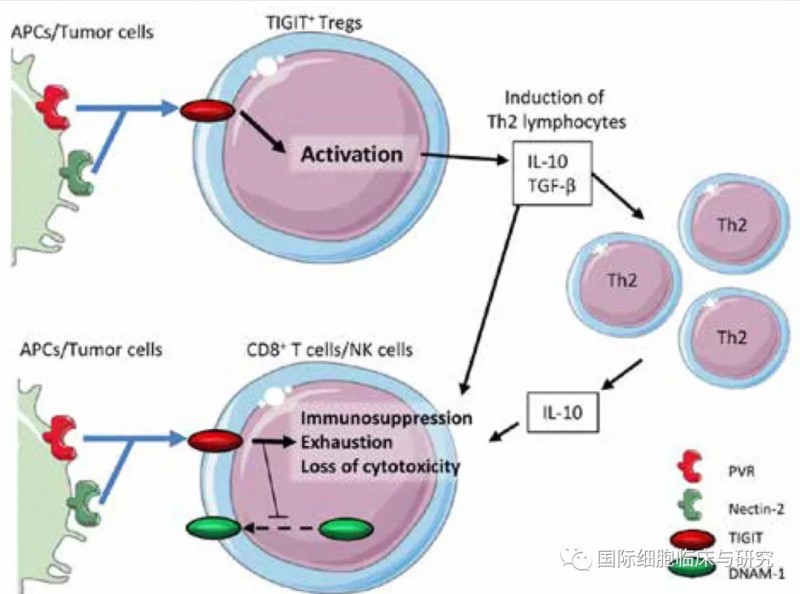
TIGIT是一种抑制性免疫检查点,主要在自然杀伤细胞(NK)和T细胞(免疫反应的主要效应物)上表达。与配体结合后,TIGIT通过其抑制性基序将抑制信号传递到细胞中,并使一系列激活下游信号的细胞蛋白失活,在抑制抗肿瘤反应中起着核心作用。
研究表明,TIGIT通过多种潜在机制下调免疫应答,在癌症免疫周期的多个步骤中起作用。除了直接抑制NK和T细胞的激活外,TIGIT还影响表达CD155的细胞(主要是树突状细胞),阻止其成熟并触发免疫抑制细胞因子IL-10的产生,从而间接抑制效应T细胞的反应。
Tiragolumab(以前称为MTIG7192A)是一种完全人源性的单克隆抗体,可阻断TIGIT与其配体PVR和CD226的结合。第一阶段的临床研究中GO30103(NCT02794571)显示Tiragolumab可作为单一疗法,也可与阿替利珠单抗联合用于晚期实体癌。其结果已在美国癌症研究协会虚拟年会上发表。
在剂量递增部分的试验中,Tiragolumab单药治疗24例,与阿替利珠单抗联合治疗49例。尽管有4例患者的肿瘤缩小,但tiragolumab单药治疗没有客观反应。联合使用组,有10例患者的肿瘤缩小,包括5例部分缓解(PR)。
在一个扩展队列中,对13名PD-L1阳性(≥1%)的非小细胞肺癌(NSCLC)且未接受免疫治疗的患者进行了联合治疗。6例患者(46%)有反应,包括2例完全缓解(CR)和4例部分缓解(PR),疾病控制率(DCR)为85%。
Tiragolumab具有良好的耐受性,并且在全部研究剂量下均具有可接受的安全性。
Tiragolumab与PD-L1单抗联用显示出强烈的抗肿瘤效果
基于前期研究的良好数据,研究者开始了2期CITYSCAPE试验(GO40290; NCT03563716),试验是针对新诊断为PD-L1阳性(肿瘤比例评分[TPS]≥ 1%的肿瘤细胞)非小细胞肺癌,还要求无EGFR或ALK突变。试验组Tiragolumab(600 mg q3w)加PD-L1单抗(阿托珠单抗),对照组为阿托珠单抗加安慰剂。
根据2020年美国临床肿瘤学会虚拟会议提供的研究结果,在最新的分析中,Tiragolumab与阿妥珠单抗联合治疗组客观缓解率(ORR)和中位无进展生存期(PFS)均得到改善。
在10.9个月的中位随访中,在Tiragolumab与阿妥珠单抗联合治疗组中意向治疗人群(N = 135)的ORR为37%,而单独使用阿替利珠单抗的ORR为21%。Tiragolumab与阿妥珠单抗联合治疗组中位PFS为5.55个月,单独使用阿替利珠单抗的中位PFS3.88个月。
在一项探索性分析中,Tiragolumab联合用药对PD-L1高表达(TPS≥50%)患者(n = 58)客观缓解率为66%,而单独使用阿替利珠单抗则为24%。联合用药未达到中位无进展生存期(NR),而阿替利珠单抗为4.11个月。
并且联合治疗耐受性良好,联合治疗组免疫相关不良事件(irAEs)的发生率更高,这些主要涉及皮疹和输注相关反应,严重程度为1级或2级。
2020年3月,罗氏(Roche)已开启了一项3期临床试验(SKYSCRAPER-01;NCT04294810),评估Tiragolumab(RG6058)与PD-L1抑制剂阿替利珠单抗(Tecentriq)联合使用,作为针对局部晚期不可切除或转移性非小细胞肺癌患者的一线治疗方法( NSCLC)。目前该试验正在包括中国在内的全球多中心招募患者,有符合适应证的患者可私信小编或登录全球肿瘤医生网提交资料评估临床获益情况,将有专业医生为大家提供帮助。
入选标准:
组织学或细胞学记录的局部晚期或复发性NSCLC不适合进行或不进行放化疗的治愈性手术;和/或确定性放疗,或转移性IV期非鳞状或鳞状NSCLC;
既往没有转移性非小细胞肺癌的全身治疗;
东部合作肿瘤小组(ECOG)绩效状态为0或1;
通过PD-L1免疫组化测定确定的肿瘤PD-L1表达;
根据实体瘤反应评估标准,版本1.1(RECIST v1.1)的可测量疾病;
足够的血液学和终末器官功能。
我们希望这一联合疗法的临床研究能够顺利完成,并尽快获批上市,为肺癌患者带来更大的生存获益,也为其他癌种的治疗提供新的思路。
小编寄语
很幸运遇见充满爱的你,转发文章让更多被癌症折磨的病友看到,将幸运传递下去。
您的举手之劳可能会改变一个不幸之人的命运。
参考资料
https://www.onclive.com/view/interest-builds-for-targeting-tigit-checkpoint
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
早期膀胱癌术后五年生存率高达90%,这五
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

警惕!乳腺癌复发偏爱这3大人群!术后一定
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【实体瘤溶溜病毒免费招募】溶瘤病毒Ml(
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
从多处转移到完全缓解!新型CAR-T细胞
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
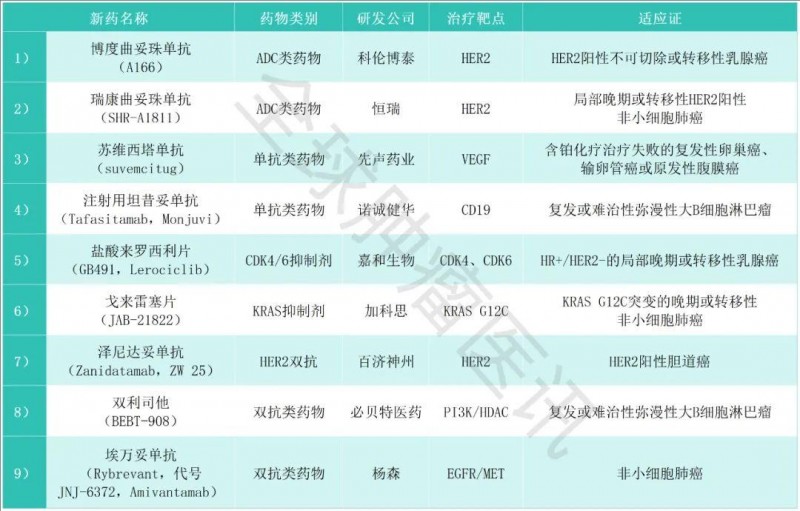
救命药加速入场!2025第二季度9款抗癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




