2025 AACR抢先看:六大TIL疗法强势突围,CR级疗效燃爆全场,暴击肺癌、肝癌、黑色素瘤等实体瘤
2025 AACR抢先看:六大TIL细胞疗法强势突围,CR级疗效燃爆全场,暴击肺癌、肝癌、黑色素瘤等实体瘤
2025年4月25日至30日,一场改写癌症治疗格局的巅峰盛会——美国癌症研究协会(AACR)年会,即将在美国芝加哥震撼启幕!作为全球历史最为悠久、规模首屈一指的肿瘤研究学术殿堂,AACR与欧洲肿瘤内科学会(ESMO)、美国临床肿瘤学会(ASCO)并驾齐驱,并称为"全球三大癌症学会"。这不仅是临床前沿研究成果的璀璨舞台,更是见证着全球抗癌研究的发展与变革!
而在本届年会上,国内外多项TIL细胞疗法正蓄势待发,以雷霆之势重磅登场!这些研究成果不仅为抗癌领域注入新动力,也为实体瘤患者带来了更多治疗希望。下面医学部小编将盘点本次会议中值得关注的几款TIL疗法,以供癌友们参考,增加大家战胜癌症的信心!
2025 AACR焦点:六款TIL细胞疗法强势突围,解锁抗癌新可能
01、砂砾生物:GT316(中国)

摘要号及会议时间:
①会议摘要号:3192.GT316:a next-generation TIL therapy identified through genome-wide CRISPR screening with promising efficacy in advanced solid tumors(译文:GT316:下一代基因编辑型TIL疗法的临床前研究和临床数据更新,在晚期实体瘤中展现出显著疗效)。
②会议时间:2025年4月28日14:00-17:00。
前沿数据抢先看:
肿瘤浸润淋巴细胞(TIL)过继细胞疗法在晚期黑色素瘤治疗领域已取得显著成效,但如何将其成功应用于其他实体瘤,并进一步提升临床治疗效果,仍是当前医学界亟待突破的重大难题。为攻克这一难关,沙砾生物凭借创新技术研发出全基因组CRISPR/Cas9筛选平台ImmuTFinder®,旨在挖掘能够增强TIL功能、拓展其治疗潜力的关键免疫调节靶点。而GT316正是沙砾生物基于ImmuTFinder®平台,通过多轮严谨的体内外筛选与验证,开发出的CRISPR/Cas9-dualKO抗衰竭TIL产品。
在首次人体试验(NCT06145802)中,GT316展现出优异的安全性与初步抗肿瘤活性,交出了一份令人瞩目的答卷。其中,一例难治性宫颈癌患者在输注GT316仅4周后,便达到完全缓解(CR)状态。治疗前,该患者阴道内24mm的转移性病灶,在第38周的放射影像检查中已实现100%缩小(详见下图)。这一突破性成果为实体瘤治疗带来新的曙光!
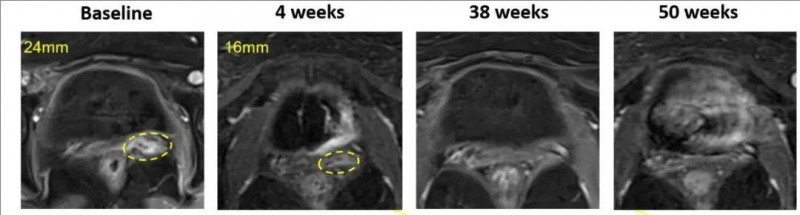
▲图源“ASCO”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
02、砂砾生物:GT300(中国)

摘要号及会议时间:
①会议摘要号:865.Engineering a next-generation dual-knockout TIL product with AaCas12b nuclease editing(译文:利用AaCas12b核酸酶编辑技术设计下一代双敲除TIL产品)。
②会议时间:2025年4月27日14:00-17:00。
前沿数据抢先看:
GT300是沙砾生物依托天泽云泰AaCas12bMax技术平台支持,制备的下一代基因编辑型TIL产品,采用CRISPR/AaCas12bMax进行设计,以破坏通过全基因组CRISPR筛选确定的两个关键免疫调节靶点,这种设计旨在增强TIL功能,并克服抑制性肿瘤微环境(TME)。GT300TIL产品具有较高的编辑效率、极少的脱靶事件,拟用于卵巢癌、结直肠癌等冷肿瘤的治疗。
相比传统SpCas9编辑的TIL产品,AaCas12bMax技术赋予GT300显著的性能优势:在大规模生产环节,其细胞扩增速率提升3-5倍,细胞活力显著增强;同时展现出更优的干细胞特性,有效抑制细胞耗竭与凋亡。体内实验数据显示,输注后的GT300细胞仍能保持优异的扩增能力,印证了该编辑技术大幅降低了细胞遗传压力。这些特性使GT300兼具高效基因编辑能力、卓越安全性,以及更出色的细胞存续与适应性能。
目前,GT300的首次人体临床试验正在中国进行中,以评估GT300在晚期实体瘤(主要是III期或IV期不可切除或转移性实体瘤)中的初步安全性和有效性。
中国患者如何寻求TCR-T疗法帮助
目前,国内多家癌症中心启动TCR-T细胞疗法临床实验,针对多种晚期实体瘤进行临床招募。
1、年龄在18岁至75周岁,晚期复发的经病理学或组织学证实的胰腺癌及结直肠癌;
2、经研究者判断无可适用的治疗方案,或无法耐受目前可用的治疗方案;
3、经HLA-A分型确认含有HLA-A*02:01亚型且肿瘤PRAME 表达经IHC检测阳性;
4、经HLA分型确认含有HLA-A*11:01亚型且肿瘤KRAS G12V阳性;
5、依照RECIST 1.1标准,至少有一个可以进行影像学测量评估的肿瘤病灶。
想寻求TCR-T及其他国内外新抗癌治疗帮助,且经济条件允许的情况下,可以先将病历提交至医学部进行初步评估,一旦审核通过,有机会获得”天价“疗法免费治疗的机会。
03、华赛伯曼:FAST-TIL(中国)

摘要号及会议时间:
①会议摘要号:CT114. FAST TIL:A more effective cell therapy product with great potential for the treatment of solid tumors(译文:FAST TIL:一种更有效的细胞治疗产品,在实体肿瘤治疗方面具有巨大潜力)。
②会议时间:2025年4月28日14:00-17:00。
前沿数据抢先看:
除了在2025 AACR大会上即将公布的FAST TIL数据外,华赛伯曼公司研发的一款自体天然加强TIL产品——HS-IT101注射液,其新药IND申请已于2023年11月29日,获中国国家药品监督管理局(NMPA)批准(受理号:CXSL2300599),用于晚期实体瘤的治疗。
04、君赛生物:创新TIL细胞疗法(中国)

摘要号及会议时间:
①会议摘要号:5827/3-Hydroxychloroquine increases the tumor killing efficiency via elevating the membrane MHC-I protein levels of tumor cells(译文:羟氯喹通过提高肿瘤细胞膜MHC-I蛋白水平提高肿瘤杀伤效率)。
②会议时间:2025年4月29日 14:00-17:00。
前沿数据抢先看:
羟氯喹(HCQ)最初是作为抗疟药开发的,近年来因其抑制自噬过程、诱导细胞凋亡以及抑制癌细胞CXCL12/CXCR4通路的分子机制,被用于治疗多种癌症。既往研究发现,自噬通过降解主要组织相容性复合体I类(MHC-I)来促进胰腺癌的免疫逃逸,因此我们推测HCQ治疗可能通过抑制自噬来恢复甚至提高肿瘤细胞的MHC-I水平,从而有益于肿瘤浸润淋巴细胞(TIL)的免疫治疗。HCQ可通过提高肿瘤细胞膜MHC-I蛋白水平显著提高肿瘤杀伤效率,但不影响TILs的增殖。此外,其对表面PD-L1的影响不显著,优于IFN-γ。这些结果可为TILs过继细胞治疗前HCQ预处理提供临床前证据(NCT06375187)。
此外,君赛生物自主研发的全球首款无需清淋和白细胞介素-2注射的天然TIL细胞新药——GC101,在晚期实体肿瘤治疗中展现出卓越疗效。临床数据显示,其客观缓解率(ORR)超过35%,4例患者实现完全缓解(CR),其中最长无瘤生存时间已超3年,为患者带来了持久的生存希望。
尤为亮眼的是,一位同时存在淋巴结、胸膜及骨转移的晚期肺腺癌患者,在接受GC101回输治疗后,增强CT影像显示靶病灶缩小36%,达到部分缓解(PR)。令人振奋的是,在回输后的24周内,该患者未接受任何其他治疗,肿瘤病灶仍持续缩小(详见下图),展现出GC101强大且持久的抗肿瘤活性,为晚期实体瘤治疗开辟了全新路径!
▼该患者在接受TIL回输治疗前,以及治疗6周、12周、18周、24周的CT对比
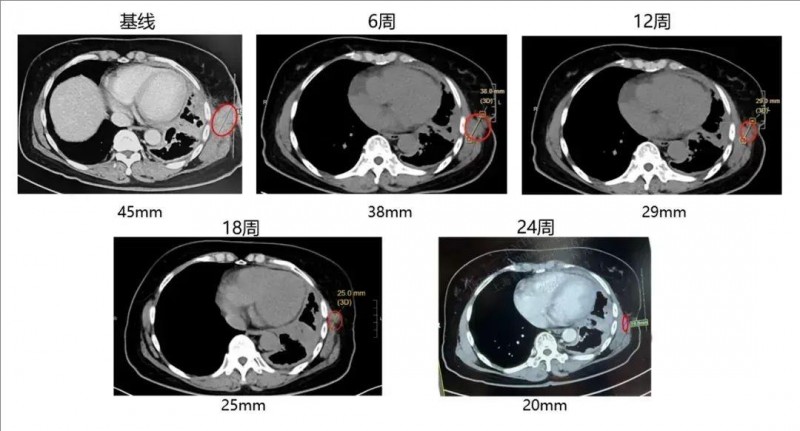
▲图源“JUNCELL”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
05、Iovance:IOV-5001(外国)

摘要号及会议时间:
①会议摘要号:4863 / 13 - IOV-5001, autologous tumor-infiltrating lymphocytes (TIL) armored with inducible membrane-tethered IL-12, shows enhanced antitumor efficacy with an improved cellular state[译文:IOV-5001,一种自体肿瘤浸润淋巴细胞(TIL),带有可诱导的膜系 IL-12,表现出增强的抗肿瘤功效,并改善了细胞状态]。
②会议时间:2025年4月29日 09:00-12:00。
前沿数据抢先看:
经基因工程改造后能分泌IL-12的自体肿瘤浸润淋巴细胞(TIL),在转移性黑色素瘤治疗中展现出显著的临床疗效。然而,循环中IL-12水平升高引发的全身毒性问题,极大限制了该疗法的广泛应用。
为突破这一困境,新一代TIL疗法IOV-5001应运而生。这是一种经过基因工程改造的可诱导型结合型IL-12TIL细胞疗法,通过特殊设计,使其仅在抗原结合后诱导表达膜系IL-12(TeIL12),从而将IL-12的活性精准限制在肿瘤微环境内,有效规避全身毒性风险。
临床前研究数据显示,IOV-5001在体外展现出强大的抗肿瘤活性;美国国家癌症研究所开展的临床试验也证实其治疗效果优于传统疗法。目前,相关IND授权研究正在推进,公司计划于2025年正式提交IND申请。
除了IOV-5001外,Iovance公司的另一款TIL产品——Lifileucel(LN-144,Amtagvi),已于2024年2月16日,获美国食品和药物管理局(FDA)批准上市,用于治疗既往接受过 PD-1 抗体治疗的不可切除或转移性黑色素瘤成人患者,它是全球首款上市的TIL疗法,为实体瘤治疗开启新纪元,具有里程碑式的重大意义!
Lifileucel的获批上市基于一项代号为C-144-01 的Ⅱ期临床试验的卓越数据,结果显示:客观缓解率(ORR)达到31.4%,疾病控制率(DCR)高达77.8%!这意味着近80%的极晚期黑色素瘤患者肿瘤出现不同程度缩小或控制稳定!
除在黑色素瘤治疗领域表现出色外,Lifileucel 在转移性非小细胞肺癌(mNSCLC)的治疗中同样成绩亮眼。
《Cancer Discovery》杂志发布的2期临床数据显示,对于免疫检查点抑制剂(ICI)耐药的晚期mNSCLC患者,Lifileucel治疗的客观缓解率(ORR)达21.4%(6/28),79.2%(19例)的患者实现肿瘤负荷下降;部分缓解率(PR)达17.9%(5/28),另有42.9%(12/28)的患者病情稳定(SD)。其中,1例患者(患者3B-02)更是达到完全缓解(CR),展现出Lifileucel强大的抗癌潜力。
尤为值得关注的是,一名41岁、携带KRASG12D突变的IV期粘液性肺腺癌男性患者,其肿瘤突变负荷(TMB)仅为3.3mut/Mb,且PD-L1表达为0%。在接受Lifileucel治疗12周后,依据RECISTv1.1标准评估,其部分缓解(PR)率高达81%(详见下图),这一突破性疗效为特定基因分型的肺癌患者带来了新的治疗希望。
▼该患者接受TIL治疗前、治疗后6周的CT扫描对比
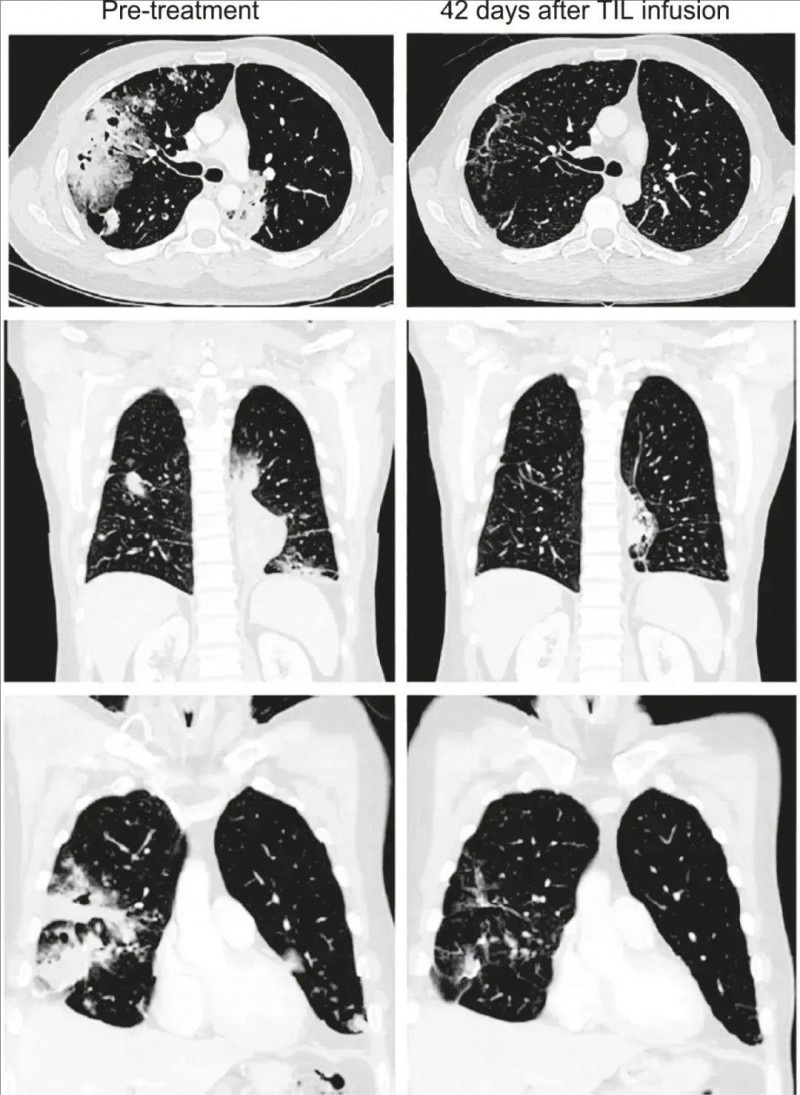
▲图源“Cancer Discov”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
06、百吉生物:CAR-TIL(中国)

摘要号及会议时间:
①会议摘要号:873.2-deoxy-D-glucose sensitizes the antigen recognition of chimeric antigen receptor-expressing tumor-infiltrating lymphocytes toward hepatocellular carcinoma cells(译文:脱氧-D-葡萄糖可增强嵌合抗原受体表达的肿瘤浸润淋巴细胞对肝细胞癌细胞的抗原识别敏感性)。
②会议时间:2025年4月29日 14:00-17:00。
前沿数据抢先看:
肿瘤浸润淋巴细胞(TIL)作为肿瘤组织内的异质性淋巴细胞群体,由多种识别肿瘤或病毒抗原的特异性T细胞克隆组成。目前,TIL疗法已获批用于晚期黑色素瘤治疗,常配合大剂量白细胞介素2(IL-2)使用。然而,肿瘤组织获取困难、肿瘤反应性T细胞个体差异显著,以及IL-2输注引发的毒性问题,严重制约了TIL疗法在更多肿瘤类型中的推广应用。
为解决个体差异问题,研究团队尝试构建表达嵌合抗原受体(CAR)的TIL,靶向肝细胞癌(HCC)细胞表面糖蛋白。但HCC细胞表面糖蛋白的高度糖基化,会掩盖单链抗体识别的关键肽表位。已有研究表明,葡萄糖/甘露糖类似物2-脱氧-D-葡萄糖(2-DG)处理胰腺癌细胞,可阻断细胞表面N-糖基化合成,增强CAR-T细胞活性;同时,2-DG处理T细胞能提升其抗肿瘤能力,并促进IL-2R在细胞表面的稳定表达。
研究数据显示:采用1~10mM浓度的2-DG预处理HCC细胞系,可呈剂量依赖性增强糖蛋白3(GPC3)的抗体识别效率,但对CD133/CD44v6与单克隆抗体的结合无明显促进作用。经2-DG预处理的GPC3阳性HCC细胞,更易被CAR-TIL杀伤,并促使CAR-TIL释放更多干扰素γ(IFNγ),大幅提升CAR-TIL对GPC3阳性HCC细胞的杀伤活性。这一发现为TIL疗法优化提供了新思路!
除了这款CAR-TIL外,百吉生物(Biosyngen)研发的全球首款针对肝癌的TIL产品——BST02注射液,在Ⅰ期临床试验中取得重大进展。试验中有一位肝癌患者在接受BST02注射液治疗18周后,靶病灶完全消除(CR),且癌栓显著缩小。目前,该位受试者无疾病进展生存时间(PFS)达到162天(约24周)。
小编寄语
TIL疗法自1988年初次尝试用于临床以来,已有30多年的发展历程,凭借其独特的优势,在黑色素瘤、肺癌、宫颈癌、乳腺癌、头颈部肿瘤等多种实体瘤领域,取得了显著的疗效,是当之无愧的实体瘤“大杀器”!
不过,癌症作为一种高度突变且极度复杂的疾病,很难仅靠单一治疗手段达到预期效果。目前仍以手术、放化疗等传统治疗手段为主。在此基础上,存在TIL细胞制备条件的患者,可在初次手术及放化疗前,及时冻存TIL细胞,用于后续治疗,以预防复发/转移,或在癌症晚期其他措施束手无策时,作为末线补救措施,为患者赢得“一线生机”。想寻求TILs疗法或国内外其他抗癌新技术(如CAR-T、TCR-T、NK细胞疗法等)帮助的患者,可将近期病理报告、治疗经历等资料,提交至医学部,进行初步评估。
参考资料
[1]Guo J,et al.A first-in-human study of CRISPR/Cas9-engineered tumor infiltrating lymphocytes (TILs) product GT316 as monotherapy in advanced solid tumors[J]. 2024.
https://meetings.asco.org/abstracts-presentations/233956/poster
[2]Liu Y,et al.686 Trial in progress: first-in-human study of next-generation Dual-KO TIL therapy GT300 in patients with advanced solid tumors[J]. 2024.
https://jitc.bmj.com/content/12/Suppl_2/A787
[3]https://www.abstractsonline.com/pp8/#!/20273
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
肠癌患者找到"重生密码&quo
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

绝境逆袭!NY-ESO-1 TCR-T疗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
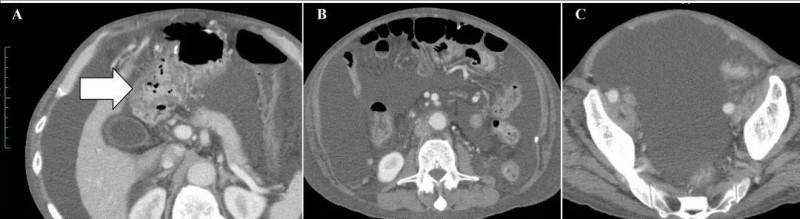
结直肠癌六大治疗性疫苗重磅集结!最长控瘤
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
253例真实世界研究证实:益生菌联合IC
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
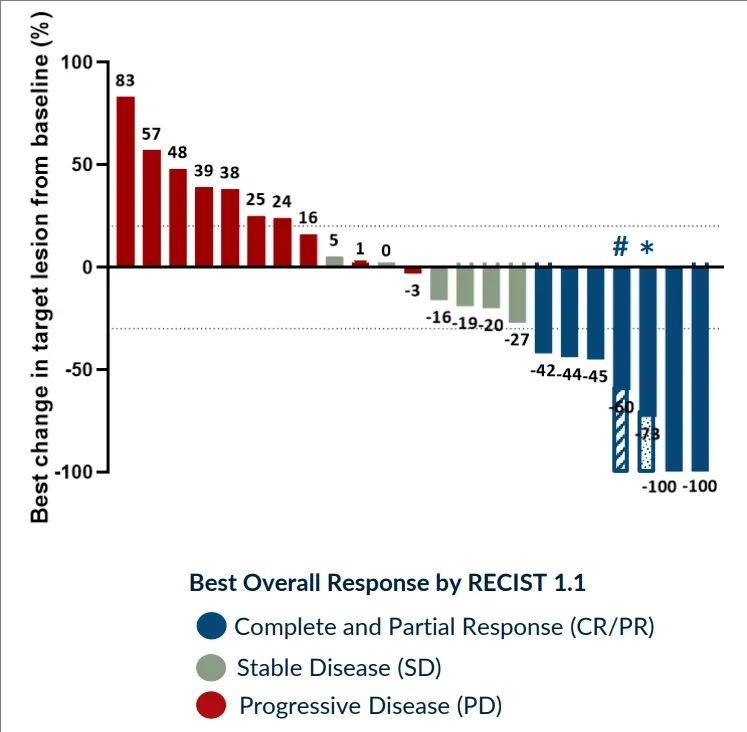
打一针激活抗癌免疫!肝癌治疗性疫苗大盘点
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
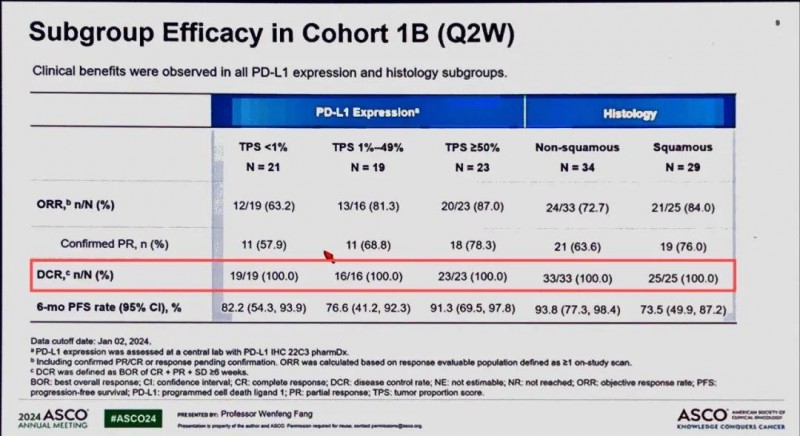
疾病控制率高达100%!2025奥希耐药
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




