脱胎于基因工程技术!以病毒为"靶",TCR-T开启癌症治疗新思路!
新"肿瘤病毒疗法"-以病毒为"靶",TCR-T疗法开启癌症治疗新思路
T细胞,全称T淋巴细胞,这是我们人体内最强大的免疫“战士”群体之一。它们的“职责”非常多,不同类型的T细胞有不同的分工,对外可清除细菌病毒、对内可清除衰老及病变的细胞,工作时释放淋巴因子增强免疫效应,工作结束之后还能转化为记忆T细胞、等待下一次遇到相同的病原体时再投入“战斗”。
癌细胞也是一种内源的“病原体”,T细胞能够识别并杀伤它们。但很多情况下,成规模的癌细胞能抑制T细胞的功能,逃避T细胞的识别,或者抑制它们的活性,从而避免被杀死。
面对这些狡猾的癌细胞,“单纯”的T细胞显得有些“力有不逮”。大部分情况下,人的免疫系统很难铲除已经发展至巅峰的(晚期)癌症。但也有一些专门为抗癌而生的、经过人为修饰的免疫细胞,就像一支专业的人体“扫黑除恶”队伍,能够强力清除这些顽固的癌细胞。
大名鼎鼎的CAR-T细胞疗法(嵌合抗原受体T细胞疗法)就是其中之一。但这一次,我们主要为大家讲解的却是另一类脱胎于基因工程技术的T细胞疗法,TCR-T疗法。
脱胎于基因工程技术的新型细胞疗法
TCR-T疗法是一类细胞受体基因工程改造的T细胞疗法。TCR的全称是T细胞抗原受体,是存在于T细胞表面的特征性标志物,能够与CD3结合,主要发挥着识别抗原的作用。
通过细胞基因工程改造,这些TCR-T细胞拥有了比T细胞更加强大的“亲和力”与“战斗力”。它们能够更准确、高效地识别除癌细胞,并能够引发更加强大的抗肿瘤效应。
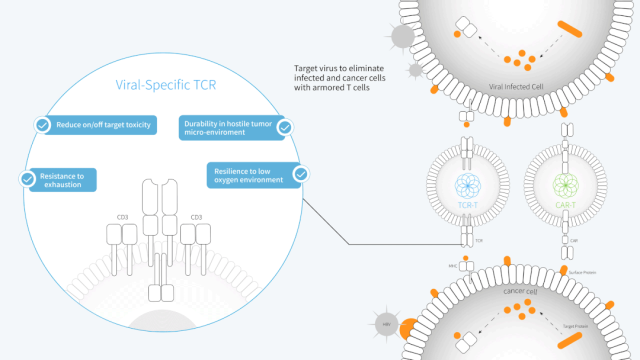
图片来源:SCG官方网站
同为基因工程改造的T细胞疗法,CAR-T和TCR-T两种疗法之间有非常多的共同点。比如,这两种疗法都致力于大幅提升T细胞对于癌细胞的识别能力和杀伤力,并且都会借助某些“靶标”来达到这一目的。
但两种疗法也存在一定的差别。整体来说,CAR-T疗法的疗效更好,但TCR-T疗法的靶标范围更加广,有望应用于一些CAR-T难以发挥作用的患者。目前为止,TCR-T疗法主要运用在黑色素瘤、肝癌、卵巢癌等肿瘤的治疗当中。
2006年,Motgan Richard等专家对17例黑色素瘤患者,使用了针对MART-1的TCR-T制剂回输治疗,2例患者的肿瘤消退;2009年,Johnson等使用改进的TCR-T制剂治疗黑色素瘤患者,这一次肿瘤消退的患者比例提升到了30%。
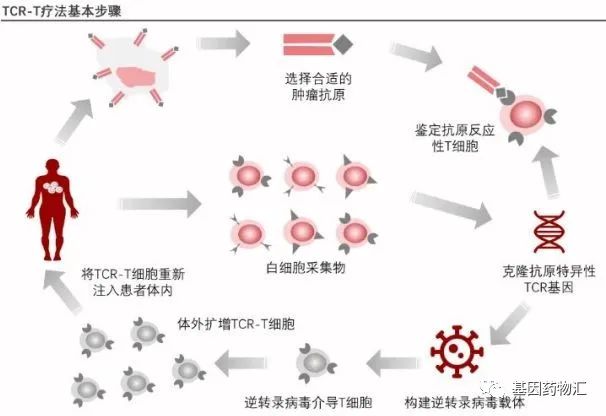
图片来源:头豹
从发展的阶段来说,CAR-T疗法的发展更加快速,目前国内已经有CAR-T制剂获得批准上市,而TCR-T疗法仍基本处于研究阶段,但前景被许多人看好,是一个非常出色的“潜力股”。
以病毒为"靶",TCR-T开启细胞疗法新思路
从现有的试验研究数据来看,CAR-T疗法在血液系统肿瘤方面的进展颇丰,在各类B细胞淋巴瘤、T细胞淋巴瘤、白血病以及骨髓瘤的治疗当中取得了非常出色的疗效;但在实体瘤领域,CAR-T疗法的进展却可以称得上是“举步维艰”,仅有几个靶点、几款疗法以及很少的适应症当中得到了不错的数据。
究其原因,癌症病灶的内环境是一者,T细胞很难深入其中;靶点选择的匮乏也是一者。对于前者,肿瘤浸润淋巴细胞(TILs)疗法潜力不错,甚至可以说是“如鱼得水*”;而对于后者,靶标范围更广的TCR-T疗法成为了新的选择。
*“如鱼得水”主要指,肿瘤浸润淋巴细胞的主要存在环境为肿瘤病灶的内环境,是一类能够深入病灶内部的免疫细胞,因此使用这类细胞在这样的环境中发挥治疗效果,如同将鱼放回水流中。
1、以乙肝病毒(HBV)为靶标
许多研究已经证实,具备乙肝病毒(HBV)特异性的TCR-T细胞,完全可以应用于与乙肝相关的肝癌的治疗之中。
根据2019年发布的论文,研究者在小鼠身上完成了初步的试验。他们在小鼠身上建立了符合需求的模型(HLA-A2+的人类肝癌模型),并通过抗体治疗取得了HBV感染得到了控制的患病小鼠模型。
TCR-T细胞的主要治疗效果在于,这类细胞能够直接杀伤被HBV感染的细胞,因此可以在HBV感染的肝癌的治疗中发挥非常好的效果。
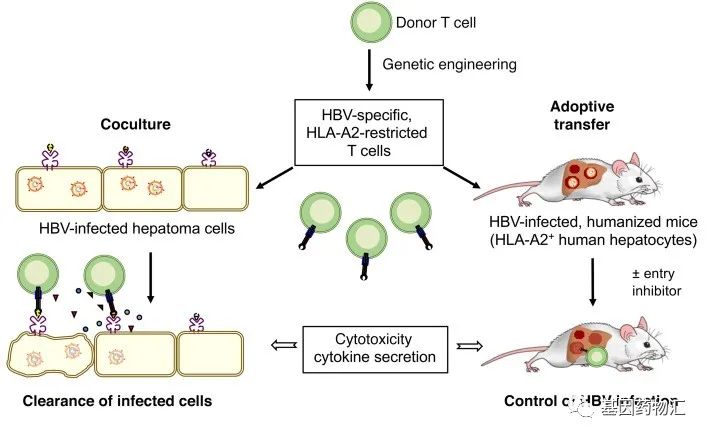
通过使用4G S20和6K C18两种特异性的TCR-T细胞治疗,研究者观察到了非常明显的差异:不论是哪一种类型的制剂,都能够非常明显地杀伤小鼠体内的癌细
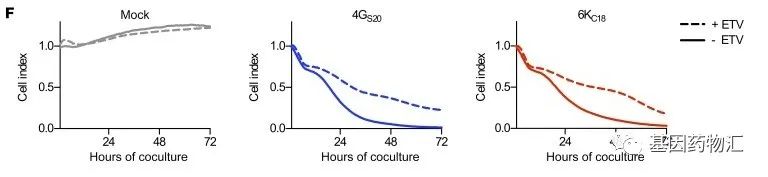
蓝色曲线及点为4G S20组,红色曲线及点为6K C18组,灰色曲线及点为对照组;可以明显地看出,TCR-T细胞对于癌细胞有非常明显的杀伤效果。
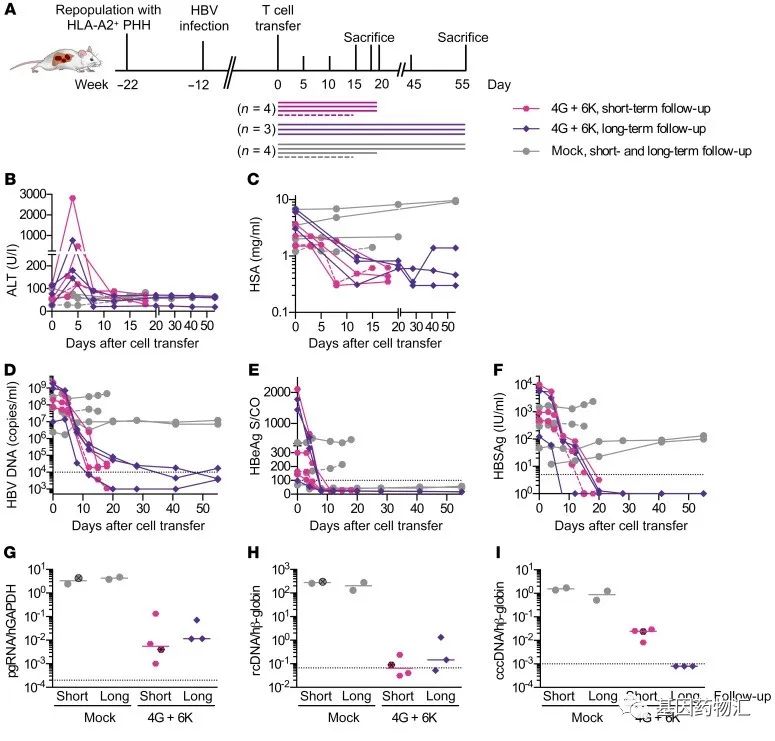
各类指标的观察以及长期随访的结构也同样证实了这一点,TCR-T细胞展现出了良好的抗病毒活性。
如果有这些肝癌患者希望申请这类临床试验项目,可以参考下方海报当中介绍的步骤,扫描二维码,下载「全球肿瘤医生」手机app(各大手机应用商店也已经上线),提交病历资料申请。
2、以人乳头瘤病毒(HPV)为靶标
HPV即人乳头瘤病毒,最常见的发病部位在皮肤及粘膜。这类病毒的分型多达130种以上,分为皮肤低危型、皮肤高危型、黏膜低危型、黏膜高危型,均能引起人体皮肤黏膜的鳞状上皮增殖,即导致肉眼可见的疣体。除此以外,高危型的HPV感染还可能发展为癌症。
皮肤高危型的HPV主要包括HPV5、8、14、17、20、36、38等,与外阴癌、阴茎癌、肛门癌、前列腺癌、膀胱癌相关;
黏膜高危型的HPV主要包括HPV16、18、30、31、33、35、53、39等,与宫颈癌、直肠癌、口腔癌、扁桃体癌等相关。
因此,HPV也成为了治疗这些癌症、尤其是其中部分诱发因素几乎全是HPV感染的癌症的治疗突破口。
癌症疫苗、TCR-T疗法等等,这些新兴的免疫治疗及细胞治疗手段,都有针对HPV的新项目,广泛覆盖宫颈癌、头颈癌以及肛门癌等HPV相关肿瘤的适应症。
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
早期膀胱癌术后五年生存率高达90%,这五
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

警惕!乳腺癌复发偏爱这3大人群!术后一定
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【实体瘤溶溜病毒免费招募】溶瘤病毒Ml(
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
从多处转移到完全缓解!新型CAR-T细胞
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
救命药加速入场!2025第二季度9款抗癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




