近一半患者肿瘤显著缩小,17名患者完全缓解!TIL疗法为癌症患者带来新曙光!
TILs疗法,TIL治疗肿瘤近一半患者肿瘤显著缩小,国内更多的TIL临床试验招募正在进行中
免疫疗法已经成为对抗癌症的一张“王牌”。除了大家熟知的PD-1,CAR-T等免疫疗法,近两年,另一款新型免疫疗法取得了前所未有的突破,有望上市!
在今年的欧洲肿瘤学会(ESMO )年会上,TIL疗法首个3期临床试验数据公布,震撼全场。研究人员说,这是第一项显示细胞疗法可改善实体癌患者预后的随机研究,为改善各种转移性实体瘤患者的治疗和潜在治愈带来了希望。
生存期翻倍,已有患者完全缓解!TIL疗法为癌症患者带来新曙光
众所周知,黑色素瘤患者的标准治疗方案之一是免疫检查点抑制剂依匹单抗,为了寻找更好的治疗方案,研究人员首次将新型免疫疗法TIL与标准治疗(依匹单抗 ipilimumab)进行对比,这项突破性结果非常振奋人心。
在这项代号为M14TIL 的3 期临床试验中,研究人员将 168 名不可切除的 IIIC-IV 期黑色素瘤患者随机分配接受依匹单抗免疫治疗(84名)或 TIL 细胞免疫治疗(84名),值得一提是,这其中89%的患者都是接受过PD-1治疗失败的难治型患者。

在2022年ESMO大会上首次报告的结果显示:
接受 TIL细胞治疗(50~200亿个TIL细胞回输)的患者的中位无进展生存期显着延长,为 7.2 个月,而接受 ipilimumab 治疗的患者为 3.1 个月;
与 ipilimumab相比,TIL 治疗的客观缓解率 (ORR)为48.8% & 21.4%,完全缓解率(CR)为20.2% & 7.1%,均增加了1倍以上。
值得一提的是,完全缓解率20.2%意味着17名患者接受治疗后,靶病灶完全消失!
并且,与 ipilimumab 治疗相比,随机接受肿瘤浸润淋巴细胞 (TIL) 治疗的患者疾病进展或死亡减少 50%!
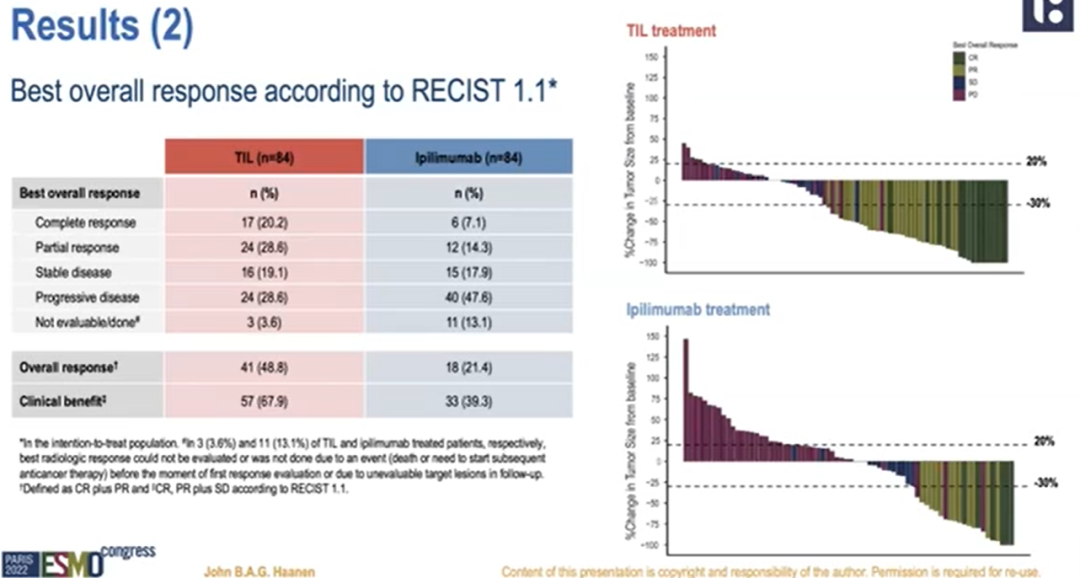
这意味着,与标准免疫治疗相比,这种全新的个体化细胞免疫治疗策略显着提高了晚期黑色素瘤患者的无进展生存期。
荷兰癌症研究所的 John Haanen 博士说:“这绝对是在改变实践,这项研究首次在一项随机对照试验中表明,细胞疗法对实体癌患者有效且有益。这项第 3 阶段研究的结果可能会导致监管批准,这将改变晚期癌症患者的治疗选择。”目前,荷兰研究人员现在正在努力让TIL 疗法获得欧盟的批准,并且没有商业参与,以确保这项疗法可以让更多患者负担得起,不受商业压力的影响。
TILs疗法究竟是如何清除肿瘤的
TIL,全称肿瘤浸润淋巴细胞(Tumor Infiltrating Lymphocytes),肿瘤组织中的一小部分免疫细胞,这些淋巴细胞中有部分是针对肿瘤特异性突变抗原的T细胞,是机体淋巴细胞侵入到肿瘤组织中,并对肿瘤起识别、抵抗和攻击作用的细胞群体,它们才是深入到敌军内部打击能力最强的免疫细胞,也是深藏在肿瘤中的宝藏!
需要大家注意的是,肿瘤中存在的TIL细胞数量直接影响患者的预后,通常,TIL细胞多的患者预后更好,因为TIL细胞在控制癌症进展及治疗中发挥重要的作用。这些细胞虽然珍贵,但却是每个肿瘤患者体内都存在的。那么为什么这些淋巴细胞不能完全清除癌症呢?
主要有以下两个原因:
癌症细胞“智能隐身”:它们使用各种机制逃避免疫系统监测。换句话说,就像它们戴上了面具,看起来和正常细胞一样,让免疫系统无法识别和杀伤它们。
免疫细胞不堪重负:癌症患者属于免疫低下的人群,体内的免疫细胞数量和活性严重不足,无法战胜数量巨大的癌细胞。
基于此,美国免疫界泰斗Rosenberg及其团队研发了TIL疗法:从肿瘤附近组织中分离出TIL细胞,加入生长因子IL-2进行体外大量扩增,达到数十亿至千亿级别,再回输到患者体内,从而扩大免疫应答,治疗原发或继发肿瘤的方法。
这种疗法将可以精准识别和杀伤癌细胞的T细胞免疫大军回输到体内,是根据每个癌症患者量身定制的个体化抗癌疗法,具有多克隆化,可特异性识别多种新生抗原,个体化,高度特异性,持久性,输注后可形成免疫记忆等特点。
可治疗肺癌、乳腺癌等多种癌症,TILs疗法有望上市
好消息是,TILs疗法是一款适用于多种实体瘤的免疫疗法,近年来,在国际上发表了众多成功案例及重磅研究数据,距离上市的脚步越来越近!
目前,除了上述荷兰癌症研究所的TIL疗法,美国的TIL疗法LN-145已在2022年8月启动上市申请的提交,一旦FDA批准,这将是首款用于实体瘤的细胞免疫疗法,将给癌症患者带来巨大的生存获益。关于这款疗法全球肿瘤医生网医学部已经写了大量的科普文章。同时TILs疗法在肺癌,乳腺癌,黑色素瘤,肉瘤等实体肿瘤中取得了卓越的临床数据。
值得国内病友们振奋的是,TIL疗法在国内已获得批准正式开展人体临床试验招募患者,想了解的病友可以致电全球肿瘤医生网医学部进行评估。
国内众多免疫疗法临床试验开花结果
实际上,很多晚期癌症患者可能没有可靶向的突变,因此,化疗和免疫疗法成为了主要治疗选择,这项新型免疫疗法的问世,将给癌症患者带来全新的希望。
此外,针对患者自身免疫系统的癌症免疫疗法被认为是“治愈”癌症的新希望。除了TILs疗法,越来越多的免疫疗法崭露头角,免疫细胞NK,DC,T细胞的临床辅助治疗正在进行大量的临床研究,有望联合化疗,靶向治疗、PD-1等标准疗法提高治疗效果,延长生存期。
比如:
1.树突细胞联合化疗在提高患者生存率方面显示出协同作用和显着潜力。总缓解率大幅提升!树突细胞疫苗联合化疗一线治疗晚期非小细胞肺癌初现曙光
2.NK细胞联合化疗,PD-1有望让胃癌患者获得更长的生存期。重磅!FDA授予全新NK细胞疗法联合化疗一线治疗晚期胃癌快速通道!
除此之外还有多靶点复合抗原T细胞目前作为免疫调节手段进行相关的临床研究。想了解最新进展的病友可联系全球肿瘤医生网医学部。
最后全球肿瘤医生网提醒广大癌症患者,虽然医学水平不断发展,治疗技术也在不断创新,但是至今为止,仍没有一种手段可以治愈肿瘤,肿瘤的治疗一定是依托于权威医院及权威专家的正规治疗,在采取常规治疗手段(手术、放疗、化疗)治疗后,根据自身的经济情况,辅助免疫治疗技术等综合疗法,达到巩固治疗,预防复发,提高生活治疗,延长生存期的目的。相信随着更多治疗方案的发展,肿瘤患者将迎来更多治疗选择和希望,我们期待人类攻克癌症的那一天早日到来。
参考文献:
https://www.esmo.org/newsroom/press-releases/cell-therapy-improves-progression-free-survival-in-advanced-melanoma-first-phase-3-study-shows
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
253例真实世界研究证实:益生菌联合IC
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
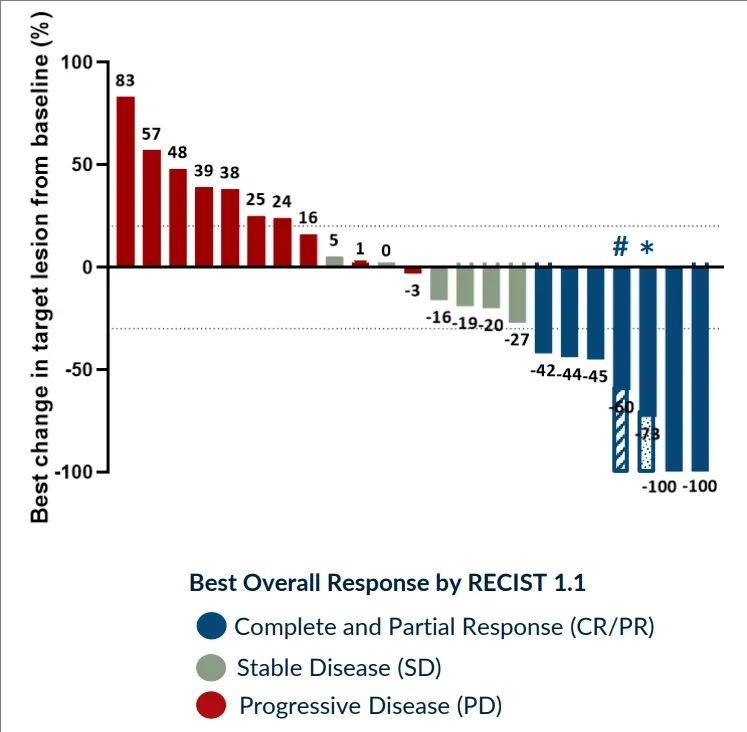
打一针激活抗癌免疫!肝癌治疗性疫苗大盘点
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
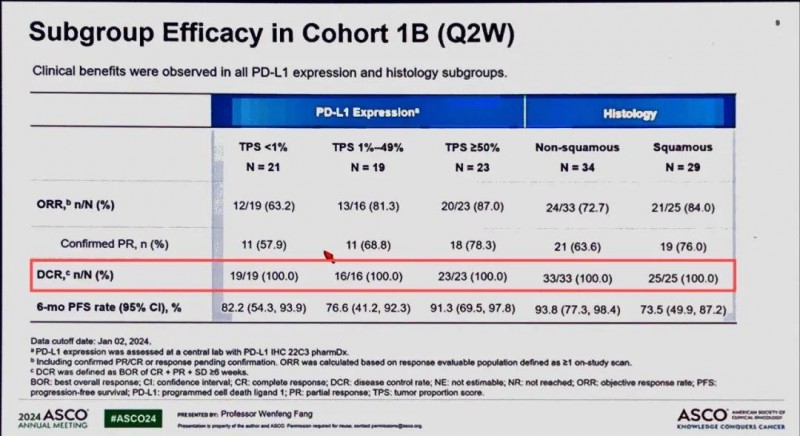
疾病控制率高达100%!2025奥希耐药
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【mRNA癌症疫苗免费招募】Vx-001
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

肝癌"黄金拍档"再发
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
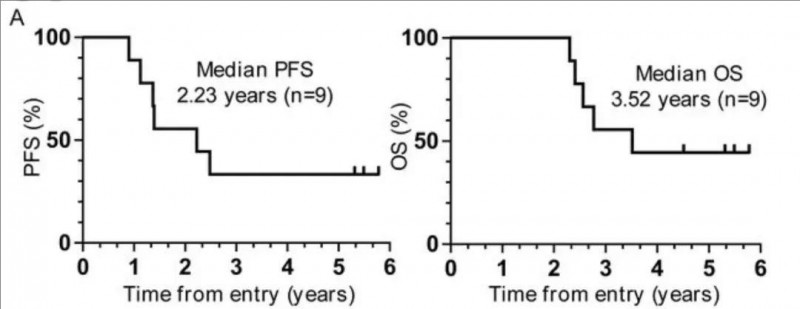
胰腺癌治疗性疫苗大盘点!最长OS超3年,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




