复星凯特第2款CAR-T产品拟纳入突破性治疗品种
复星凯特第二款CAR-T疗法FKC889(Tecartus、Brexucabtagene Autoleucel,KTE-X19)拟纳入突破性疗法品种
药明康德内容团队报道
3月24日,中国国家药监局药品审评中心(CDE)官网公示,复星凯特申请的FKC889拟纳入突破性治疗品种,拟开发用于复发/难治性套细胞淋巴瘤(MCL)。公开资料显示,FKC889是复星凯特从吉利德科学(Gilead Sciences)旗下Kite Pharma公司引进Tecartus在中国进行产业化、商业化的CAR-T细胞治疗药物,它也是继阿基仑赛之后,复星凯特在血液肿瘤领域的第2款CAR-T细胞治疗药物。
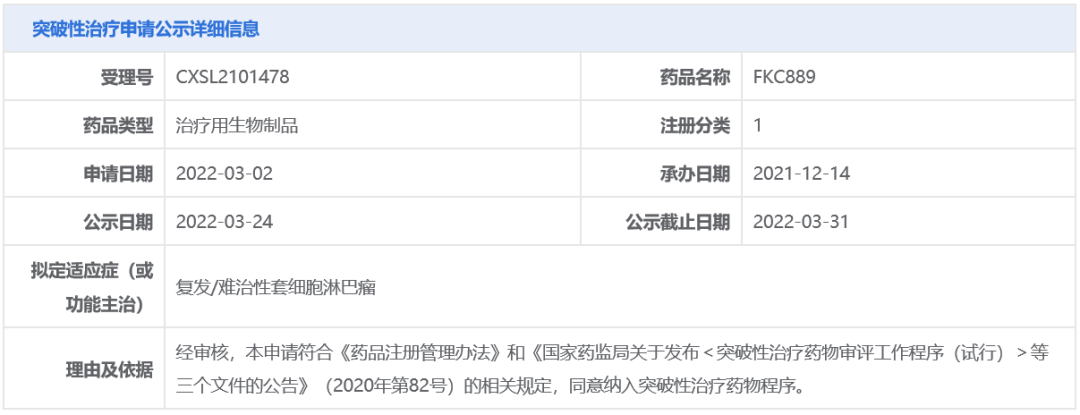
截图来源:CDE官网
Tecartus(brexucabtagene autoleucel,原名KTE-X19)是一款靶向CD19的自体CAR-T产品,它使用了包含T细胞筛选和淋巴细胞富集的XLP制造工艺。对于某些有循环淋巴母细胞迹象的B细胞恶性肿瘤来说,淋巴细胞富集是CAR-T产品制造的必要步骤。此前,Tecartus曾获得美国FDA授予的突破性疗法认定和欧洲EMA授予的优先药物资格(PRIME)等。2020年7月,Tecartus在美国获批用于治疗复发/难治性套细胞淋巴瘤成人患者。Kite公司曾在新闻稿指出,这是首款获批治疗这类患者的CAR-T产品。
在中国,Tecartus曾于今年3月初获批临床,拟用于既往接受过二线及以上治疗后复发或难治性套细胞淋巴瘤成人患者,此次即为该临床申请拟纳入突破性治疗品种。

对于套细胞淋巴瘤患者,此前Tecartus已在一项名为ZUMA-2的关键性临床试验中取得积极结果。数据显示,针对既往已接受过化疗、抗CD20抗体治疗和布鲁顿酪氨酸激酶抑制剂治疗的复发/难治性套细胞淋巴瘤成人患者,中位随访17.5个月时,客观缓解率(ORR)为92%,其中完全缓解率为67%。在所有疗效可评估的60名患者中,在数据截止时48%的患者仍处于持续缓解状态。在所有68名患者中,3级及以上细胞因子释放综合征(CRS)发生率为15%,3级及以上神经毒性的发生率为31%。
套细胞淋巴瘤由淋巴结套区的细胞癌变引起,是B细胞来源的具有侵袭性的非霍奇金淋巴瘤的一个罕见亚型,常见于60岁以上的男性。虽然目前有多种治疗这一癌症类型的疗法,但是患者最终都会对已有疗法产生耐药性。套细胞淋巴瘤在复发后具有高度侵袭性,患者迫切需要创新治疗选择。
值得一提的是,除了套细胞淋巴瘤,Tecartus还在临床试验中探索治疗急性淋巴细胞白血病(ALL)、慢性淋巴细胞白血病(CLL)等癌症的治疗效果。2021年10月,Kite公司宣布Tecartus获得FDA批准扩展适应症,用于治疗复发或难治性B细胞急性淋巴细胞白血病成人患者,这也是首个获批治疗成人ALL的CAR-T产品。
希望Tecartus在中国的临床研究也进展顺利,早日为更多癌症患者带来新的治疗选择。
参考资料:
[1]中国国家药监局药品审评中心(CDE)官网.Retrieved Mar 24,2022, From https://www.cde.org.cn/main/xxgk/listpage/9f9c74c73e0f8f56a8bfbc646055026d
[2]复星凯特第二款CAR-T细胞治疗药物FKC889获批临床. Retrieved Mar 2, 2022, from http://www.fosunkitebio.com/news/details-7083.html
[3] U.S. FDA Approves Kite’s Tecartus™, the First and Only CAR T Treatment for Relapsed or Refractory Mantle Cell Lymphoma. Retrieved July 24, 2020, from https://www.businesswire.com/news/home/20200724005428/en/U.S.-FDA-Approves-Kite%E2%80%99s-Tecartus%E2%84%A2-CAR-Treatment
[4] FDA approves brexucabtagene autoleucel for relapsed or refractory B-cell precursor acute lymphoblastic leukemia. Retrieved October 1, 2021, from https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-brexucabtagene-autoleucel-relapsed-or-refractory-b-cell-precursor-acute-lymphoblastic
内容来源: 医药观澜
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
253例真实世界研究证实:益生菌联合IC
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
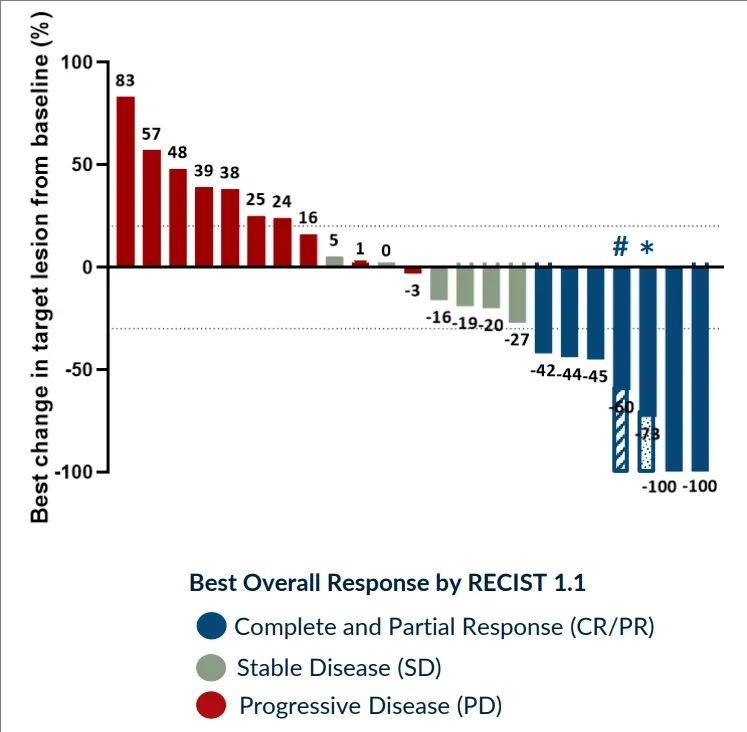
打一针激活抗癌免疫!肝癌治疗性疫苗大盘点
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
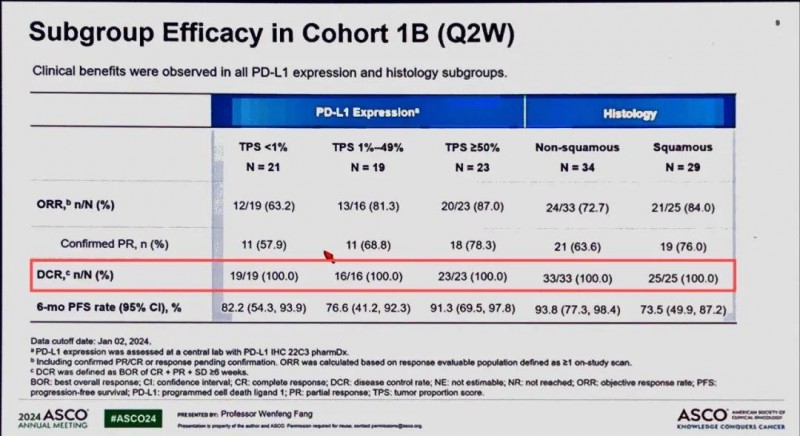
疾病控制率高达100%!2025奥希耐药
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【mRNA癌症疫苗免费招募】Vx-001
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

肝癌"黄金拍档"再发
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
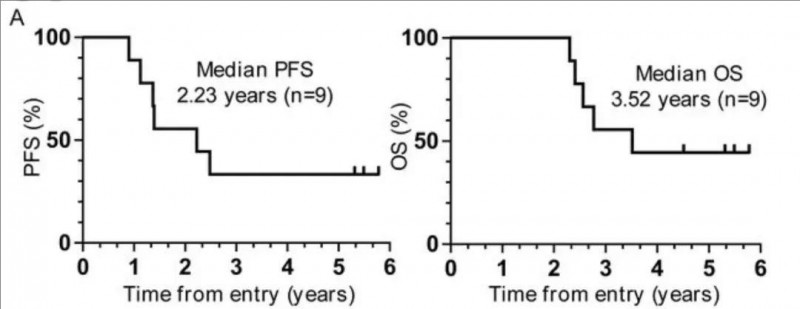
胰腺癌治疗性疫苗大盘点!最长OS超3年,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




