【临床试验招募】胃癌患者福音!国产版雷莫芦单抗免费用药机会来了!
招募标准
胃癌靶向药物国产版雷莫芦单抗(Me-Too产品)金妥昔单抗临床试验招募中
中国胃癌靶向药现状
早期胃癌患者5年生存率可达到90%~100%,但晚期胃癌患者5年生存率仅约30%,大量患者确诊时已经失去手术机会。加之放射治疗消化道肿瘤效果不理想,药物治疗成为了晚期胃癌患者最重要的治疗手段之一。除传统化疗外,靶向治疗的重要性已经受到越来越多的认可。
在胃癌的靶向治疗中,针对HER2靶点的药物曲妥珠单抗于1998年获批,且已经在国内上市、纳入医保。但根据我国真实数据分析,HER2阳性患者在胃癌中仅占8.3%~8.8%,仍有超过90%的患者无法接受曲妥珠单抗的治疗。
幸而抗血管生成类靶向药物面世,让这部分患者也能接受靶向药物的治疗。我国自主研发的抗血管生成类药物阿帕替尼在国内上市,为改善国内患者生存质量、延长生存期做出了巨大贡献。
但遗憾的是,目前已经获得FDA批准于国外上市、并已经取得了确切疗效的抗血管生成类药物雷莫芦单抗短期内并不能在国内上市。因此,尽管雷莫芦单抗已经被证实能够延长晚期胃癌患者的生存期,并在临床上得到了肿瘤专家的广泛认可与推荐,但每月约6万元的治疗费用以及国外药物极高的获取难度,仍使众多患者望而却步,丧失治疗良机。
为了解决这一难题,也为了改善胃癌患者的生存质量,我国药企针对雷莫芦单抗相同靶点人血管内皮生长因子受体2(VEGFR2/KDR)进行深入研究、攻坚克难,终于研制出了“国产版雷莫芦单抗”(Me-Too产品)金妥昔单抗,为胃癌患者生存助力!
迎战胃癌,金妥昔单抗整装待发
金妥昔单抗为雷莫芦单抗的Me-Too产品,属于抗人血管内皮生长因子受体2(VEGFR2/KDR)单克隆抗体,能够特异性的与人VEGFR2胞外结构域相结合。在体内通过阻止VEGFR2与其配体的结合,抑制该信号通路介导的血管内皮细胞增殖作用、抗凋亡作用、细胞迁移作用和血管通透性增加的作用,以达到抑制肿瘤的发展与转移的效果。
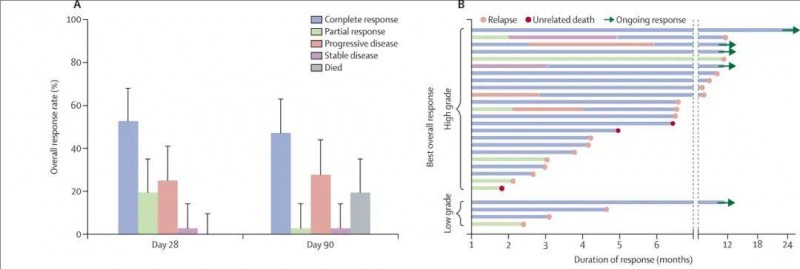
既往研究结果已经证实,雷莫芦单抗对于晚期胃癌患者的生存情况有显著的改善效果。在一项名为RAONBOW的全球性Ⅲ期实验中采用雷莫芦单抗+紫杉醇方案及安慰剂+紫杉醇方案治疗二线难治或初始治疗后病情仍进展的晚期胃癌或胃-食管结合部腺癌患者进行对比,结果雷莫芦单抗组患者中位总生存期为9.6个月、中位无进展生存期为4.4个月,安慰剂组患者为7.4个月、2.9个月;两组患者客观缓解率分别为28%和16%,雷莫芦单抗展现出了显著的优势。
与雷莫芦单抗相同,金妥昔单抗并不依赖某一特定突变类型发挥杀癌效果,因此可以对更多患者发挥治疗效果。通过阻止血管生成,金妥昔单抗能够阻断肿瘤病灶的血液供应,一方面掐断了病灶的养分供应,一方面降低了癌细胞通过血液向周围或远处组织浸润及转移的风险,从遏制生长与阻止转移两个方面作用,有效阻止肿瘤的进一步恶化。
相比起目前应用已经比较广泛的曲妥珠单抗,金妥昔单抗能够治疗更多无法从HER2靶向药物中获益的患者,为这部分患者带来希望。
目前,金妥昔单抗在国内的Ⅰb/Ⅱ期临床研究已经展开,计划招募76例晚期胃及胃食管结合部腺癌患者,挑战二线治疗方案!
金妥昔单抗Ⅰ期临床试验开启,胃癌患者免费用药机会来了
在此次试验中主要研究金妥昔单抗二线治疗晚期复发及转移性胃癌患者的药代动力学及耐受性,所有参与临床试验的患者均接受金妥昔单抗联合紫杉醇治疗,不设置空白对照组。全国多家大学附属医院同步进行,患者可以就近接受治疗。
除此以外,针对金妥昔单抗治疗其他多种实体瘤的临床试验正在筹备中,有望在未来开启,造福更多患者。
试验分期:Ⅰb/Ⅱ期
招募数量:共76例
纳入标准:
1、年龄18~75周岁,性别不限;
2、经组织学诊断的晚期或转移性胃或胃食管结合部腺癌患者,且既往接受过含铂类联合氟尿嘧啶类药物一线化疗期间或治疗结束后3个月内疾病进展(辅助或新辅助治疗期间或治疗结束后6个月内疾病进展的受试者可以入组);
3、 根据RECIST1.1实体瘤疗效评价标准至少有一个可测量病灶(即存在实体病灶);
4、ECOG体力状况评分0~1分;
5、骨髓储备、肝功能、肾功能、凝血功能基本正常;
6、有生育能力的受试者,在研究期间和末次给药后的3个月期内,同意采取有效避孕措施,且女性入组时血妊娠试验阴性
7、详细纳入标准及排除标准可咨询全球肿瘤医生网医学部。
申请流程:
1、按要求将病历资料提交至全球肿瘤医生网医学部;
2、医学部初步评估后匹配合适的临床试验;
3、向相应的试验中心提交病历资料;
4、评估通过后协助患者参加临床试验。
申请方式:
做过基因检测的病友,请将报告发送至全球肿瘤医生网医学部,我们的专家将为您全面分析检测报告,匹配能够入组的临床试验,以及有无新药可以使用。
1、请将基因检测报告,诊断报告电子版或拍照发送至doctor.huang@globecancer.com,邮件中留下联系方式,医学部收到报告分析完毕后一个工作日内电话联系;
2、直接致电全球肿瘤医生网医学部(400-666-7998)咨询相关医生。
↓扫描二维码申请入组↓

写给患者的话
的确,长期以来,EGFR 20号外显子插入突变型患者的治疗效果并不理想,与其他EGFR突变型患者相比存在不小的差距。但各位病友并不应该为此而感到绝望、更不能提早放弃。我们可以看到,随着医疗水平的发展,研究者已经将目光放到了这些“罕见突变”上,新药涌现,光明的前景正在徐徐展开。
如今,我国医疗水平逐渐跟上了世界的脚步,自主研发的新药频频问世,国内患者获得先进药物治疗的希望终于不再遥不可及。我们衷心地希望,JMT-101能够帮助更多国内患者战胜肿瘤、收获幸福生活。








![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




