近半数患者成功抗癌!揭秘肠道菌群的隐藏价值,击溃肝癌、胃癌等多癌种,ICI耐药亦有效
肠道菌群抗癌,揭秘肠道菌群的作用和隐藏价值,击溃肝癌、胃癌等多癌种,ICI耐药亦有效
肠道不仅是人体内最大的“排污厂”和“加油站”,还是人体重要但又极易被忽视的免疫器官,人体约70%的免疫细胞都集中在肠道。近年研究发现,肠道菌群在调节机体免疫力、抗肿瘤治疗中,发挥着至关重要的作用,已成为全球癌症领域的研究热点。
2024年7月25日,由韩国国家癌症中心、韩国政府等支持的一项研究证实,粪便微生物群移植帮助近半数胃肠道肿瘤患者,克服了对免疫疗法的抵抗力,显著增强了癌症免疫治疗的效果!该结果同步发表在国际知名杂志《细胞宿主与微生物》上。一时之间引起热烈讨论,这个隐藏在肠道中的“抗癌秘密武器”,终于开始在世界舞台上“大放异彩”!
韩国重大发现:晚期胃肠道肿瘤粪便微生物群移植后,疾病控制率近50%
▲截图源自“OneLive”
韩国本次进行的这项临床研究(NCT04264975),共入组13例对PD-1抑制剂耐药的晚期难治性胃肠道肿瘤患者,包括转移性胃癌(4例)、肝细胞癌(4例)、食管鳞状细胞癌(5例),中位年龄为60岁(范围:38~76岁),且既往均接受过大量全身治疗(中位数为10次,范围:4~34次)。所有患者在接受纳武单抗(nivolumab)单药治疗后,均出现确诊疾病进展,其中46.2%(6例)的患者出现原发性耐药,53.8%(7例)的患者出现继发性耐药。在确认疾病进展后立即入组,在继续接受nivolumab治疗的同时,还接受粪便微生物群移植(FMT)。
结果显示:接受粪便微生物群移植(FMT)的13例患者中,有6例(近一半)获得了持续的微生物群变化和临床益处。其中,1例患者获得部分缓解(PR),5例患者达到疾病稳定(SD),客观缓解率(ORR)为7.7%,疾病控制率(DCR)高达46.2%,这也意味着,近半数患者在FMT移植后,获得了临床疗效。这也凸显了FMT和持续免疫治疗的综合治疗效果(详见下图)。
图1 晚期实体瘤患者接受FMT联合纳武单抗治疗后的临床反应
▲图源“Cell Host Microbe”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
一例肝细胞癌患者,FMT移植后获得PR,肿瘤缩小47.7%
更令人惊讶的是,一位对纳武单抗具有原发性耐药性,且病情持续进展的转移性肝细胞癌(HCC)患者(R7),在接受粪便微生物群移植(FMT)+持续免疫治疗后,实现了部分缓解(PR),并且肿瘤病灶显著缩小。
1、肿瘤病灶缩小:该患者在第一次粪便微生物群移植(FMT)后,靶病灶仅增加了13%。在第二次粪便微生物群移植8周后,肿瘤显著缩小了30.5%。并最终实现了部分缓解(PR),且肿瘤大小较第一次FMT前,缩小了47.7%(详见下图)。
▲图源“Cell Host Microbe”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:在第二次FMT8周后,肿瘤缩小,并实现PR(下方红色星号)。
2、肿瘤标志物下降:在第二次粪便微生物群移植8周后,血清甲胎蛋白(AFP)、拮抗剂II诱导蛋白(PIVKA-II)等肿瘤标志物,也显著下降(详见下图)。
▲图源“Cell Host Microbe”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
综上,免疫检查点抑制剂(ICI)虽彻底改变了癌症治疗,但许多患者从未产生反应或在初始反应后产生耐药性。而上述研究结果显示,FMT联合免疫疗法可有效改变患者的肠道菌群,增强晚期实体瘤对ICI的反应,从而显著增强临床疗效。
隐藏在肠道中的"抗癌秘钥",肠道菌群身份大揭秘
肠道是人体最大的消化器官,也是与外界接触最大的器官之一,除了我们熟知的消化功能外;肠道因其独特结构,不断接触各种抗原和微生物,为保护机体免受病原体侵害,同时维持稳定的内环境,人体肠道还进化出了独特的区域免疫功能。
肠道微环境可通过益生菌或菌群移植重建,起到重新调整免疫稳态的作用。其中,肠道菌群指广泛分布、栖息于胃肠道内、参与维持肠道生理和免疫稳定性的多种微生物,在维持肠道稳态中起着重要作用,并且能够改变免疫系统的结构和功能,对宿主的整体健康不可或缺。
2015年《Nature(科学)》杂志中首次提出“肠道微生物群,在免疫疗法反应中的作用”,文中指出,肠道菌群可产生强大的免疫反应,在调节宿主的免疫调节、维持癌症免疫稳态、维持肿瘤微环境(TME)等方面,发挥着重要作用。目前主要可通过饮食干预、粪便菌群移植(FMT)、补充益生菌、补充益生元等方式,调节或改变肠道菌群,从而提高抗癌疗效。
1、粪便菌群移植(FMT):从健康个体捐献者的粪便中,分离出粪便菌群,以荚膜或菌液的形式,通过胶囊口服或内窥镜灌注等方式,移植到患者的肠道中,从而重建新的肠道菌群、恢复微生物的多样性,最终达到提高机体免疫力、增加抗癌效果等目的。
2、益生菌:被联合国粮食及农业组织定义为“注射足够量时,对宿主有益的活微生物”,能够调节肠道菌群、促进消化、增强宿主免疫应答、提高抗肿瘤治疗的有效性。
3、益生元:是一类不被宿主消化吸收,但却能选择性地促进结肠中目标菌种生长、改善宿主健康的有机物,主要包括多糖、低聚糖等,常见如人参多糖、膳食纤维等。
肠道菌群不是一成不变的
肠道微生物组在生命早期发育,从出生到2~3岁,会发生显著变化;并在成年期保持相对稳定;之后会随着年龄增长,而发生一定的变化,主要经历以下几个阶段:
婴幼儿阶段
婴幼儿在分娩阶段,接触到外界环境开始,获得初始的肠道菌群;之后会随着年龄的不断增加,而逐渐向高多样性和稳定性转变。
1、在出生几天后,婴幼儿肠道中的主导菌群以链球菌、肠杆菌等为主;在之后的几周内,双歧杆菌成为优势物种。
2、在停止母乳喂养、摄入固体食物后,婴幼儿肠道菌群会快速增加,优势菌株逐渐变为梭状芽孢杆菌等。
成人阶段(青年、中年)
相较于婴幼儿时期,成年阶段具有相对稳定的肠道菌群结构,且肠道菌群物种多样性、组成结构,会随年龄增长而出现一定的变化。其中,青年人的肠道优势菌群为双歧杆菌属、瘤胃球菌属;中年人则为拟杆菌。
老年阶段
老年人肠道菌群的丰度、多样性、组成与年轻人有所不同。大多数情况下,老年人粪便微生物群的微生物多样性降低;同时优势菌种发生变化,有益微生物减少、有害菌增加,肠道菌群失衡。具体表现为双歧杆菌减少,而颤螺菌属、普雷沃氏菌属增加。
肠道菌群的影响因素
肠道微生物群代表着一个高度动态的环境,肠道菌群在不同年龄人群中所表现出来的差异,可能与多种因素有关,比如环境因素、饮食因素(如饮食偏好、膳食习惯改变)、个体因素(如年龄、性别等)、睡眠习惯、长期用药、情绪压力、遗传等(详见下图)。
图2 肠道菌群的影响因素
▲图源“CNKI”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
这也是市面上在售的很多益生菌,并不适合大多癌症患者的原因。除了考虑上述因素外,癌症患者还需根据自身的癌种类型、治疗方案、免疫功能受损情况等,在营养师或有执照的医疗保健专业人员的指导下,尽可能选择针对患者自身病情的“私人订制”版益生菌,此类个体化益生菌根据患者自身病情,筛选出特定的菌种,相当于“对症下药”,在进入肠道后,可重整肠道环境,排除害菌,帮助肠道建立起优势菌种架构,有助于显著改善患者病情,以达到预期的效果。
如果您还想了解益生菌或定制益生菌而定更多信息,可联系医学部,咨询权威的营养专家。
粪便微生物群移植联合抗PD-L1,黑色素瘤2年未见复发
通过粪便微生物群移植,积极调节肠道菌群,除了对胃肠道肿瘤有改善作用外,还有助于改善转移性黑色素瘤的预后。此外,近年研究发现,通过补充个性化益生菌或粪便微生物群移植,还有助于缓解放化疗所致的副作用,如口腔黏膜炎、胃肠道反应等。《世界临床病例杂志》近期就报道了一个“FMT联合抗PD-L1免疫疗法,治疗转移性黑色素瘤”的惊艳案例。
本例幸运患者是一位57岁的男性,2019年10月确诊为转移性 BRAF V-600E突变黑色素瘤,开始使用纳武单抗(Nivolumab)治疗,并获得部分缓解(PR)。但2020年10月,病情出现进展,计算机断层扫描显示,右腋窝淋巴结肿大、右髂骨转移。后续接受伊匹木单抗、派姆单抗(Pembrolizumab)治疗后,但病情仍持续进展。2021年4月,患者仅通过结肠镜接受粪便微生物群移植(FMT),同时接受手术切除,并维持派姆单抗治疗。
结果显示,粪便微生物群移植(FMT)后,该患者右侧胸部皮下疾病缩小。截止数据统计时(2023年6月23日),患者仍处于缓解期,这也意味着,治疗2年未见黑色素瘤复发的迹象(详见下图)。
图3 FMT的时间序列和对应的PET图像
▲图源“WJCC”,版权归原作者所有,如无意中侵犯了知识产权,请联系我们删除
注:粪便微生物移植(FMT)后,疾病规模缩小,表明派姆单抗在FMT移植后,恢复了活性。
综上,本例难治性黑色素瘤患者,经粪便微生物群移植(FMT)+抗PD-L1联合治疗后,获得良好的临床和长期效果,且未见明显的副作用。
小编寄语
积极保持肠道健康、维持肠道菌群的平衡,有助于改善整体健康状况、提升机体的免疫力,同时增强传统抗癌药的疗效,降低放化疗、手术等传统治疗的副作用。
但鉴于癌症的复杂性和患者的个体差异,在使用微生物组进行个性化抗癌前,需要对患者的微生物组,进行个性化评估和分析,以便为癌症患者设计特征性微生物组介导的抗肿瘤方案,以提高治疗效果,并消除治疗副作用。
最后全球肿瘤医生网医学部温馨提示,如果癌症患者因各种原因,无法维持健康体重、正常的营养需求时,需接受专业的营养支持治疗,包括口服营养补充或肠外营养支持。如果您还想了解肠道菌群、粪菌移植、定制益生菌的更多讯息,可以咨询全医学部,获取专业营养师的帮助。
参考资料
[1]Kim Y,et al.Fecal microbiota transplantation improves anti-PD-1 inhibitor efficacy in unresectable or metastatic solid cancers refractory to anti-PD-1 inhibitor[J]. Cell Host & Microbe, 2024.
https://www.sciencedirect.com/science/article/pii/S1931312824002282?via%3Dihub
[2]Del Giglio A,et al.Fecal transplantation in patient with metastatic melanoma refractory to immunotherapy: A case report. World J Clin Cases. 2023 Aug 26;11(24):5830-5834.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10505991/
[3]柯善林.肠道菌群随宿主年龄的动态变化以及对宿主衰老和病原体感染的影响研究[D].江西农业大学,2021.
DOI:10.27177/d.cnki.gjxnu.2021.000002.
[4]https://www.onclive.com/view/fecal-microbiota-transplants-may-enhance-immunotherapy-efficacy-in-gi-cancers
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
早期膀胱癌术后五年生存率高达90%,这五
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

警惕!乳腺癌复发偏爱这3大人群!术后一定
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【实体瘤溶溜病毒免费招募】溶瘤病毒Ml(
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
从多处转移到完全缓解!新型CAR-T细胞
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
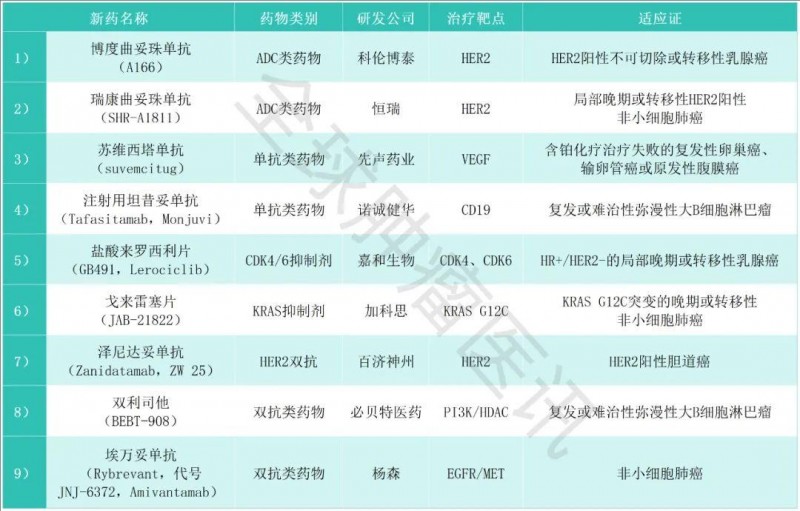
救命药加速入场!2025第二季度9款抗癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




