三款多发性骨髓瘤CAR-T产品获FDA批准,有望打破复发或难治魔咒
美国FDA批准三款CAR-T产品Carvykti、西达基奥仑赛、伊基奥仑赛用于多发性骨髓瘤,有望打破复发或难治的魔咒
来自法国的William Casler(威廉·卡斯勒)自2009年诊断出多发性骨髓瘤后,抗癌之路漫长又曲折,不仅先后进行过两次移植手术,参与过卡非佐米/达拉木单抗/地塞米松三联疗法的临床试验,之后还一直接受泊马度胺治疗,但其血常规相关指标(红细胞、白细胞、血小板计数)很难达到正常水平。
幸运的是,他后来在巴黎圣路易斯医院接受了CAR-T细胞治疗,经治疗后部分症状得到了缓解,轻链从近900下降到6,M峰值水平可测量值为4。随着后续的一系列治疗,威廉的病情得到了很大的改善。
何谓多发性骨髓瘤
多发性骨髓瘤(MM)是一种浆细胞恶性肿瘤,约占血液系统恶性肿瘤的10%,其特征是骨髓中恶性浆细胞的克隆性增殖,并伴有单克隆免疫球蛋白(即M蛋白)过量产生、终末器官损伤。
虽然随着单克隆抗体(如伊沙妥昔单抗、达雷妥尤单抗)、蛋白酶体抑制剂(硼替佐米、卡非佐米)、免疫调节药物(如沙利度胺、泊马度胺)等新型治疗药物的应用,多发性骨髓瘤患者的生存结局得到了较大改善,但几乎所有患者都不可避免地会因耐药而复发。因此,临床迫切需要探索新的治疗方法。
值得庆幸的是,近年来随着精准医学的发展,研究人员针对多发性骨髓瘤的特异性治疗靶点,研发出了新兴的CAR-T细胞疗法,并获得美国食品和药物管理局(FDA)批准,为多发性骨髓瘤患者带来了新的希望!
自带"GPS"的CAR-T细胞,精准定位多发性骨髓瘤靶点
CAR-T细胞(即嵌合抗原受体T细胞)疗法,是通过给CAR插入一段编码的DNA片段,对患者自身T细胞进行基因重新编程,以诱导抗肿瘤反应的一种细胞免疫疗法。
这里提到的“CAR”是特定抗原的重组受体,回输后一旦遇到肿瘤,即可快速产生特定的肿瘤靶向T细胞,仿佛自带“导航头”,可通过多种方式介导肿瘤杀伤,包括分泌含有穿孔素和颗粒酶的细胞毒性颗粒、产生促炎细胞因子、激活Fas/Fas配体途径等。
目前,CAR-T细胞治疗多发性骨髓瘤应用较多的靶点是B细胞成熟抗原(BCMA),为复发或难治性MM患者带来了新的希望。
目前国际干细胞研究医学部急招B细胞淋巴瘤、T细胞淋巴瘤、T细胞白血病(T-ALL)、急性淋巴细胞白血病、非霍奇金淋巴瘤、胃癌、肝癌、胰腺癌、结直肠癌、间皮瘤、卵巢癌等癌种!
想要评估病情是否能够接受CAR-T疗法可将病理报告、治疗经历及出院小结等提交至国际干细胞研究医学部,进行初步评估!
治疗多发性骨髓瘤的CAR-T"明星"产品
1、Abecma—全球首款抗BCMA CAR-T疗法,客观缓解率达72%
Abecma(Idecabtagene vicleucel)是全球首款靶向BCMA的CAR-T疗法,先后获得美国食品和药物管理局(FDA)、日本厚生劳动省批准,用于治疗复发或难治性多发性骨髓瘤(R/R MM)。
此次获批是基于一项名为“KarMMa”的关键Ⅱ期临床试验,该试验招募了127例成人复发或难治性多发性骨髓瘤患者,这些患者此前至少接受过三线抗骨髓瘤治疗(包括免疫调节药物、抗CD38单克隆抗体、蛋白酶体抑制剂)。
经Abecma治疗后,在100例可评估疗效的患者中,客观缓解率(ORR)达72%,其中完全缓解率达28%,中位缓解持续时间为10.7个月。
2、Carvykti——首款获FDA批准的国产CAR-T疗法,客观缓解率达85%
Carvykti(西达基奥仑赛,cilta-cel)是首款获得FDA批准的国产CAR-T疗法,由传奇生物自主研发,并于2022年5月、9月,分别在欧盟和日本上市,主要用于治疗难治或复发性多发性骨髓瘤(R/R MM)。
本次获批是基于CARTITUDE-1的结果,该研究选取97例既往至少接受过三线治疗的R/R MM成年患者。结果显示,几乎所有人(98%)都对治疗有反应,其中,78%的患者骨髓或血液中未出现癌症迹象,反应中位持续时间为22个月。
目前Carvykti相关试验已进展到CARTITUDE-4,传奇生物在2023年ASCO会议上公布了最新研究数据。该研究纳入了既往接受过一至三线治疗的419例患者,并随机分配为西达基奥仑赛组(cilta-cel,n=208)、标准治疗方案组(SOC,n=211)。
经过16个月的中位随访,cilta-cel组患者的死亡风险或疾病进展降低了74%,客观缓解率(ORR)为85%,完全缓解率(CR)为73%,;而SOC组患者的ORR为67%,CR为22%。该结果再次验证了cilta-cel在复发或难治性骨髓瘤治疗中的亮眼成绩!
3、福可苏——我国首个获批的多发性骨髓瘤的细胞治疗产品,客观缓解率达96%
福可苏(伊基奥仑赛注射液)是全球首款全人源靶向的BCMA CAR-T产品,由我国自主研发且全流程自主生产;同时也是国内首款获批用于治疗多发性骨髓瘤的细胞产品,在中国抗癌史上留下了浓墨重彩的一笔!
它由驯鹿生物及信达生物联合研发,并获中国药监局(NMPA)批准上市,以B细胞成熟抗原(BCMA)为靶点,用于治疗复发或难治性多发性骨髓瘤(R/R MM)患者,这些患者既往大多接受过3种或以上治疗,且至少使用过一种蛋白酶体抑制剂及免疫调节剂。
此次获批是基于FUMANBA-1中国多中心I/II期临床研究数据,该研究选取103例复发/难治多发性骨髓瘤患者,结果于2023年ASCO年会上更新。
经过13.8个月的中位随访,在可评估疗效的101例患者中,客观缓解率(ORR)达96%,严格意义的完全缓解/完全缓解率(sCR/CR)为74.3%(75/101),95%的受试者达到微小残留病灶(MRD)阴性。
其中,在12例既往接受过CAR-T治疗的患者中,9例获得缓解,5例获得严格意义的完全缓解(sCR)。在89例既往未接受过CAR-T治疗的患者中,ORR达到98.9%,严格意义的完全缓解/完全缓解率(sCR/CR)达到了78.7%。
小编有话说
多发性骨髓瘤约占血液系统恶性肿瘤的10%,其耐药性和高复发率一直是影响预后的主要因素。近年来,随着新型药物、靶向治疗、免疫细胞疗法的不断发展,尤其是抗BCMA CAR-T细胞疗法的出现,为复发或难治性多发性骨髓瘤患者带来了新的曙光。2021年我国迎来了细胞免疫治疗的元年,目前全球共有三款治疗多发性骨髓瘤的CAR-T产品,其中两款由我国研发,这也标志着我国走在了世界前列。
小编也希望随着CAR-T技术的不断发展,未来可以造福更多的患者,给他们带来更长的生存期,更高的生活品质!
参考资料
[1]Zhang X,et al.CAR-T cell therapy in multiple myeloma: Current limitations and potential strategies. Front Immunol. 2023 Feb 20;14:1101495. doi: 10.3389/fimmu.2023.1101495.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9986336/
[2]Rendo MJ,et al.CAR T-Cell Therapy for Patients with Multiple Myeloma: Current Evidence and Challenges. Blood Lymphat Cancer. 2022 Aug 29;12:119-136. doi: 10.2147/BLCTT.S327016.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9439649/
[3]https://www.cancer.gov/news-events/cancer-currents-blog/2022/fda-carvykti-multiple-myeloma
[4]https://healthtree.org/myeloma/community/articles/myeloma-story-car-t-therapy
[5https://www.clinicaltrialsarena.com/projects/abecma-idecabtagene-vicleucel-multiple-myeloma/?cf-view
[6]https://www.globenewswire.com/en/news-release/2023/06/05/2682187/0/en/CARVYKTI-ciltacabtagene-autoleucel-cilta-cel-Reduces-Risk-of-Disease-Progression-or-Death-by-74-Percent-in-Earlier-Line-Multiple-Myeloma-Treatment-in-the-Landmark-Phase-3-CARTITUDE.html
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
早期膀胱癌术后五年生存率高达90%,这五
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

警惕!乳腺癌复发偏爱这3大人群!术后一定
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【实体瘤溶溜病毒免费招募】溶瘤病毒Ml(
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
从多处转移到完全缓解!新型CAR-T细胞
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
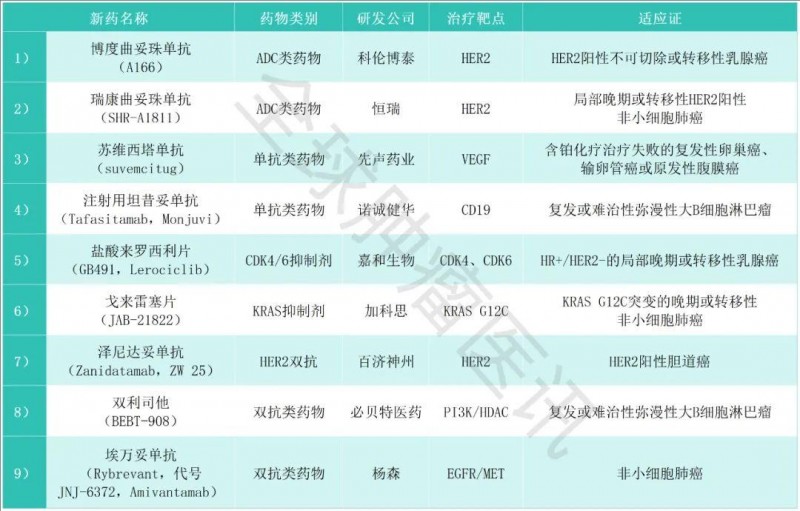
救命药加速入场!2025第二季度9款抗癌
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

抗癌月报(3月)|上市新药,CAR-T,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05







![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




