非小细胞肺癌奥希替尼耐药?这6种方案也许能保命!第2种方案有机会尝试的患者最多
奥希替尼为什么会耐药、原因有哪些,奥希替尼耐药后还有药吗,奥希替尼耐药后用什么药,奥希替尼(AZD9291)耐药后怎么办
正在用靶向治疗药物的癌症患者最怕的事情是什么?不良反应,还是说,耐药?
“耐药”这件事就像是悬在所有患者头顶的一柄达摩克利斯之剑,是一柄高悬头顶的危险利刃,不知何时会落下。如果一直不耐药,患者得到的疗效就可以长期地维持下去,甚至生活如常人;而一旦耐药,病灶就会再次开始迅速地生长,癌症卷土重来。
一位55岁的女性肺腺癌患者,最初确诊时是EGFR外显子19缺失(ex19del),用了一段时间的克唑替尼,后发展为EGFR T790M耐药突变;随后使用了第三代EGFR抑制剂奥希替尼,但又在一年后耐药,转变成了KRAS外显子2(G12D)和外显子3(Q61H)突变。
当时是2019年初,不论是对于奥希替尼耐药,还是KRAS突变,临床上都没有非常好的治疗手段。患者接受了两个周期的白蛋白紫杉醇+卡铂化疗,共6周,病灶没有任何缩小。最终,因为身体状况不佳,患者放弃了包括免疫检查点抑制剂在内的进一步抗肿瘤治疗。
时间一转到了3年后,现在,面对同样情况的患者们,又有哪些新的治疗选择呢?
常见的奥希替尼耐药原因有哪些
想找到一种效果比较好的方案来应对包括奥希替尼在内的第三代EGFR抑制剂耐药,那么首先就需要搞清楚患者为何会对奥希替尼耐药。简单来说,患者对于奥希替尼耐药的原因可以分为两类:一类是依赖EGFR的机制,一类是不依赖EGFR的机制。
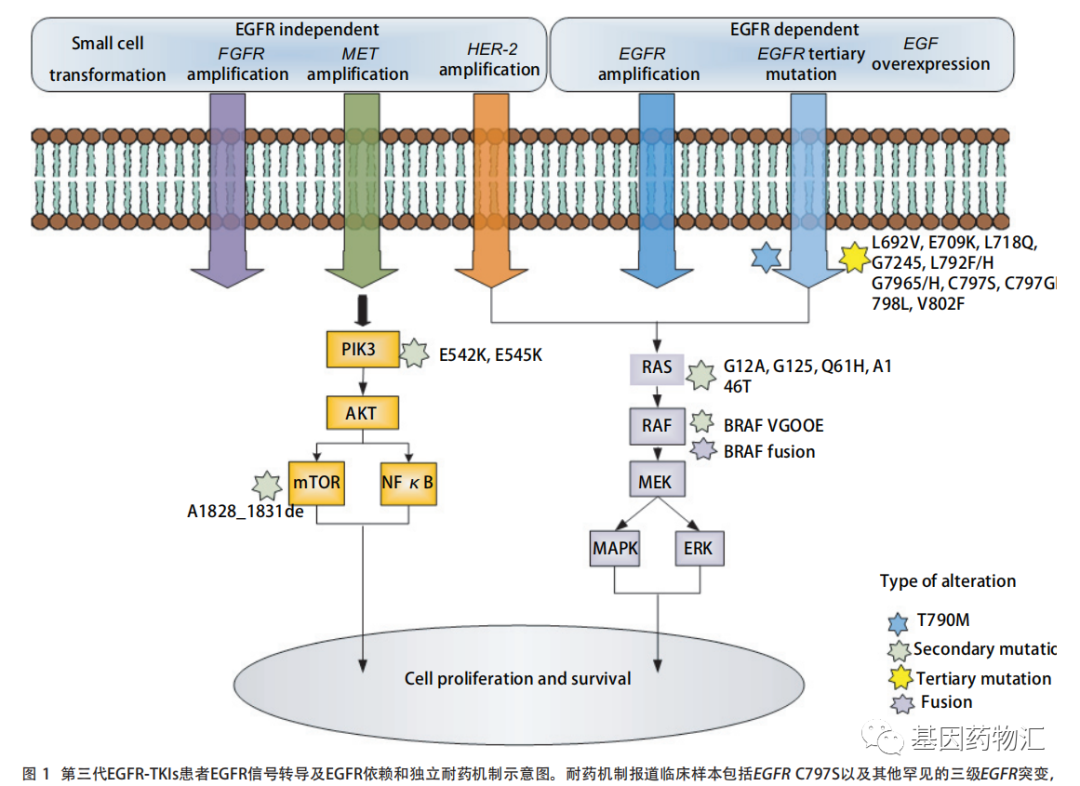
图片来源:《奥希替尼在非小细胞肺癌靶向治疗中的获得性耐药机制》DOI: 10.3779/j.issn.1009-3419.2020.103.0
除了病理类型转为小细胞肺癌以外,奥希替尼耐药患者常见的病理类型还包括EGFR Del19/T790M/C797S及L858R/T790M/C797S三突变(约占20%~40%左右)、MET(约占25%)、EGFR ex20ins、HER2/3、FGFR、RAS、mTOR等等。
EGFR C797S:最常见的耐药突变
大部分接受第三代EGFR抑制剂治疗的患者,耐药时间在1年左右,而如今距离奥希替尼的普及已经有3~5年的时间,患者对能够用于治疗第三代药物耐药的第四代EGFR抑制剂的需求,正在日益扩大。
EGFR Cys797Ser(C797S)突变是最常见的第三代EGFR抑制剂耐药突变,也就是T790M突变的患者,对于EGFR抑制剂再次耐药的时候最常见的突变类型。这种突变主要分为EGFR Del19/T790M/C797S和L858R/T790M/C797S三突变两类。
1、第四代EGFR抑制剂,"国研"走上世界前列
目前,首款走入临床试验阶段的第四代EGFR抑制剂是由我国药企研发的新药TQB3804。这款药物不以EGFR Del19等突变类型为主要靶标,而是专门针对第三代EGFR抑制剂耐药后常见的C797S突变,因此对于第三代药物耐药后患者的治疗效果更加出色。
目前,TQB3804在临床前试验中已经展现出了良好的效果,进一步的人体试验项目正在进行,我们会密切关注试验结果。
除此以外,由外国药企研发的BLU-945在临床前研究中也展现出了出色的潜力,目前正在进行进一步的临床试验。
2、顺式?反式?部分患者可从前代药物治疗中获益
因EGFR抑制剂耐药而导致的T790M/C797S突变还分为顺式突变和反式突变,对于耐药后治疗有着重要的影响。
我们都知道,人体DNA是双链结构,当T790M和C797S突变出现在同一条DNA链上时被称为T790M/C797S顺式突变,当这两个突变出现在不同的DNA链上时被称为T790M/C797S反式突变。临床上顺式突变比较多见,约占85%。
但从治疗的角度来说,这部分比较少见的反式突变患者可能是比较“幸运”的——这部分患者对于第一代+第三代EGFR抑制剂的联合方案比较敏感。
许多临床应用案例都证实了这种方案的效果,在ASCO大会上也曾经公开了一项小规模的试验结果。使用第一代EGFR抑制剂吉非替尼+第三代EGFR抑制剂奥希替尼联合治疗,患者的中位无进展生存期约为22.5个月,整体缓解率高达88.9%;病情持续进展的患者,耐药的原因均为旁路扩增等,均未检测出C797S、T790M突变。但这种方案的缺点在于,患者的治疗中经历的不良反应比较明显,耐受性稍差。
相信有不少患者已经从这种治疗模式中获益,我们非常希望研究者可以进一步优化治疗方案,明确适应症范围,并减少或降低不良反应,使更多患者从中获益。
MET:分多种亚型,部分亚型已有药物上市
从第一代到第三代EGFR抑制剂,MET都是一个让医生与患者非常头疼的耐药突变类型。且与MET相关的亚型非常多,包括MET扩增、c-MET过表达、MET外显子14跳跃突变等等,即使使用相同的药物,这些亚型的疗效也不一样,整体并不理想。
直到近两年MET抑制剂以及EGFR/MET“双抗”问世之后,这些患者终于迎来了新的希望。
1、MET抑制剂:多款新药问世,耐药、脑转移患者均可获益
近两年获批上市的MET抑制剂不少,包括率先经日本厚生劳动省批准的特普替尼、经美国FDA批准的卡马替尼、以及经中国MNPA批准的沃利替尼等等。这些已经上市的药物与临近上市的新药,在MET突变患者的治疗中均展现出了远超既往方案的效果。
其中瑞普替尼治疗的整体缓解率达到42.4%,卡马替尼治疗的整体缓解率达到了67.9%,两款药物的疾病控制率均超过了90%,且缓解持续时间分别达到了12.39个月和9.72~11.14个月。
而特普替尼在发生了脑转移的患者的治疗中也展现出了良好的潜力,患者的全身客观缓解率为52.4%,疾病控制率76.2%;中位缓解持续时间9.5个月,中位无进展生存期9.5个月。
使用沃利替尼治疗MET外显子14跳跃突变患者,整体缓解率为49.2%,疾病控制率达到了93.4%,中位缓解持续时间9.6个月。
亚组分析结果显示,初治患者整体缓解率54.2%,疾病控制率达到了95.8%,中位缓解持续6.8个月;在经治患者中,沃利替尼治疗的整体缓解率也达到了46.0%,疾病控制率同样高达91.9%。曾经接受过化疗、免疫治疗或靶向治疗等多线治疗的患者,中位无进展生存期达到了13.8个月。
2、EGFR/MET双抗:"双管齐下"、突破耐药困境
既然MET突变是EGFR耐药最重要的原因之一,那么使用双靶点抑制剂、即“双抗”药物,是否能够将治疗的效果再次提升一个台阶?
这样的治疗思路也受到了重视。在这项试验当中,研究者分析了使用EGFR/MET双抗Amivantamab-vmjw(Rybrevant,JNJ-6372)以及第三代EGFR抑制剂拉泽替尼(Lazertinib)联合方案,共同治疗奥希替尼及铂类化疗后疾病进展的非小细胞肺癌患者(不局限于MET异常)的疗效,已经取得了不错的前期数据!
数据公布时,中位随访时间为4.6个月,在80例可以评估的患者当中,整体控制率高达41%!患者的临床获益率,即包括11周以上缓解期的完全缓解、部分缓解及疾病稳定患者,共69%。
即使是已经接受过大量预处理的患者,即已经在前线使用过铂类化疗、奥希替尼以及其它多种治疗方案的患者,接受联合方案治疗的缓解率仍有21%,临床获益率51%。
JNJ-6372是一款近期备受关注的EGFR/MET双抗,已经经FDA批准了治疗EGFR ex20ins突变非小细胞肺癌的适应症。而这款药物独特的靶点组合,赋予它的潜力远超过了一个“难治突变”。
目前,JNJ-6372与拉泽替尼联合治疗奥希替尼耐药患者的中国中心临床试验,正在招募中国患者。这样的前沿方案试验机会非常难得,入组筛选也会更加严格。希望尝试申请这一试验的患者,可以联系基因药物汇-临床新药招募中心,提交病例并申请进行入组评估。
3、奥希替尼+沃利替尼:奥希替尼耐药后MET异常的"解决方案"
早先我们提过ORCHARD试验很多次,认为这是一项真正将靶向治疗的“个性化”发挥到了极致的临床试验。
这项研究主要针对第三代EGFR抑制剂奥希替尼耐药的患者。研究中,所有受试的奥希替尼耐药患者都会再次接受基因检测,并根据检测结果施予治疗。
比方说,若患者的耐药表现为MET扩增,那么他们会接受奥希替尼+沃利替尼(Savolitinib,Volitinib,一款国产MET抑制剂)的方案治疗。根据目前已经公开的数据,这种方案的效果相当不错。
20例受试患者当中17例病灶可评估,这部分患者的整体缓解率为41%,疾病控制率为82%;此外3级或以上不良事件发生率为30%,3例患者(15%)因不良事件而停止联合方案治疗,但没有因不良事件而死亡的病例。
HER3:ADC"家族"又出"救命药",疾病控制率超高
HER2/3突变同样是奥希替尼耐药最主要的原因之一。来自日本的U3-1402是一款HER3抗体偶联药物,在往届ESMO大会上,研究者曾经公开了这款药物治疗EGFR抑制剂耐药患者的疗效数据,疾病控制率达到了惊人的70%!
研究中,86%的患者曾经接受过奥希替尼治疗,90%的患者使用过化疗;患者的中位治疗线数的4线,其中包括2线EGFR抑制剂治疗。
当然,U3-1402最具突破性的意义在于,根据ASCO大会和WCLC大会上公开的结果,不论是何种类型的耐药突变,都可以从这款药物的治疗中获益。这意味着,一旦这款药物成功获批上市,EGFR抑制剂耐药的患者,等来的很可能是一款具有“通用价值”的重磅新药。
EGFR ex20ins
除了MET、RET等异常以外,真正让医生和患者头疼的还有另一种EGFR突变的亚型——外显子20插入突变(ex20ins)。这类患者被认为根本不可能从包括奥希替尼在内的EGFR抑制剂治疗当中获益,缓解率在0~28%,一二代药物治疗的中位无进展生存期在3个月以内。
在一项筛选了62464例晚期非小细胞肺癌患者的统计研究中,ex20ins患者的中位无进展生存期仅有2.86个月,中位总生存期仅有7.45个月,与其它EGFR突变亚型的10.45个月和25.49个月相比,甚至不到三分之一。
当然,在“特效药”诞生之前,医生们也考虑过另一种方案。如果常规的方案效果不佳,那么将药物剂量改为大剂量,效果会如何呢?
一项来自荷兰的试验,使用大剂量的奥希替尼(160 mg)治疗EGFR ex20ins阳性、T790M阴性的晚期非小细胞肺癌患者,受试患者共24例。结果整体缓解率为27%,包含了1例临床完全缓解的患者;中位无进展生存期为5.5个月,中位缓解持续时间为8.2个月,中位总生存期15.8个月。治疗中21%的患者需要减少治疗剂量。
虽然加大了剂量,但是27%的缓解率还是和其它报告差不多,不良事件的发生率也差不多,算不上理想。对于ex20ins患者来说,目前更好的选择,就是两款已经在国外获批上市的药物以外,以及参加这一靶点药物的临床试验。
1、EGFR-MET双抗:缓解率与生存期,优势均显著
随着研究重心的倾斜,目前临床上已经有了越来越多的EGFR ex20ins抑制剂临床试验,患者的治疗前景非常光明。
Mobocertinib(TAK-788)治疗的整体缓解率为35%,中位治疗时间13.9个月,中位无进展生存期7.3个月。
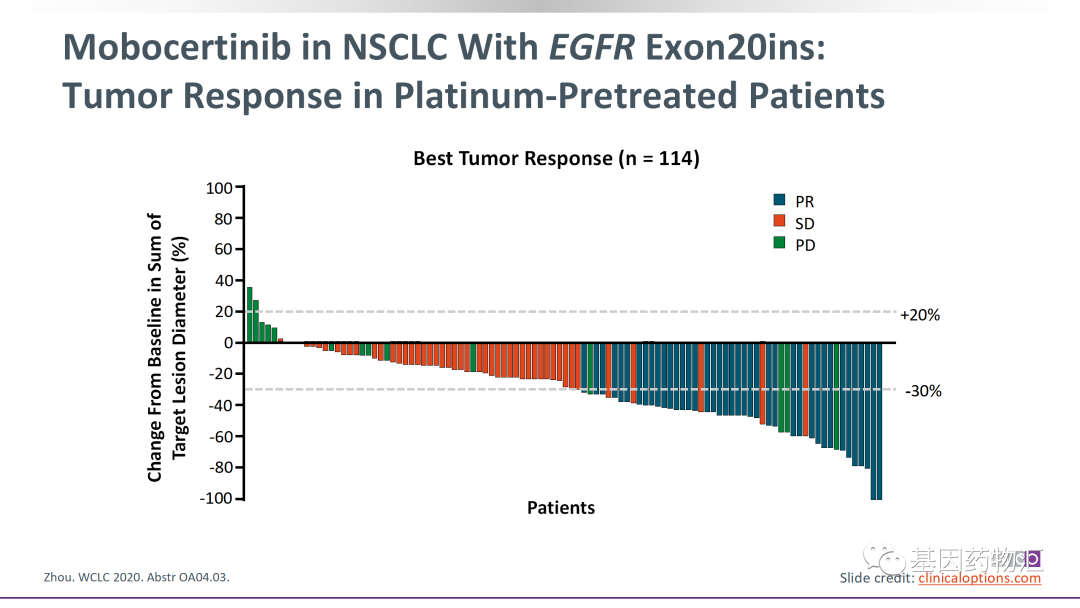
Amivantamab(JNJ-6372)治疗的整体缓解率为40%,中位治疗时间11.1个月,中位无进展生存期8.3个月,中位总生存期22.8个月。
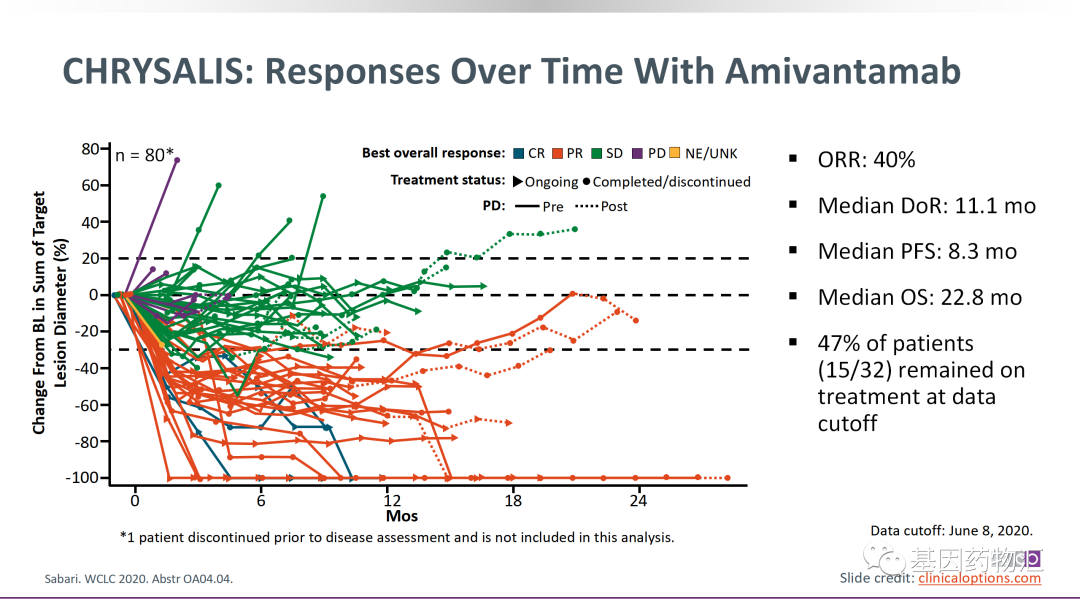
Poziotinib治疗的整体缓解率为27.8%,中位缓解持续时间6.5个月。
目前,针对EGFR ex20ins患者的临床试验非常多,有需求的患者,以及希望参与临床试验、尝试新药治疗的患者,可以联系基因药物汇-临床新药招募中心了解详情。
从癌细胞表面抗原突破:耐昔妥珠单抗"无视"耐药
耐昔妥珠单抗(Necitumumab)这个名字,相信不少患者都觉得有些耳熟。的确,尽管这款药物已经获批了肺鳞癌的适应症,但对患者疗效的改善并不明显,表现一直不温不火,与各类“突破性”的消息无缘。
但在2019年ASCO大会上,耐昔妥珠单抗一跃成为了“黑马”,再次被发掘出了从未有过的全新潜力。耐昔妥珠单抗+奥希替尼的联合用药组合,治疗各类EGFR抑制剂耐药的患者均获得了非常出色的缓解率。
其中,联合方案治疗第一二代EGFR抑制剂耐药的患者,整体缓解率29%;治疗第三代EGFR抑制剂耐药的患者,整体缓解率13%;其中,治疗T790M/C797S双突变的患者,整体缓解率竟达到了50%!
耐昔妥珠单抗这款药物很有特点。作为一款大分子药物,它的作用位点是癌细胞表面的EGFR受体,而非小分子药物所靶向的细胞内的酪氨酸激酶。在越来越多小分子药物以压倒性的优势取代大分子药物的如今,这款药物竟然又一次以“黑马”的身份亮相,让人不得不感叹,也许很多时候并不是药物的效果不好,而是没有找到这款药物最好的适应症,导致药物的“实力”发挥不太充分。
耐药患者是否有机会尝试免疫治疗?需要关注这些
除了上面各类突变以外,对以奥希替尼为代表的第三代EGFR抑制剂耐药的患者,还可能出现一种情况——经检测患者已经不存在EGFR突变,且PD-L1表达为阳性,或者一些特殊的、可能代表PD-1/PD-L1抑制剂治疗效果更好的突变阳性。这种情况下,患者可以使用免疫检查点抑制剂治疗吗?
我们都知道,EGFR突变是PD-1抑制剂的一种低效基因突变,也就是说,存在EGFR突变的患者,基本上很难从PD-1/PD-L1治疗当中获益。但如果患者已经明确地不再存在EGFR突变,并且还有一些能够从免疫治疗当中获益的指征,那么免疫检查点抑制剂也不失为一种治疗选择。
在另一个案例当中,患者同样是肺腺癌,从最初EGFR ex19del突变使用吉非替尼,到耐药后出现EGFR T790M突变是使用奥希替尼,最终因KRAS外显子3(R68S)突变阳性而耐药。患者后续的治疗选择了白蛋白紫杉醇+纳武单抗(纳武利尤单抗),4个周期的治疗后,达到了临床部分缓解!
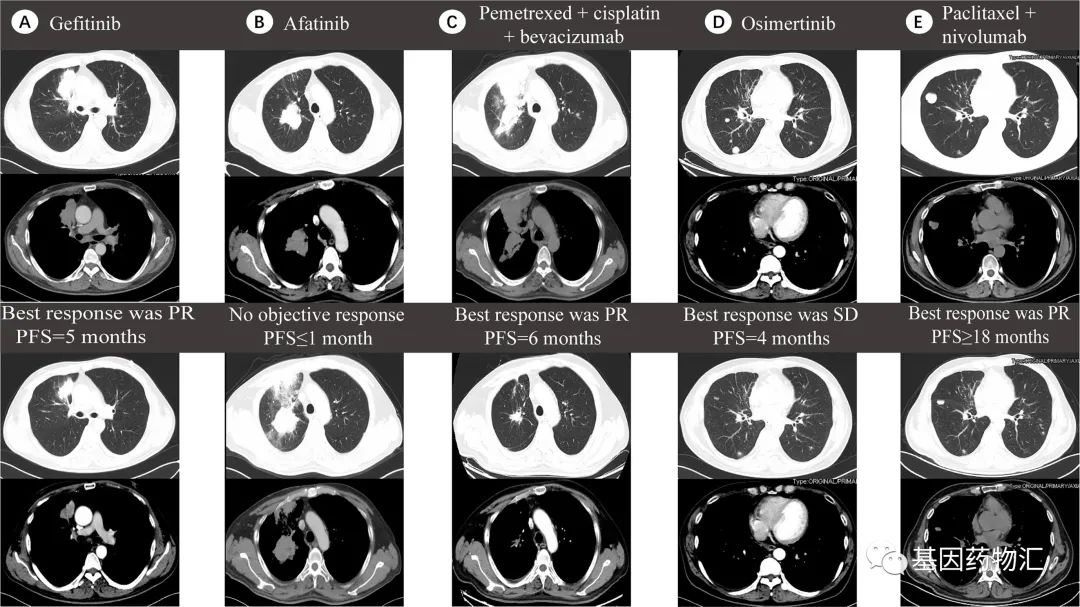
这说明,在部分非常特殊的情况下,免疫检查点抑制剂也能够成为这部分患者的选择。
"后奥希替尼时代",新药将至、检测先行
除了上述几种相对比较常见的耐药突变类型以外,还有少部分患者因RET融合等突变而发生了耐药,尽管不像上述耐药类型的患者那样,已经有疗效比较明确的新药或新方案,但也有一些临床试验项目,正在针对这一耐药突变类型的治疗进行研究,例如奥希替尼联合塞尔帕替尼(Selpercatinib,即LOXO-292)方案等。
读完这篇总结,相信大家已经看到了“后奥希替尼时代”多样而个性化的治疗选择。但想要从中挑选出适合自己的一种,首先应当明确自己的耐药突变类型。
随着癌症精准治疗的发展,基因检测已经成为了每一名癌症患者确诊后必须进行的检测项目。不论是初治的患者,还是经过一系列治疗后发生了耐药的患者,都应当在基因检测的指导下选择最有可能获益的方案,才能真正有效地延长生存期。
奥希替尼耐药,患者的靶向治疗“目录”就翻到了结尾?当然不是这样。无数的研究者、医生都在不断地书写,扩充着这份能够为患者“续命”的“目录”,开启一个接续于“奥希替尼时代”之后的“后奥希替尼时代”。
我们衷心希望这些新药临床试验能够取得圆满的成功,将更多有价值的选择,送到癌症患者们的面前。
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
肠癌患者找到"重生密码&quo
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

绝境逆袭!NY-ESO-1 TCR-T疗
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
结直肠癌六大治疗性疫苗重磅集结!最长控瘤
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
253例真实世界研究证实:益生菌联合IC
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
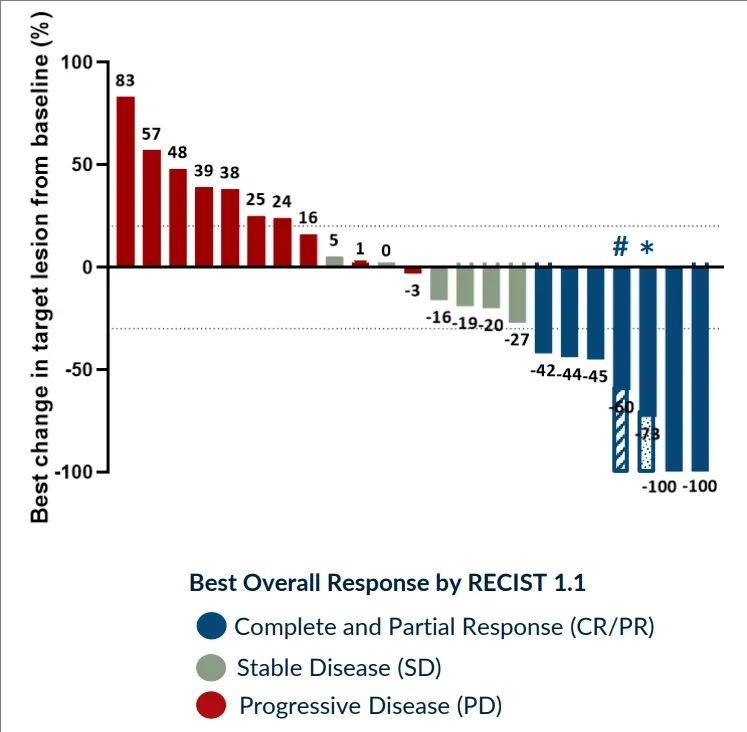
打一针激活抗癌免疫!肝癌治疗性疫苗大盘点
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
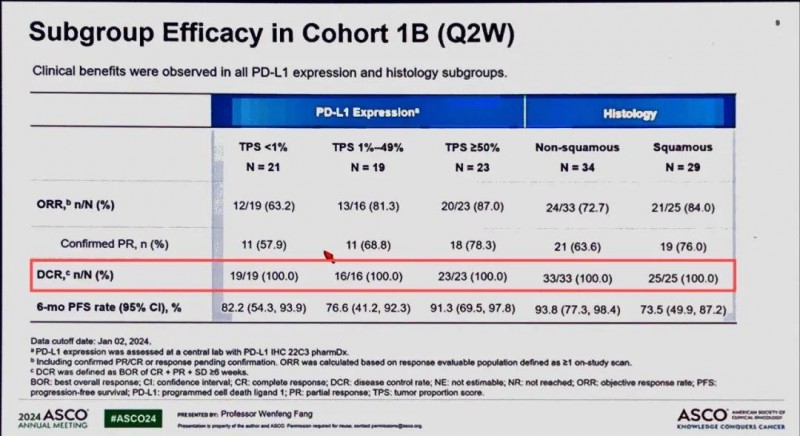
疾病控制率高达100%!2025奥希耐药
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05








![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




