8月FDA大事记:国产药开始发力了!越来越多的国研新药走上世界舞台
FDA大事记:2021年8月越来越多的国产抗癌新药走上世界舞台
8月,FDA迎来了一波新的“爆发”,几款重磅新药获得批准,还有许多非常有潜力的药物获得了孤儿药资格,代表着一个又一个“难治”的癌症适应症,终于有望迎来新的“解决方案”。
获批的新药当中,最值得重视的是多斯塔利单抗。8月18日,这款PD-1抑制剂获批了实体瘤的适应症,正式成为了第四款正式上市的“广谱抗癌药”,以及继派姆单抗之后的第二款获批实体瘤的PD-1抑制剂。
01、派姆单抗获批肾细胞癌一线治疗适应症,免疫+靶向再下一城
药物名称:派姆单抗(Pembrolizumab,Keytruda)+乐伐替尼(Lenvatinib,Lenvima)
简介:这是派姆单抗与乐伐替尼这对“搭档”获批的第二个适应症,也是这一组合至少十大适应症当中的一种。派姆单抗与乐伐替尼的组合的获批或在研适应症横跨非小细胞肺癌、胃癌、肝癌、胆管癌、子宫内膜癌、大肠癌、黑色素瘤、头颈癌、尿路上皮癌等多类实体瘤。
适应症:一线治疗晚期肾细胞癌成年患者
日期:2021年8月12日
状态:批准
相关阅读:派姆单抗获批肾细胞癌一线治疗适应症,免疫+靶向再下一城!
相关临床试验及数据:
【CLEAR/KEYNOTE-581试验】接受派姆单抗+乐伐替尼治疗的患者中位无进展生存期23.9个月,接受依维莫司+乐伐替尼治疗的患者中位无进展生存期14.7个月,接受舒尼替尼单药治疗的患者中位无进展生存期为9.2个月。
接受派姆单抗+乐伐替尼治疗的患者整体缓解率为71%,其中完全缓解率高达16.1%;接受依维莫司+乐伐替尼治疗的患者整体缓解率为53.5%,接受舒尼替尼治疗的患者整体缓解率为36.1%。
派姆单抗+乐伐替尼治疗患者中位缓解持续25.8个月,依维莫司+乐伐替尼治疗中位缓解持续16.6个月,舒尼替尼单药治疗中位缓解持续14.6个月。
02、又一款全癌种抗癌药获批,疾病缓解3年
药物名称:多斯塔利单抗(Dostarlimab-gxly,Jemperli)
简介:多斯塔利单抗是一款PD-1抑制剂,也是继派姆单抗之后第二款获批了实体瘤适应症的PD-1抑制剂。
适应症:错配修复缺陷(dMMR)的复发或晚期实体瘤成年患者
日期:2021年8月18日
状态:加速批准
相关阅读:又一款全癌种抗癌药获批,疾病缓解3年!有哪些不限癌种的抗癌新药?
相关临床试验及数据:
【GARNET试验】在dMMR的实体瘤患者中多斯塔利单抗取得了41.6%的出色缓解率,其中包括了超过9%的完全缓解率;除此以外,超过95.4%的患者缓解持续了半年以上,中位缓解持续时间长达34.7个月,接近3年。
03、无病生存期翻倍!纳武单抗辅助治疗尿路上皮癌新适应症获批
药物名称:纳武单抗(Nivolumab,Opdivo)
简介:纳武单抗是一款经典的PD-1抑制剂。
适应症:辅助治疗根治性切除术后复发风险高的尿路上皮癌患者,无论患者是否接受过新辅助化疗、是否存在淋巴结受累或PD-L1状态如何
日期:2021年8月20日
状态:批准
相关阅读:无病生存期翻倍!纳武单抗辅助治疗尿路上皮癌新适应症获批
相关临床试验及数据:
【CheckMate-274试验】术后接受纳武单抗辅助治疗的患者,中位无病生存期为20.8个月,几乎达到了接受安慰剂治疗的患者的10.8个月的两倍。尤其在PD-L1表达≥1%的患者当中,纳武单抗方案的优势更加明显,患者疾病复发或死亡的风险降低了45%。
04、胆管癌新药获批,22%的患者无进展生存期超过1年
药物名称:Ivosidenib(Tibsovo,IVO,AG-120)
简介:Ivosidenib(IVO,AG-120)是一款靶向IDH1突变的药物,曾于2018年7月获得FDA批准用于治疗IDH1阳性的复发或难治性急性髓细胞白血病。
适应症:曾接受过前线方案治疗的IDH1突变阳性胆管癌患者
日期:2021年8月26日
状态:批准
相关阅读:胆管癌新药Ivosidenib获FDA批准,22%的患者无进展生存期超过1年!
相关临床试验及数据:
【ClarIDHy试验】使用Ivosidenib治疗胆管癌,患者的中位无进展生存期为2.7个月,超过了安慰剂的1.4个月。此外,Ivosidenib治疗的6个月无进展生存率为32%,12个月无进展生存率为22%;而安慰剂治疗的患者分别为0%和0%。
除了新获批的药物以外,还有一部分新药获得了孤儿药、快速通道等称号或资格,代表着它们的潜力得到了FDA的认可,未来发展受到了重视。
其中一部分药物,非常有希望填补现有的治疗空白,让一部分患者取得更好的治疗效果。
01、粘膜黑色素瘤新药进入快速通道
药物名称:Nemvaleukin Alfa
简介:Nemvaleukin Alfa是一种白细胞介素-2(IL-2)变体免疫疗法。
适应症:粘膜黑色素瘤
日期:2021年8月3日
状态:快速通道
相关阅读:暂无
相关临床试验及数据:
【ARTISTRY-6试验】正在进行临床试验。
02、超过60%的患者无病生存3年!阿特珠单抗进军肺癌辅助治疗领域
药物名称:阿特珠单抗(Atezolizumab,Tecentriq)
简介:阿特珠单抗是一款经典的PD-L1抑制剂。
适应症:PD-L1表达水平≥1%的非小细胞肺癌患者,作为手术或铂类化疗后的辅助治疗方案
日期:2021年8月3日
状态:优先审查
相关阅读:超过60%的患者无病生存3年!阿特珠单抗进军肺癌辅助治疗领域!
相关临床试验及数据:
【IMpower010试验】接受阿特珠单抗治疗的患者,3年无病生存率为60.6%,最佳支持治疗的患者仅为48.2%。
03、九个靶点的"神药"又有新适应症了!拉博替尼治疗甲状腺癌获FDA优先审查
药物名称:卡博替尼(Cabozantinib,Cabometyx)
简介:卡博替尼是一款靶向治疗药物,可以作用于9类靶标。
适应症:12岁及以上的分化型甲状腺癌患者,这些患者应在前线治疗后进展且放射性碘难治
日期:2021年8月5日
状态:优先审查
相关阅读:九个靶点的“神药”又有新适应症了!拉博替尼治疗甲状腺癌获FDA优先审查
相关临床试验及数据:
【COSMIC-311试验】接受安慰剂治疗的患者,无进展生存期仅仅维持了1.9个月,而接受卡博替尼治疗的患者,仍有超过半数保持无进展,根据目前的随访时间判断,中位无进展生存期已经超过了6.2个月。总生存期方面,卡博替尼治疗同样也为更多患者争取了更长的总生存期。
除此以外,研究者表示,接受卡博替尼治疗的意向性治疗人群中,76%的患者病灶大小有缩小,而接受安慰剂的患者中仅有29%。
04、派姆单抗又迎黑色素瘤辅助治疗新适应症,已获FDA优先审查资格
药物名称:派姆单抗(Pembrolizumab,Keytruda)
简介:派姆单抗是最经典的PD-1抑制剂之一。
适应症:接受完全切除手术后的Ⅱb/c期黑色素瘤成年及儿童患者的辅助治疗
日期:2021年8月6日
状态:优先审查
相关阅读:派姆单抗又迎黑色素瘤辅助治疗新适应症,已获FDA优先审查资格
相关临床试验及数据:
【KEYNOTE-716试验】即将公开。
05、罕见肿瘤也有新希望!软组织肉瘤新药Sotigalimab获孤儿药称号
药物名称:Sotigalimab(APX005M)
简介:Sotigalimab是一款新型人源化抗CD40单克隆抗体,目前正处于Ⅱ期临床试验阶段。CD40是一种位于抗原呈递细胞表面的共刺激受体,能够同时激活先天性免疫系统和适应性免疫系统。因此,Sotigalimab在与抗原呈底细胞上的CD40结合后,可以发挥免疫增强的效果,诱导多种免疫反应,促使免疫系统的多个功能发挥作用,攻击癌细胞。
适应症:软组织肉瘤
日期:2021年8月6日
状态:孤儿药
相关阅读:罕见肿瘤也有新希望!软组织肉瘤新药Sotigalimab获孤儿药称号!
相关临床试验及数据:
【NCT03719430】正在进行临床试验。
06、派姆单抗辅助治疗肾细胞癌患者适应症获优先审查
药物名称:派姆单抗(Pembrolizumab,Keytruda)
简介:派姆单抗是最经典的PD-1抑制剂之一。
适应症:辅助治疗肾切除术后的肾细胞癌患者,这些患者在肾切除术后具有中高或高复发风险,或有转移病灶
日期:2021年8月10日
状态:优先审查
相关阅读:暂无
相关临床试验及数据:
【KEYNOTE-564试验】接受派姆单抗辅助治疗的患者,12个月和24个月无病生存率分别为85.7%和77.3%,接受安慰剂的患者分别为76.2%和68.1%。
07、近90%的患者生存期超过2年!特瑞普利单抗获FDA鼻咽癌突破性疗法称号
药物名称:特瑞普利单抗(Toripalimab)+吉西他滨+顺铂
简介:特瑞普利单抗是一款我国自主研发的PD-1抑制剂,目前已经在国内获批上市。
适应症:一线治疗复发或转移性鼻咽癌患者
日期:2021年8月13日
状态:突破性疗法
相关阅读:近90%的患者生存期超过2年!特瑞普利单抗获FDA鼻咽癌突破性疗法称号
相关临床试验及数据:
【JUPITER-02试验】接受特瑞普利单抗联合方案治疗的患者,中位无进展生存期为11.7个月,明显超过了吉西他滨+顺铂方案治疗的8.0个月。在1年无进展生存率方面,特瑞普利单抗联合方案同样优势显著(49.4% vs 27.9%)。
接受特瑞普利单抗联合方案治疗的患者中,生存期超过了1年和2年的患者分别达到了91.6%和87.1%;而接受吉西他滨+顺铂方案治疗的患者中,这两项数值仅有77.8%和63.3%。
在整体缓解率(77.4% vs 66.4%)和中位缓解持续时间(10.0个月 vs 5.7个月)方面,特瑞普利单抗方案的优势同样非常显著。
08、用另一种类型的药物抗KRAS!国研新药获FDA快速通道资格
药物名称:IN10018
简介:IN10018是一款高效的选择性ATP竞争性的FAK小分子抑制剂,目前正在美国、澳大利亚和中国进行临床试验与开发。
适应症:铂耐药的卵巢癌患者
日期:2021年8月17日
状态:快速通道
相关阅读:用另一种类型的药物抗KRAS!国研新药获FDA快速通道资格!
相关临床试验及数据:
正在进行临床试验。
09、新药获FDA孤儿药称号,这部分骨髓瘤患者即将迎来新药
药物名称:CFT7455
简介:CFT7455属于一类被称为MonoDAC的全新口服药物,靶向IKZF1/3,目前已经被证实在多发性骨髓瘤、非霍奇金淋巴瘤、外周T细胞淋巴瘤和套细胞淋巴瘤等多类血液系统肿瘤的治疗中具有良好的潜力。
适应症:多发性骨髓瘤
日期:2021年8月17日
状态:孤儿药
相关阅读:新药获FDA孤儿药称号,这部分骨髓瘤患者即将迎来新药
相关临床试验及数据:
【临床前研究】使用CFT7455来处理间变性大细胞淋巴瘤细胞,仅6小时,就能使IKZF1蛋白水平锐减89%。
10、治疗超过5线,缓解率仍可达到60%!新型CAR-T疗法获FDA孤儿药称号
药物名称:ALLO-715
简介:ALLO-715是一款CAR-T细胞疗法
适应症:多发性骨髓瘤
日期:2021年8月17日
状态:孤儿药
相关阅读:治疗超过5线,缓解率仍可达到60%!新型CAR-T疗法获FDA孤儿药称号!
相关临床试验及数据:
【UNIVERSAL研究】整体缓解率60%。
11、用药8周,肿瘤缩小超过90%!胰腺癌新靶点药物获FDA孤儿药资格
药物名称:LP-184
简介:LP-184是一款作用于DNA修复途径,即核苷酸切除修复(NER)和同源重组(HR)途径的药物。存在修复缺陷的癌症,包括相关基因(BRCA1、BRCA2、ATM、ATR、ERCC2、ERCC3、ERCC4、ERCC5、ERCC6、FANCD2、RAD51和PALB2等)突变或缺陷的癌症患者,都是这款药物的潜在获益人群。
适应症:胰腺癌
日期:2021年8月11日
状态:孤儿药
相关阅读:用药8周,肿瘤缩小超过90%!胰腺癌新靶点药物获FDA孤儿药资格
相关临床试验及数据:
正在进行临床试验。
12、妇瘤新ADC药物进入快速通道
药物名称:STRO-002
简介:STRO-002是一款靶向叶酸受体α(FolRα)的抗体-药物偶联物(ADC)。
适应症:曾接受过1~3线全身治疗的铂耐药性卵巢上皮癌、输卵管癌或原发性腹膜癌患者
日期:2021年8月18日
状态:快速通道
相关阅读:暂无
相关临床试验及数据:
【STRO-002-GM1试验】整体缓解率32.3%,其中完全缓解率3%。
13、慢粒白血病新药获FDA优先审查,反应率翻倍
药物名称:Asciminib(ABL001)
简介:Asciminib是一款由诺华(Novartis)研发的靶向治疗新药,主要作用于ABL肉豆蔻酰口袋,也被称为STAMP抑制剂。
适应症:慢性粒细胞白血病
日期:2021年8月26日
状态:优先审查
相关临床试验及数据:
【ASCEMBL试验】接受Asciminib治疗的患者,主要分子学反应率为25.5%,远超过了Bosutinib治疗患者的13.2%。
14、四十年来首个突破!葡萄膜黑色素瘤新药已提交申请
药物名称:Tebentafusp(IMCgp100)
简介:Tebentafusp是一款新型双特异性蛋白,由能够与CD3结合的抗体结构以及T细胞抗原受体T细胞(抗原)受体(T cell receptor,TCR)共同组成。
适应症:HLA-A*02:01阳性的转移性葡萄膜黑色素瘤
日期:2021年8月24日
状态:提交申请
相关临床试验及数据:
【IMCgp100-202试验】接受Tebentafusp治疗的患者,中位总生存期为21.7个月,而使用派姆单抗或伊匹木单抗方案治疗的患者,中位总生存期为16.0个月。从比例上来说,接受Tebentafusp治疗的患者1年生存率为73.2%,接受派姆单抗或伊匹木单抗治疗的患者1年生存率为58.5%。
15、LP-184获FDA胶质母细胞瘤及其它恶性胶质瘤孤儿药资格
药物名称:LP-184
简介:LP-184是一款作用于DNA修复途径,即核苷酸切除修复(NER)和同源重组(HR)途径的药物。存在修复缺陷的癌症,包括相关基因(BRCA1、BRCA2、ATM、ATR、ERCC2、ERCC3、ERCC4、ERCC5、ERCC6、FANCD2、RAD51和PALB2等)突变或缺陷的癌症患者,都是这款药物的潜在获益人群。
适应症:多形性胶质母细胞瘤及其它恶性胶质瘤患者
日期:2021年8月31日
状态:孤儿药
相关阅读:LP-184获FDA胶质母细胞瘤及其它恶性胶质瘤孤儿药资格
相关临床试验及数据:
正在进行临床试验。
扫描进患者病友群

肺癌|胃癌|肝癌|结直肠癌|胰腺癌
乳腺癌|脑瘤|淋巴瘤|儿童肿瘤等

相关推荐
253例真实世界研究证实:益生菌联合IC
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
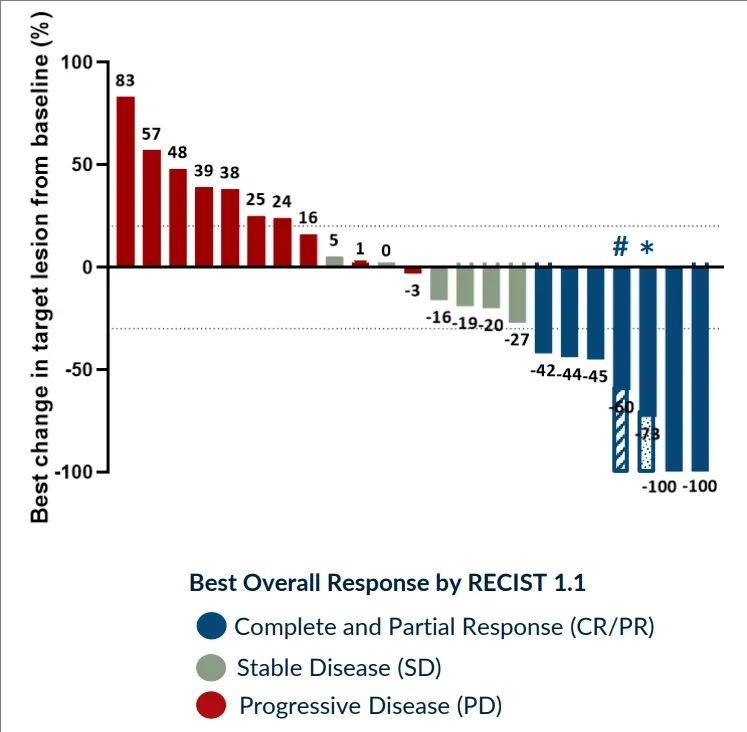
打一针激活抗癌免疫!肝癌治疗性疫苗大盘点
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
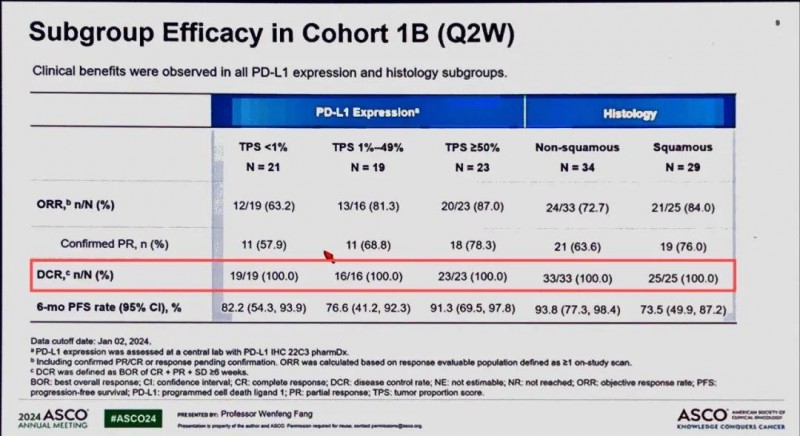
疾病控制率高达100%!2025奥希耐药
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

【mRNA癌症疫苗免费招募】Vx-001
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05

肝癌"黄金拍档"再发
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05
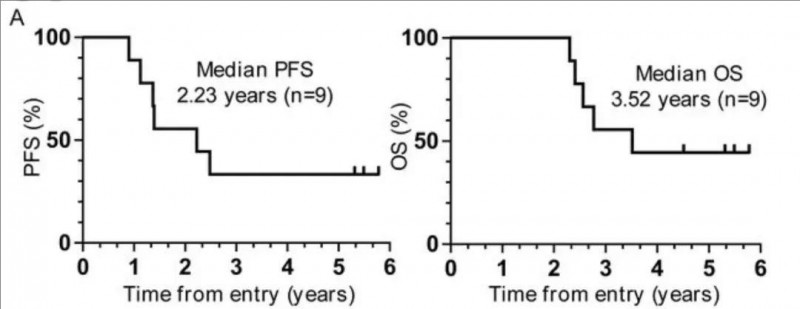
胰腺癌治疗性疫苗大盘点!最长OS超3年,
EGFR突变型患者在非小细胞肺癌中约占30%,在欧美患者中约占10%~20%,在亚洲患者中占比超过50%,是非小细胞肺癌的第二大致癌驱动因素。...
全球肿瘤医生网 2020-08-05






![[field:title/]](/uploads/allimg/20200224/1-2002241I5262J.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241I3461D.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H94LK.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241HKW34.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H619327.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H34H52.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241H22IH.jpg)
![[field:title/]](/uploads/allimg/20200224/1-2002241G93O18.jpg)




